Ближайшие результаты эндоваскулярной реперфузии миокарда в сравнении с только медикаментозным лечением больных с q-образующим острым инфарктом миокарда
Мачитидзе Екатерина Цезаревна
« Ближайшие результаты эндоваскулярной реперфузии миокарда в сравнении с только медикаментозным лечением больных с Q-образующим острым инфарктом миокарда »
14.01.05 - кардиология
медицинские науки
Д 850.018.01
101 000, Москва, Сверчков пер., д.5.
Предполагаемая дата защиты 11 марта 2010 года.
Выставлено на сайт -
Автореферат (Документ Word - 1470 kb)
На правах рукописи
Мачитидзе Екатерина Цезаревна
«Ближайшие результаты эндоваскулярной реперфузии миокарда в сравнении с только медикаментозным лечением больных с Q-образующим острым инфарктом миокарда»
14.01.05 – Кардиология
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва 2010
Работа выполнена в Научно- практическом центре интервенционной кардиоангиологии Департамента здравоохранения города Москвы
Научный руководитель:
Доктор медицинских наук, профессор Иоселиани Давид Георгиевич
Официальные оппоненты:
Доктор медицинских наук, профессор Чукаева Ирина Ивановна
Доктор медицинских наук, профессор Руда Михаил Яковлевич
Ведущая организация:
Московский областной научно-исследовательский клинический институт
им. М.Ф. Владимирского МЗ РФ
Защита диссертации состоится «_11___» __марта________ 2010 года в _14____ часов
на заседании Диссертационного совета Д 850.018.01 Научно- практического центра интервенционной кардиоангиологии Департамента здравоохранения города Москвы по адресу:
101 000, Москва, Сверчков пер., д.5.
С диссертацией можно ознакомиться в библиотеке Научно-практического центра интервенционной кардиоангиологии
Автореферат разослан " " 2010 года.
Ученый секретарь Диссертационного совета
Кандидат медицинских наук Чернышева И. Е.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Ишемическая болезнь сердца, в частности острый инфаркт миокарда (ОИМ), является главной причиной среди сердечно - сосудистых заболеваний, приводящей к высокой летальности и инвалидизации населения. Несмотря на значительные успехи в диагностике и лечении этого заболевания, госпитальная смертность в России остается высокой (18%), тогда как в большинстве стран Европы и США этот показатель составляет примерно 10-12%. Между тем, более широкое использование современных высокотехнологических методов диагностики и лечения ОИМ способствовало бы улучшению ближайших и отдаленных результатов этого заболевания. К примеру, некоторые исследователи утверждают, что ургентная эндоваскулярная реперфузия миокарда значительно улучшает прогноз больных и снижает как госпитальную, так и отдаленную летальность. Подтверждением может служить и тот факт, что благодаря широкому использованию эндоваскулярных методов диагностики и лечения ОИМ, в Научно-практическом центре интервенционной кардиоангиологии г.Москвы за последние десять лет удалось снизить госпитальную летальность с 13% до 4-5% в год (Рис.1). Несмотря на это, в России преобладающим методом лечения остается только консервативная лекарственная терапия. Например, баллонную ангиопластику и стентирование в России получают лишь около 1% пациентов с ишемической болезнью сердца (ИБС), хотя многие клиники нашей страны обладают возможностями рентгенохирургических методов диагностики и лечения острого инфаркта миокарда, и тем не менее, довольствуются только медикаментозными методами лечения этого заболевания. Поэтому, Следовательно, с позиции доказательной медицины, необходимо дальнейшее накопление положительного опыта эндоваскулярной реперфузии миокарда у больных ОИМ сравнивая его с результатами общепринятого медикаментозного (консервативного) лечения этого заболевания.
Все вышеизложенное явилось поводом для проведения данного исследования, целью которого явилась сравнительная оценка госпитального течения и прогноза больных с Q - образующим ОИМ при эндоваскулярной
реперфузии миокарда в остром периоде заболевания, с одной стороны, и при медикаментозной терапии только, с другой. В остальном тактика диагностики и лечения этих двух групп больных существенно не отличалась.

Рис.1. Динамика летальности от ОИМ в зависимости от количества проведенных эндоваскулярных процедур (в НПЦИК).
Задачи исследования:
- Изучить госпитальные результаты эндоваскулярного лечения больных с Q-образующим ОИМ по следующим показателям: общей и кардиальной летальности; рецидиву ИМ; возобновлению ранней постинфарктной стенокардии; развитию аритмий; недостаточности кровообращения.
- Изучить госпитальные результаты аналогичных больных при только медикаментозном лечении по названным выше показателям.
- Провести сравнительный анализ полученных данных в двух изученных группах больных.
Научная новизна. Впервые на основе комплексного анализа инструментальных и клинических данных проведена сравнительная оценка результатов медикаментозного и эндоваскулярного лечения идентичных больных с Q - образующим острым инфарктом миокарда и доказано достоверное преимущество эндоваскулярной реперфузии миокарда перед консервативным лечением в отношении выживаемости и снижения риска развития грозных осложнений на госпитальном этапе лечения. Практическая значимость. Проведенное исследование убедительно показало необходимость широкого использования реперфузии миокарда в первые часы заболевания у больных с Q - образующим инфарктом миокарда в отношении снижения летальности и других грозных осложнений. Уточнена тактика лечебных мероприятий, в которой важное место заняла диагностика состояния коронарного русла и миокарда, также как эндоваскулярная реперфузия миокарда с последующей активной дезагрегантной терапией.
Положения, выносимые на защиту:
- Клиническое течение заболевания и прогноз больных, перенесших Q - образующий ОИМ, зависит от выбранной тактики лечения.
- Чрескожная эндоваскулярная реперфузия является эффективным и безопасным методом лечения Q-образующего ОИМ, в результате которой достоверно cнижается госпитальная летальность и частота других грозных осложнений, а также улучшается функциональная способность левого желудочка. Этот метод лечения Q - образующего инфаркта миокарда имеет существенное преимущеcтво перед консервативным медикаментозным лечением.
Внедрение. Основные результаты исследования внедрены в клиническую практику отделений Научно-практического центра интервенционной кардиоангиологии г. Москвы, ГКБ №7, №15, №81, НИИ скорой помощи им. Н.В.Склифосовского.
Публикации. По теме диссертации опубликованы 2 печатные работы.
Апробация диссертации состоялась 17 июня 2009года на совместном заседании кафедры факультетской терапии педиатрического факультета Российского Государственного Медицинского Университета Росздрава, Ученого Совета и межотделенческой конференции Научно- практического центра интервенционной кардиоангиологии. Диссертация рекомендована к защите.
Структура и объем работы. Диссертация состоит из введения, пяти глав (обзор научной литературы; клиническая характеристика больных и методы обследования, методы лечения; сравнительные результаты лечения; анализ летальности; обсуждение полученных результатов), выводов, практических рекомендаций, списка литературы, который включает 35 отечественных и 160 зарубежных источников. Работа изложена на 115 страницах, содержит 17 таблиц и иллюстрирована 27 рисунками.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Клиническая характеристика больных и методы исследования.
В исследование вошли 864 больных с Q-образующим острым инфарктом миокарда, получивших лечение в НПЦИК с 2004 г. по 2007 г.
В зависимости от тактики лечения, все больные ОИМ были разделены на 2 группы. В 1 группу вошли 529 (61,2%) больных, которым наряду с общепринятыми методами диагностики и лечения, на стационарном этапе выполнялись ургентная или полуургентная селективная коронароангиография и лечебные эндоваскулярные процедуры, направленные на реперфузию миокарда. В подавляющем большинстве случаев (70,3%) эти процедуры выполняли ургентно в первые часы заболевания - до 24 ч от начала ангинозного приступа. У остальных пациентов процедуры выполнялись отсрочено - в более поздние сроки стационарного лечения - от 2 до 21 дня. Показанием для проведения отсроченных процедур являлись ранняя постинфарктная стенокардия или другие клинико-лабораторные признаки продолжающейся гипоксии миокарда.
2 группу составили 335 (38,8%) больных с Q- образующим ОИМ, которым по тем или иным причинам не выполнялись селективная коронароангиография и эндоваскулярные лечебные процедуры (отказ больных от исследования, непереносимость йода, входящего в состав рентгеноконтрастных препаратов, отсутствие функционирующей ангиографической службы во время отпускного периода и некоторых праздничных дней).
По основным исходным клинико- лабораторным и анамнестическим данным сравниваемые группы больных между собой достоверно не различались (Таблица 1). Средний возраст пациентов в первой группе составил 54,6±9,2 лет, во второй группе - 56,1±10,3лет. В обеих группах преобладали лица мужского пола - 86,2% и 81,6% соответственно. В первой группе было незначительно большее количество больных с системным тромболизисом (18,9 % против 12,2 %).
Таблица 1 Исходные клинические показатели
| ПОКАЗАТЕЛЬ | 1ГРУППА эндоваскулярное лечение (n=529) | 2ГРУППА медикаментозное лечение (n =335) | Р |
| Возраст, годы Мужской пол Артериальная гипертензия Курение Сахарный диабет Гиперхолестеринемия ИМ в анамнезе Стенокардия в анамнезе Дебют ИБС Системная ТЛТ ФВ ЛЖ, % Острая аневризма сердца Время,прошедшее от начала заболевания до начала терапии до 24 часов: < 6 часов 6-24 часа более 24 часов | 54,6±9,2 456(86,2%) 346(65,4%) 328(62%) 60(11,3%) 342(64,7%) 78(14,7%) 163(30,9%) 288 (54,4%) 100(18,9%) 52,6±12,2 86(16,2 %) 372(70,3%) 209(39,5%) 163(30,8%) 157(29,7%) | 56,1±10,3 273(81,5%) 239(71,3%) 186(55,5%) 40(11,7%) 201(60,0%) 65(19,4%) 94(28,1%) 176 (52,5 %) 41(12,2%) 49±12,9 67(20,0 %) 245(73,1%) 125(37,3%) 120(35,8%) 90(26,9%) | >0,05 >0,05 >0,05 <0,05 >0,05 >0,05 >0,05 >0,05 >0,05 <0,05 >0,05 >0,05 >0,05 >0,05 >0,05 >0,05 |
Наибольшее число пациентов поступило в сроки до 24 часов от начала заболевания ( около 72,0% ), из них - около 54,0%- в сроки до 6 часов.
У большинства пациентов первой группы, поступивших в ранние сроки ОИМ, выявляли острую окклюзию инфаркт-ответственной артерии (ИОА), тогда как, у пациентов, поступивших в более поздние сроки, причиной ОИМ чаще являлась субтотальная окклюзия ИОА.
Инфаркт миокарда наиболее часто наблюдали в бассейне ПМЖВ и ПКА (260 / 49,2% и 166 / 31,4 %), далее - ОВ ( 58 / 11,0%), ДВ ( 25 / 4,7%), ВТК (17/3,2%), ствол ЛКА ( 3 / 0,5% ). Чаще наблюдали поражения проксимального и среднего сегментов ИОА.
Диагноз ОИМ устанавливали на основании критериев ВОЗ, исходя из совокупности клинических данных, результатов электрокардиографического исследования, патологического увеличения концентрации кардиоспецифических ферментов в крови и наличия зон асинергии при эхокардиографическом исследовании (в случае отсутствия у этих больных ОИМ в анамнезе).
В отделении кардиореанимации больным с ОИМ в соответствии с имеющимся в НПЦИК протоколом проводилось лечение, включающее инфузионную терапию нитратами, антикоагулянтами (гепарин), препаратами блокирующими -адренергические рецепторы, дезагрегантами, ингибиторами АПФ, в части случаев антагонистами кальция.
Эндоваскулярные лечебные процедуры (ЭВП) на инфаркт-ответственной артерии выполнялись 529 пациентам, причем у 297 ( 56,1 % ) пациентов была выполнена процедура баллонной ангиопластики, еще у 165 ( 31,2 % ) - баллонная ангиопластика сочеталась c эндопротезированием инфаркт-ответственной артерии. В 67(12,7 %) случаях было выполнено стентирование прямым способом (Рис.2).

Рис.2. Эндоваскулярные лечебные процедуры на ИОА.
Всего этим больным было выполнено 695 эндоваскулярных лечебных процедур. Из них 621 (89, 4 %) эндоваскулярное вмешательство было выполнено только на ИОА ( у 472 (89,2%) больных ), тогда как еще 74 (10,6%) эндоваскулярных процедур ангиопластики было выполнено на других коронарных артериях ( у 57 (10,8%) больных была достигнута полная реваскуляризация миокарда ).
В работе использовали следующие методы исследования:
1.Анамнез заболевания и жизни.
2.Электрокардиографическое исследование в 12-ти стандартных отведениях.
3.Суточное мониторирование ЭКГ. При анализе данных использовали показатели суммарного времени и глубины смещения интервала ST и суммарного времени инверсии зубца T, нарушения ритма оценивали по классификации Лауна.
4.Велоэргометрическую пробу проводили по методике ступенеобразно возрастающих нагрузок. Нагрузку начинали с мощности 150 кг м/мин (25 Вт), в дальнейшем каждые 3 минуты нагрузку увеличивали на 150 кг м/мин. За весь период исследования и в течение 5 минут восстановительного периода проводили непрерывный мониторинг и регистрацию ЭКГ. Пробу оценивали как положительную, если на высоте нагрузки у пациента развивался ангинозный приступ в сочетании или без ЭКГ- признаков депрессии или элевации сегмента ST более чем на 1 мм от изолинии; отрицательной - в случае достижения субмаксимальной ЧСС при отсутствии боли и ишемических изменений на ЭКГ. Во всех остальных случаях проба считалась неинформативной. При оценке толерантности к физической нагрузке использовали 3 градации: низкая (при достижении мощности не более 25-75 Вт); средняя (между 75-125 Вт); высокая (от 125Вт и более).
5.Эхокардиография. Посредством метода изучали следующие показатели: размеры камер сердца в систолу и диастолу, толщину миокарда ЛЖ, ударный объем ЛЖ, фракцию выброса, степень асинергии миокарда, наличие патологических потоков. Кинетику стенок ЛЖ изучали из парастернального и апикального доступов (по длинной и короткой осям и 2-х и 4-х камерных позициях, соответственно). Конечно-диастолический и конечно- систолический объемы рассчитывали по формуле площадь-длина в модификации Simpson из апикальной позиции в проекции длинной оси ЛЖ.
6.Селективная коронароангиография и левая вентрикулография выполнялись по методике M.Judkins (1967). Анализ общей и сегментарной сократимости ЛЖ проводили по методу Липтона. При этом, выделяли 5 сегментов: 1- передне-базальный, 2 - передне-латеральный, 3 - верхушечный, 4 - задне-диафрагмальный, 5 - задне-базальный. При коронароангиографии сначала контрастировали систему ЛКА, а затем - систему ПКА. Обычно для оценки состояния ЛКА использовали 4 - 6 проекций, для диагностики поражения ПКА - 3 - 5 проекций. Использовали следующие характеристики поражения коронарных артерий: 1) гемодинамически незначимый стеноз (<50%); 2) гемодинамически значимый стеноз (>50%); 3)окклюзия. Эндоваскулярные процедуры выполняли по общепринятой методике. Критериями оптимального непосредственного ангиографического успеха считали отсутствие выраженной диссекции интимы (типа С-F) и дистальной эмболизации; остаточный стеноз до 30% для пациентов с транслюминальной баллонной ангиопластикой (ТЛАП) и до 10-20% в случае стентирования; восстановление антеградного кровотока TIMI 2-3.
Статистическая обработка результатов исследования проводилась с помощью стандартных непараметрических методов статистики: критерия Манна-Уитни сравнения средних значений, корреляционного анализа по Спирмену (различия считались достоверными при p < 0,05, что в таблице Стьюдента соответствует 95% достоверности), для оценки статистической значимости различий при малом числе наблюдений использовался точный критерий Фишера.
Результаты исследования и их обсуждение
В 1 группе непосредственный ангиографический успех выполненных ЭВП составил 92,4% (489 пациентов). Среди осложнений, связанных непосредственно с ЭВП, в 21 (4,0 %) случае отмечали тромбоз/реокклюзию ИОА: в 1 ( 0,2 % ) случае в результате наступила смерть больного, в 8 (1,5 %) случаях развился нефатальный рецидив ИМ. Ещё у 12 ( 2,2 % ) пациентов с затяжным ангинозным приступом и субокклюзией ИОА данных за повреждение миокарда не получено. Всем 20 ( 3,8 % ) пациентам с тромбозом ИОА и 9 ( 1,7 % ) пациентам с клиникой нестабильной стенокардии и угрожающей диссекцией сосуда после первичной ангиопластики проведены успешные повторные ЭВП в экстренном порядке с восстановлением антеградного кровотока TIMI 3 и последующим неосложненным течением заболевания. В 11(2,1%) случаях стентирование ИОА сопровождалось дистальной эмболизацией (Таблица 2).
Таблица 2
Осложнения и ургентные ЭВП в ближайшем послеоперационном периоде
| Показатели | Группа 1 (n=529) |
| Дистальная эмболизация | 11 (2,1%) |
| Тромбоз/реокклюзия ИОА (всего) | 21 (4,0%) |
| Нефатальный рецидив ИМ | 8 (1,5%) |
| Затяжной ангинозный приступ- (субокклюзия ИОА) | 12 (2,2%) |
| Смерть | 1 (0,2%) |
| Нестабильная стенокардия (ангиографически - угрожающая диссекция сосуда) | 9 (1,7%) |
| Экстренная повторная ТЛАП ИОА | 29 (5,5%) |
Клинические результаты исследования оценивали на основании данных по летальности, рецидивам ИМ, постинфарктной стенокардии, прогрессированию недостаточности кровообращения и инсульта мозга. Информация о течении заболевания на госпитальном этапе в изученных группах представлена в таблице 3.
Таблица 3
Госпитальные результаты лечения в изученных группах
| Группа 1 (n=529) | Группа 2 (n=335) | Р | |
| Неосложненное течение заболевания | 436(82,4%) | 171(51,0% ) | 0,0001 |
| Осложненное течение заболевания: Приступы стенокардии Рецидив ИМ (нефатальный) НК ( Killip> Другие осложнения Летальность: Общая От кардиальных причин | 22(4,2%) 8(1,5%) 52(9,8%) 26(4,9%) 11(2,1%) 7(1,3%) | 50(15,0%) 25(7,5%) 50(15,0%) 13(3,9%) 39(11,6%) 35(10,5%) | 0,001 0,04 0,001 0,6 0,001 0,001 |
Неосложненное клиническое течение заболевания (без летальных случаев, рецидивов инфаркта миокарда, ранней постинфарктной стенокардии, прогрессирования недостаточности кровообращения, ОНМК, ТЭЛА) отмечали у 436(82,4%) пациентов 1 группы и 171(51,0%) пациента 2 группы (P<0,05),(Рис.3).

Рис.3. Неосложненное и осложненное клиническое течение заболевания на госпитальном этапе.
Раннюю постинфарктную стенокардию достоверно реже (4,2 %) наблюдали у пациентов первой группы, нежели во второй группе (15,0 %),(P=0,001), (Рис.4).

Рис.4.. Частота ранней постинфарктной стенокардии на госпитальном этапе.
Также реже наблюдали в первой группе случаи рецидива ИМ ( 1, 5 % ), чем во второй группе ( 7, 5 % ), (P=0,04),(Рис.5).
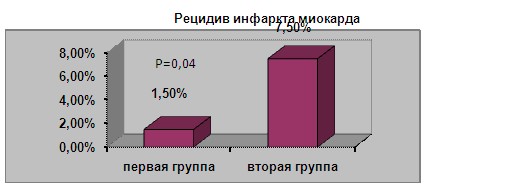
Рис.5. Частота рецидива инфаркта миокарда в изученных группах.
По таким показателям, как возникновение мерцательной аритмии и нарушений проводимости сердца, также была достоверна разница между сравниваемыми группами. Если в первой группе эти показатели были 4,5% и 7,4% соответственно, то во второй группе они были достоверно (P=0,001) выше (Рис.6).

Рис.6. Частота возникновения различных видов аритмии в сравниваемых группах.
В первой группе сердечная недостаточность составила 9,8 % и была достоверно ниже, чем во второй группе (15, 0 %),(P=0,001), (Рис.7).

Рис. 7. Частота клинических проявлений сердечной недостаточности в изученных группах.
Различались группы и по выраженности сердечной недостаточности (Рис.8).

Рис.8. Распределение больных по степени ЛЖ-недостаточности (согласно классификации Killip).
Сердечная недостаточность суммарно была более выражена во второй группе. Так, недостаточность II и III ФК во второй группе наблюдалась у 120
( 35,8 % ) больных, тогда как в первой группе - у 136 ( 25,7 % ) больных (p<0,05). К тому же, у 12, 9 % больных второй группы в острой фазе ИМ имел место отек легких, тогда как в первой группе это осложнение наблюдали лишь в 2, 6 % случаев. Кардиогенный шок также реже наблюдали в первой группе больных ( 0,6 % и 3,0 % соответственно, Р<0,05 ).
Таким образом, по частоте возникновения кардиальных осложнений имели место достоверные различия в пользу больных с эндоваскулярным лечением. Тоже можно сказать и о разрывах стенок миокарда ЛЖ. В нашем исследовании это осложнение наблюдалось в 0,4 % и 3, 6 % случаев соответственно в первой и во второй группах, (Таблица 4).
Таблица 4. Кардиальные осложнения в остром периоде ИМ
| Кардиальные осложнения в остром периоде ИМ | Эндоваскулярное лечение (n =529) | Медикаментозное лечение (n =335) | P |
| Нарушения ритма сердца | 82 (15,5%) | 83 (24,8%) | <0,05 |
| Нарушения проводимости сердца | 39 (7,4%) | 56 (16,7%) | <0,05 |
| Левожелудочковая недостаточность(I, II кл. по Killip); | 52 ( 9,8 % ) | 50 (15,0% ) | <0,05 |
| Отек легких | 14 ( 2, 6 % ) | 43 ( 12, 9 % ) | <0,05 |
| Кардиогенный шок | 3 ( 0, 6 % ) | 10 ( 3, 0 % ) | <0,05 |
| Разрыв миокарда | 2 ( 0, 4 % ) | 12 ( 3, 6 % ) | <0,05 |
По таким некардиальным осложнениям, как тромбоэмболия легочной артерии ( 0,2% - 1 группа, 0,9% - 2 группа ), желудочно-кишечное кровотечение ( 1,3% - 1 группа, 1,2% - 2 группа ), ишемический или геморрагический инсульт мозга ( 0,6% -1 группа, 1,8% - 2 группа ) достоверных различий между изученными группами найдено не было (Таблица 5).
Таблица 5
Некардиальные осложнения в изученных группах
| Показатели | Группа 1 (n=529) | Группа 2 (n=335) | Р |
| Цереброваскулярные осложнения (ОНМК) | 3 (0,6%) | 6 (1,8%) | >0,05 |
| Желудочно-кишечное кровотечение | 7 (1,3%) | 4 (1,2%) | >0,05 |
| Гематома в месте пункции | 7 (1,3%) | - | - |
| Тромбоэмболия легочной артерии | 1 (0,2%) | 3 (0,9%) | >0,05 |
| Аллергические реакции | 8 (1,5%) | - | - |
Данные суточного мониторирования ЭКГ также убедительно подтвердили эффективность эндоваскулярной реперфузии миокарда у больных с ОИМ. Так, у пациентов 1 группы достоверно реже наблюдали признаки транзиторной гипоксии миокарда, нежели у больных 2 группы. При этом, в первой группе
при суточном мониторировании ЭКГ данных за ишемию миокарда не было получено у 469 (90,0%) пациентов, тогда как во второй группе лишь у 201 (65, 3 %) больного (Рис.9).

Рис.9. Результаты суточного мониторирования ЭКГ на стационарном этапе в изученных группах.
Нагрузочные тесты, выполненные больным перед выпиской из стационара, также подтвердили преимущество метода эндоваскулярной реперфузии миокарда перед консервативным методом лечения ОИМ в отношении ликвидации гипоксии миокарда. В первой группе результаты нагрузочного теста были отрицательными у 193 (44,7%) пациентов, тогда как во второй группе - только у 49 ( 21, 8 % ) пациентов, p<0,05 (Рис.10). Максимальная (пороговая) мощность выполненной нагрузки в группе с ЭВП была выше 600-750 кг м/мин (100-125 Вт), тогда как в группе с только медикаментозным лечением этот показатель не превышал 450-600 кг м/мин (75-100 Вт).
 Рис. 10. Результаты нагрузочного тестирования (ВЭМ-проба, Тредмил- тест) больных перед выпиской из стационара в изученных группах.
Рис. 10. Результаты нагрузочного тестирования (ВЭМ-проба, Тредмил- тест) больных перед выпиской из стационара в изученных группах.
В целом общая летальность изученных пациентов на госпитальном этапе составила 5,8%, умерло 50 человек. В 42 (4,8%) случаях причина смерти была кардиологической и 8 (0,9%) случаях - не кардиологической. Анализ летальных исходов на госпитальном этапе в группах эндоваскулярного и медикаментозного лечения представлен в таблице 6.
Таблица 6
Анализ госпитальной летальности в изученных группах
| Показатель | 1ГРУППА (n=529) | 2ГРУППА (n=335) | Р<0,05 | ||
| 1Агруппа < 24 час (n=372) | 1Бгруппа 24 час -21 день (n=157) | 2Агруппа < 24 час (n=245) | 2Бгруппа 24 час -21 день (n=90) | ||
| Выживаемость | 518(97,9%) | 296(88,3%) | для 1Гр.-2Гр. | ||
| Летальность (общая) | 11(2,1%) | 39(11,6%) | для 1Гр.-2Гр. | ||
| 10(2,7%) | 1(0,6%) | 34(13,9%) | 5(5,6%) | для 1А-2А для 1Б-2Б | |
| Летальность (кардиальная) | 7(1,3%) | 35(10,5%) | для 1Гр.-2Гр. | ||
| 6(1,6%) | 1(0,6%) | 30(12,2%) | 5(5,5%) | для 1А-2А для 1Б -2Б | |
| Причины смерти: -кардиогенный шок - разрыв стенок миокарда - НК (Killip> -Фибрилляция желудочков -острая коронарная недостаточность в результате тромбоза стента/окклюзии ИОА | 1(2,0%) 2(4,0%) 2(4,0%) 1(2,0%) 1(2,0%) | 10(20,0%) 12(24,0%) 9(18,0%) 4(8,0%) - | Для 1 гр.- 2 гр. Для 1 гр.- 2 гр. Для 1 гр.- 2 гр. Для 1 гр.- 2 гр. - | ||
Как видно из представленных в таблице данных, во 2-ой группе были достоверно более высокие показатели летальности нежели в первой группе. Это касается как общей летальности, так и смерти от сердечных причин.
При этом, достоверность различий сохраняется как у пациентов, поступивших в стационар в первые 24 часа от начала заболевания (1,6% и 12,2% соответственно в изученных группах), так и у больных, поступивших в более поздние сроки ( 0,6% и 5,5%, P<0,05 ).
Основными причинами кардиальной летальности на госпитальном этапе были: кардиогенный шок - 2,0% в 1 группе и 20,0% во 2 группе; разрыв стенок левого желудочка с последующей тампонадой сердца - 4,0% в 1 группе и 24,0% во 2 группе; рефрактерная к лечению сердечная недостаточность- 4,0% в 1 группе и 18,0% во 2-ой; сложные нарушения ритма и проводимости - 2,0% в 1 группе и 8,0% во 2 группе. В 2,0% случаев в первой группе наблюдали тромбоз стента / окклюзию ИОА.
Другими, не кардиальными, причинами летальности были: тромбоэмболия легочной артерии - 4,0% во 2 группе; желудочно-кишечное кровотечение - 4,0% в 1 группе и 2,0% во 2 группе; ишемический или геморрагический инсульт мозга - 4,0 % в 1 группе и 2,0 % во 2 группе.
Для выявления факторов, могущих влиять на исход заболевания при ОИМ на госпитальном этапе, нами был проведен корреляционно - статистический анализ клинико-лабораторных и анамнестических данных этих пациентов. Анализу были подвергнуты такие показатели как возраст, пол, артериальная гипертензия, наличие сахарного диабета, перенесенный ранее ИМ, локализация поражения, наличие ранней постинфарктной стенокардии, рецидива ИМ, использованные методы лечения (медикаментозное или эндоваскулярное) с учетом сроков реваскуляризации.
Признаками, влияющими на неблагоприятный исход заболевания, по нашим данным, могут быть преклонный возраст, женский пол. Летальность среди женщин в целом была выше, чем среди мужчин, но в большей степени это касалось больных второй группы. Во 2 группе из 65 женщин умерло 10 (15,4%), из 270 мужчин - 29 (10,7%), в 1 группе из 70 женщин умерла 1 (1,4%), из 459 мужчин умерло 10 (2,2%), (р< 0,05). С увеличением возраста также имело место увеличение летальности больных. Наибольшая летальность отмечалась среди пациентов старше 60 лет во 2-ой группе больных (27 пациентов - 54,0%).
Более неблагоприятный прогноз в отношении летальности имели больные с анамнезом перенесенного инфаркта миокарда, т.е. с постинфарктным кардиосклерозом. Летальность среди пациентов с повторным ОИМ была более высокой в обеих группах - 14%, тогда как среди пациентов с первичным ИМ - 4,2%, р<0,05. При этом, во 2 группе эта закономерность была более выражена - 21,5% против 7,7% - в 1-ой группе больных (р<0,05).
При локализации инфаркта миокарда на передней стенке ЛЖ также повышается вероятность летального исхода (54% от всех летальных случаев).
Функциональное состояние левого желудочка играет крайне важную роль в выживании больных с ОИМ. Так, у пациентов с I степенью ЛЖ- недостаточности как в 1-ой, так и во 2-ой группах, летальность отсутствовала, тогда как у пациентов со II, III и IV - степенью ЛЖ-недостаточности, летальность составила соответственно в изученных группах 6% и 38%, p<0,05.
Особо следует отметить, что смертность при кардиогенном шоке в 1 группе составила 33,3%, а во второй группе - 100,0%, (p<0,05).
Таким образом, проведенное исследование убедительно показало, что при ОИМ, выполненная в первые часы заболевания эндоваскулярная реперфузия миокарда, способствует значительному улучшению ближайшего прогноза этих пациентов, что заключается в существенном снижении госпитальной летальности; рецидивов ОИМ; ликвидации приступов стенокардии и уменьшении частоты развития левожелудочковой недостаточности. Эффект реперфузии наблюдается как у пациентов, которым реперфузия была выполнена в первые часы, так и у пациентов, которым эта процедура выполнялась в более поздние сроки заболевания. Однако, эффект реперфузии тем более выражен, чем раньше она выполнена. Следовательно, необходимо стремиться к выполнению эндоваскулярной реперфузии миокарда у всех больных ОИМ, за исключением тех, у которых имеются на то четкие противопоказания.
ВЫВОДЫ
- Неосложненное клиническое течение на госпитальном этапе (без серьезных осложнений и летальных исходов) у больных с Q - образующим ОИМ при эндоваскулярной реперфузии миокарда наблюдали в 82,4% случаев, что примерно в 1,5 раза выше, чем у аналогичных пациентов при консервативном лечении (51,0%).
- Госпитальная летальность больных с Q - образующим ОИМ при эндоваскулярной реперфузии миокарда составила 2,1% и была достоверно ниже (в 5 раз), чем у аналогичных больных получивших только медикаментозную терапию (11,6%).
- Рецидив острого инфаркта миокарда на госпитальном этапе у больных с Q - образующим ИМ после эндоваскулярной реперфузии составил 1,5% и был достоверно меньше (в 5 раз), чем у пациентов только с медикаментозным лечением (7,5%).
- Ранняя постинфарктная стенокардия на госпитальном этапе наблюдалась у больных ОИМ после эндоваскулярной реперфузии миокарда в 4,2 % случаев и была примерно в 3,5 раза ниже, чем у аналогичных пациентов получивших консервативную терапию (15,0%).
- У пациентов с разной выраженностью левожелудочковой недостаточности летальность при только медикаментозной терапии составила 38%, что более чем в 6 раз превышает аналогичный показатель в группе больных получивших эндоваскулярную реперфузию миокарда (6%).
- Факторами риска неблагоприятного течения и госпитального исхода у больных ОИМ являлись женский пол, пожилой возраст (старше 60 лет), ИМ в анамнезе, передний ИМ, дисфункция ЛЖ (III и IV степень ЛЖ-недостаточности). Влияние вышеперечисленных факторов на показатели летальности в значительно большей степени прослеживалось в группе больных с медикаментозной терапией.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- У больных с Q - образующим ОИМ в первые часы заболевания следует стремиться к эндоваскулярной реперфузии миокарда с целью снижения летальности и других грозных осложнений на госпитальном этапе.
- У больных с Q - образующим ОИМ при возобновлении ранних приступов стенокардии на госпитальном этапе необходимо выполнение коронароангиографии и, при показаниях, эндоваскулярной реперфузии миокарда с целью предупреждения грозных осложнений.
Список работ, опубликованных по теме диссертации
- Е.Ц. Мачитидзе, С.В. Роган, С.П. Семитко, Д.Г.Иоселиани. Сравнительная оценка госпитальной летальности больных, перенесших эндоваскулярные лечебные процедуры в острой стадии ИМ, и получивших только консервативное лечение (без ЭВП). Третий Российский съезд интервенционных кардиоангиологов. Москва 2008г. Тезисы. Международный Журнал интервенционной кардиоангиологии, 2008, №14, стр. 67.
- Е.Ц. Мачитидзе, Д.Г.Иоселиани. Влияет ли на госпитальный прогноз больных с Q-образующим ОИМ эндоваскулярная реперфузия миокарда в первые часы заболевания? Международный Журнал интервенционной кардиоангиологии, 2009, №17, стр.11-14.
- Д.Г. Иоселиани, Е.Ц. Мачитидзе, И.Ю. Костянов, А.Г. Колединский.
Сравнительная оценка госпитального течения и исхода лечения больных с Q-образующим ОИМ при эндоваскулярной реперфузии миокарда и без нее. Журнал "Кардиология". Сдана в печать.

