Ускоренные режимы лучевой терапии больных раком молочной железы iib-iii стадии (
На правах рукописи
КУРНОСОВ
АЛЕКСАНДР АЛЕКСАНДРОВИЧ
УСКОРЕННЫЕ РЕЖИМЫ ЛУЧЕВОЙ ТЕРАПИИ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ IIB-III СТАДИИ
(14.00.14. - онкология,
14.00.19-лучевая диагностика, лучевая терапия)
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
МОСКВА — 2008
Работа выполнена в ГУ Российский онкологический научный центр им. Н.Н.Блохина РАМН (директор — академик РАН и РАМН, проф. М.И.Давыдов)
Научные руководители:
Д.м.н., профессор М. И. Нечушкин
Д.м.н. И.А. Гладилина
Официальные оппоненты:
доктор медицинских наук, профессор Титова В.А.
доктор медицинских наук Иванов В.М.
Ведущее учреждение:
ГУ Медицинский Радиологический Научный Центр РАМН
Защита диссертации состоится «……………..» 2008 г., в «…» часов на заседании диссертационного совета Д 001.017.01 при ГУ Российский онкологический научный центр им. Н.Н.Блохина РАМН (115478, Москва, Каширское шоссе, 24).
С диссертацией можно ознакомиться в библиотеке ГУ РОНЦ им. Н.Н.Блохина РАМН.
Автореферат разослан «……………………..» 2008 г.
Ученый секретарь диссертационного совета,
доктор медицинских наук, профессор Ю.В. Шишкин
Актуальность проблемы.
На сегодняшний день проблема лечения рака молочной железы (РМЖ) приобретает особенно большое значение в связи с неуклонным ростом заболеваемости, относительной неэффективностью предлагаемых профилактических и скрининговых программ, а также тем, что около половины больных впервые обращаются за медицинской помощью с достаточно запущенными формами заболевания - местно-распространенным раком [Летягин В.П. 2000, Нечушкин М.И. 2001]. Лечение данной категории пациенток достаточно сложно и многогранно. Эффективность лечения остается неудовлетворительной в связи с развитием в ближайшие годы после проведенного комплексного или комбинированного лечения отдаленных метастазов и местных рецидивов, которые влияют как на выживаемость, так и на качество жизни больных.
Принимая во внимание тот факт, что РМЖ является системным заболеванием даже на ранних стадиях процесса, в лечении больных широко используются комплексные программы лечения. Системное воздействие, включающее химиотерапию и гормонотерапию или их сочетание, отодвигает сроки и уменьшает вероятность развития рецидивов и дистанционных метастазов. [Bonadonna G., 1996]
Лучевая терапия (ЛТ), являясь методом локального воздействия, снижает риск возникновения местного рецидива с 35-32% до 8-9% что в свою очередь, по мнению многих авторов, может влиять в целом на выживаемость больных, улучшая показатели как общей так и безрецидивной выживаемости в целом на 10% [Overgaard M., Jensen M-J., Overgaard J., et al. 1999,Overgaard M., Hansen P.S., Overgaard J., et al. 1997].
Несмотря на большое число работ, касающихся адъювантной терапии, остаются нерешенные вопросы по использованию радиационного воздействия у больных с пораженными лимфатическими узлами (ЛУ) и пациенток местно-распространенным РМЖ, которым на хирургическом этапе планируется или произведена радикальная мастэктомия.
В настоящее время нет четких показаний по применению предоперационной ЛТ у больных РМЖ, а также недостаточно данных по степени ее влияния на местный контроль в сравнении с послеоперационным облучением. В последние годы много исследователей изучают влияние клинико-морфологических факторов прогноза на дальнейшее развитие заболевания, таких как инвазия опухолевыми клетками сосудистого русла, степень злокачественности опухоли, число пораженных ЛУ, размер опухоли, ее рецепторный статус, возраст пациенток и др. Однако на сегодняшний день не изучены вопросы индивидуального прогнозирования локорегионарных рецидивов, показаний и противопоказаний к ЛТ на основе прогностических факторов. До настоящего времени остаются нерешенные вопросы о целесообразности использования адьювантной ЛТ у пожилых пациенток, у больных с тяжелой сопутствующей патологией, а также у женщин, имеющих опухоли с низким риском рецидивирования [Pierce L. 2003].
В последние годы интенсивно изучаются вопросы рационального сочетания адъювантной лучевой и химиотерапии. Внедрение в клиническую практику новых комбинаций химиопрепаратов (таксаны) неоадъювантной и адъювантной химиотерапии, диктует необходимость изучения новых схем системного лечения в комбинации с ЛТ, с учетом прогностических факторов, методик и режимов радиационного воздействия [Citron M., Berry D., Cirrincione C., et al.2003].
Остается открытым вопрос по влиянию облучения на местный контроль и выживаемость у больных с количеством пораженных подмышечных ЛУ от одного до трех. В настоящее время активно изучаются вопросы влияния различных факторов прогноза на частоту метастазирования в парастернальный коллектор и целесообразности использования ЛТ на данную зону.
Таким образом, в настоящее время предметом клинических исследований является изучение течения заболевания в зависимости от
наличия неблагоприятных факторов прогноза, метода системного воздействия и проведенного лучевого лечения, разработка наиболее оптимальных режимов лучевого лечения в зависимости от стадии, факторов неблагоприятного прогноза, а также схем системной терапии, что подтверждает актуальность настоящего исследования.
Цель исследования.
Целью данного исследования является улучшение отдаленных результатов лечения больных РМЖ IIб-III стадий за счет оптимизации программ комплексного лечения с использованием ускоренных режимов ЛТ.
Задачи исследования.
1. Изучить отдаленные результаты лечения больных РМЖ IIб-III стадий с использованием предоперационной и послеоперационной ЛТ в стандартном и ускоренном режимах фракционирования.
2. Провести сравнительный анализ отдаленных результатов лечения больных РМЖ IIб-III стадий в зависимости от программы комплексного лечения и методики ЛТ
3. Выявить наиболее значимые факторы прогноза при комбинированном лечении РМЖ, влияющие на результаты локо-регионарного контроля и продолжительность жизни больных.
4.Изучить частоту и характер постлучевых повреждений нормальных тканей.
5. Разработать показания и противопоказания к ЛТ у больных РМЖ IIB-III стадий.
Научная новизна.
На большом клиническом материале представлены отдаленные результаты лечения и проведен сравнительный анализ различных методик (предоперационная, послеоперационная) и режимов ЛТ в комплексной программе лечения больных РМЖ IIB-III стадий в зависимости от морфологических факторов прогноза и вида системного воздействия.
Определены наиболее значимые факторы прогноза, определяющие оптимальную тактику лучевого лечения больных РМЖ IIB-III стадий.
Изучены вопросы постлучевых повреждений нормальных тканей в зависимости от методики и режима лучевого лечения в комбинации с различными схемами химиотерапии.
Проведен многофакторный анализ больным РМЖ IIB-III стадий с целью выявления значимых прогностических признаков для индивидуального построения модели лечения.
Научно-практическая значимость.
Анализ большого клинического материала дает возможность планировать ЛТ с учетом морфологических и клинических факторов прогноза, оптимизировать подходы к назначению ЛТ, что позволит улучшить результаты локо-регионарного контроля, отдаленные результаты лечения и качество жизни больных РМЖ IIB-III стадий. Данные этого исследования имеют большое значение для широкой сети практического здравоохранения, поскольку они позволяют оптимизировать лечебные подходы в комплексной терапии больных IIB-III стадий с использованием лучевого метода лечения.
Апробация диссертации.
Диссертация апробирована 26 октября 2007 года на совместной научной конференции отдела радиационной онкологии, хирургического отделения диагностики опухолей, хирургического отделения опухолей молочных желез, хирургического отделения опухолей женской репродуктивной системы, поликлиники, отделения клинической фармакологии и химиотерапии, отделения радиохирургии НИИ КО ГУ РОНЦ им. Н.Н. Блохина РАМН, кафедры онкологии ГОУ ВПО РГМУ, кафедры онкологии РМАПО
Публикации. По теме диссертации опубликовано 3 научные работы.
Объем и структура диссертации. Диссертация изложена на 152 страницах машинописного текста, содержит 5 таблиц, 78 рисунков. Состоит
из введения, обзора литературы, глав «материал и методы», «результаты локо-регионарного контроля больных раком молочной железы IIB – III cтадий», «сравнительный анализ отдаленных результатов лечения больных раком молочной железы в зависимости от характера проведенного лечения», «многофакторный анализ», заключения и выводов. Список литературы включает 368 источников, в том числе 40 отечественных авторов.
1. КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА МАТЕРИАЛА
Работа основана на ретроспективном анализе 392 историй болезни (стационарных, амбулаторных и лучевых карт) пациенток, получавших первичное лечение в отделении радиохирургии ГУ РОНЦ им. Н.Н. Блохина РАМН в период с 1985 по 2000 годы, страдающих РМЖ IIB-III стадий. Стадирование проводилось по «TNM классификация злокачественных опухолей. Шестое издание» под редакцией и переводом проф. Н.Н. Блинова по данным гистологического исследования удаленного материала Стадирование осуществлялось по критерию p.
Всем больным, включенным в анализ, в плане хирургического лечения была проведена радикальная мастэктомия. В исследование не были включены больные, имевшие в анамнезе злокачественные образования, пациентки с двухсторонним РМЖ или синхронным раком иной локализации, а также больные с отечно-инфильтративной формой рака. Все больные наблюдались в поликлинике ГУ РОНЦ им. Н. Н. Блохина РАМН не менее 5-ти лет.
Возраст больных колебался в пределах от 24 до 78 лет, средний возраст составил 52,4± 0,59 года. Распределение больных в зависимости от возраста показано на рисунке 1.
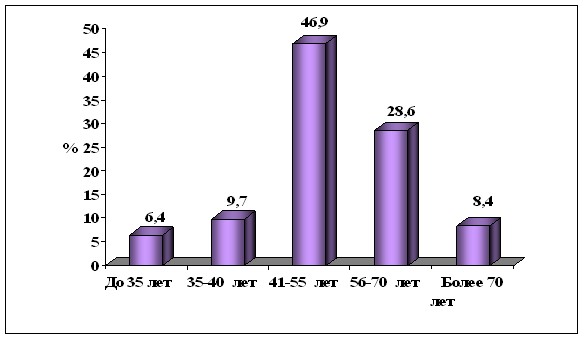
Рис. 1. Распределение больных в зависимости от возраста.
174 (44,4%) пациентки имели сохранную менструальную функцию, а 136 (34,7%) пациенток находились в менопаузе сроком более. Чаще всего опухолевое образование локализовалось во внутренних и центральных квадрантах молочной железы – 198 пациенток(50,5%). Это обусловлено спецификой отделения радиохирургиии, где на протяжении длительного времени проводились исследования по изучению РМЖ центральной и внутренней локализации, а также работы посвященные поражению парастернального лимфатического коллектора. Второй по локализации опухоли был верхне-наружный квадрант –122 больные (31,1%). В исследуемых группах преобладающей формой был инфильтративно-протоковый рак – 261 (66,6%) больная, второй по встречаемости отмечен инфильтративно-дольковый рак -80 пациенток(20,4%). Редкие формы опухоли (медуллярный, слизистый, тубулярный) выявлены у 13 (3,3%) больных, а смешанные опухоли наблюдались у 21(5,4%) пациентки.
У большинства больных- 289 человек(73,7%) диагностирована 3а-3с стадии заболевания. В таблице 1 показано распределение больных по системе TNM.
Таблица 1.
Распределение больных по системе TNM
| Т/N | N0 | N1 | N2 | N3 | Всего |
| Т1 | ---- | ---- | 12(3,05%) | 8(2,1%) | 20(5,1%) |
| Т2 | ---- | 90(22,9%) | 65(16,7%) | 40(10,1%) | 195(49,7%) |
| Т3 | 18(4,6%) | 28(7,1%) | 12(3,05%) | 16(4,2%) | 74(18,9%) |
| Т4 | 11(2,9%) | 42(10,8%) | 24(6%) | 26(6,6%) | 103(26,3%) |
| Всего | 29(7,5%) | 160(40,8%) | 113(28,8%) | 90(22,9%) | 392(100%) |
Распределение больных в зависимости от стадии заболевания представлено в таблице 2.
Таблица 2.
Распределение больных в зависимости от стадии.
| Стадия | Число больных | |
| Абс. | Отн.% | |
| 2б | 103 | 26,3 |
| 3а | 122 | 31,1 |
| 3б | 77 | 19,6 |
| 3с | 90 | 23,0 |
| Всего | 392 | 100,0 |
Наличие неблагоприятных морфологических факторов, таких как: раковые эмболы в лимфатических и/или кровеносных сосудах, опухолевая инфильтрация капсулы ЛУ, распространение опухолевых клеток за капсулу ЛУ с опухолевой инфильтрацией жировой клетчатки подмышечной впадины, 3 степень злокачественности опухоли, поражение 4-х и более подмышечных ЛУ было отмечено у 239 пациенток (61%). В эту группу вошли те больные, которые имели в наличии хотя бы один из перечисленных выше признаков. Большее число пациенток - 231 (58,9%) имели РЭ отрицательные опухоли, а РЭ положительные опухоли отмечались у 143 больных (36,5%). 63 пациентки (16,1%) имели РЭ и РП положительные опухоли, а у 131 больной (33,4%) диагностированы отрицательные опухоли по обоим типам рецепторов. У 18 больных(4,6%) рецепторный статус не определялся, а у 101 больной (25,8%) не определялись рецепторы к прогестерону.
Всем больным была проведена радикальная мастэктомия по одному из 2-х вариантов: с сохранением большой грудной мышцы (по Пейти) – 227(57,9%) больных и с сохранением обеих грудных мышц (по Маддену) - 165 (42,1%) пациенткам. Большинству больных -248 (63,3%) была выполнена биопсия парастернальных ЛУ в 1-4 межреберьях открытым или торакоскопическим способом. Из них у 65 (26,2%) пациенток были диагностированы метастазы в парастернальный лимфатический коллектор. Количество удаленных ЛУ подмышечной области колебалось от 2 до более 20, а среднее значение составило 9.
Большинство больных -363 (92,6%), получили комплексное лечение. Только 19(4,8%) больным было выполнено оперативное вмешательство. Адъювантная терапия не проводилась данным больным в связи с наличием у них тяжелой сопутствующей патологии (15) или отказе пациенток от дополнительного лечения (4). Одиннадцать (2,8%) пациенток получили комбинированное лечение, включавшее ЛТ на пред, или послеоперационном этапах. Химиотерапия проведена 318 (81,1%) больным, а гормонотерапия тамоксифеном (не менее 1 года) 165 (42,1%) больным. Основным режимом химиотерапии был классический CMF, который был проведен 188 (48%) больным. Схемы полихимиотерапии с включением антрациклинов получили 127 (39,9%) пациенток.
Для оценки влияния ЛТ на выживаемость и частоту локорегионарного рецидивирования, больные были распределены на 3 группы:
I группа – больные, получившие предоперационную ЛТ – 145 (37%).
II группа – больные, которым в послеоперационном периоде проводилась ЛТ –138 (35,2%).
III группа – больные, которым ЛТ не проводилась –109 (27,8%).
2. МЕТОДИКИ И РЕЖИМЫ ПРОВЕДЕНИЯ ЛУЧЕВОЙ ТЕРАПИИ.
Методики ЛТ.
Облучение молочной железы до операции, либо передней грудной стенки после радикальной мастэктомии проводилось с латерального и медиального тангенциальных полей (> 22 см) в положении больной на спине с отведенной в сторону рукой. Для устойчивого положения больной во время облучения использовались специальные подставки и фиксирующие устройства. В объем облучения включалась передняя грудная стенка и прилежащая легочная ткань. Верхний край поля располагался на уровне второго межреберного промежутка. Над- подключичную и аксиллярную зону 3 уровня облучали с одного переднего фигурного поля. Если данная зона не включалась в объем облучения, то верхняя граница поля соответствовала уровню ключицы. Латеральная граница поля проходила по средней подмышечной линии. В объем облучения включались аксиллярные ЛУ 1 и 2 уровней. Нижняя граница поля располагалась на 3 см ниже субмаммарной складки при локализации опухоли в верхних и медиальных квадрантах молочной железы. При локализации опухоли в нижних квадрантах молочной железы, нижняя граница поля смещалась на 5 см ниже субмаммарной складки. Медиальная граница тангенциального поля соответствовала срединной линии, отступя на 1 см от нее. В случае облучения парастернальной области, медиальная граница поля соответствовала латеральному краю парастернальной зоны.
Парастернальная зона облучалась с одного переднего поля. Медиальная граница поля соответствовала срединной линии, латеральная – на 5-6 см кнаружи от срединной линии, верхняя – граничила с нижней границей надключичного поля, и нижняя – проходила через мечевидный отросток грудины. В лечении парастернальной зоны была использована как дистанционная терапия- у 99 (25,3%) пациенток, так и внутритканевая ЛТ источником излучения Co60 и Cf 256 у 118 (30,1%) пациенток. Облучение проводилось штырьковыми источниками Со60, которые при помощи катетера проводились в просвет верхне-грудной артерии и закреплялись там на 48 часов. СОД за время облучения составляла 80 иГр на расстоянии 1 см от источника.
Дистанционную ЛТ проводили на линейных ускорителях электронов и гамма-терапевтических аппаратах. Использовали фотонное излучение низких энергий (6 МэВ) или гамма-излучения.
Следует также отметить, что 58 (33%) больным из 174, у которых менструальная функция была сохранена, перед назначением гормонотерапии тамоксифеном было проведено отключение функции яичников либо лучевым (РОД 4 Гр, 4 фракции), либо хирургическим методами.
Режимы ЛТ.
В лечении больных были использованы следующие режимы фракционирования дозы:
Предоперационная ЛТ (145 больных).
- Гипофракционированная ЛТ с применением крупных фракций
-РОД 7Гр х 2 фракции до СОД 14 Гр ( изоэффективные 29 Гр при классическом фракционировании) – 46 больных;
-РОД 5 Гр до СОД 20Гр ( изоэффективные 32 Гр при классическом фракционировании) – 87 больных.
- Стандартная ЛТ РОД 2 Гр 5 раз в неделю до СОД 40 Гр -12 больных.
Послеоперационная ЛТ (138 больных).
1. Стандартная ЛТ РОД 2 Гр 5 раз в неделю до СОД 44-46 Гр - 39 больных.
2. Режим динамического фракционирования – РОД 5 Гр 2 фракции, затем РОД 2 Гр 12-13 фракций ( изоэффективные 40-44 Гр при классическом фракционировании) – 99 больных.
3. РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ
3.1 Локальные и регионарные рецидивы.
Проанализированы результаты локо-регионарного контроля больных, в зависимости от вида лечения и основных прогностических факторов. При наблюдении за больными в течение 10 лет локальные рецидивы выявлены у 62 (15,8%) больных, регионарные – у 21 (5,3%) пациентки. Рецидивы выявлялись в сроки от 6 месяцев до 96 месяцев, в среднем через 22 месяца. Отдаленные метастазы диагностированы у 152 (38,7%) пациенток, в сроки от 6 до 118 месяцев, в среднем через 27,5 месяцев. У 45 (54,2%) больных отдаленные метастазы отмечались на фоне рецидива заболевания.
Чаще у больных отдаленные метастазы выявлялись в кости -68 (44,7%) и легкие -23 (15,3%), реже в головной мозг- 9 (6%), ЛУ средостения -5 (3,2%), ЛУ контралатеральной аксиллярной области -4(2,6%) и сочетанные -43 (28,2%). Метахронные опухоли наблюдались крайне редко – у 28 (7,1%) пациенток. Из них у 17 (60,7%) больных диагностированы злокачественные опухоли противоположной молочной железы. При прослеженности больных в течение 10 лет живы в состоянии полной клинической ремиссии - 173-(44,2%) больных, исчезли из-под наблюдения 37 (9,4%) пациенток и умерли 182 (46,4%) больных от прогрессирования заболевания.
У больных 1 группы (предоперационная ЛТ) выявлены локальные рецидивы у 16 (11,0%) и регионарные у 9 (4,1%) пациенток. Во 2-ой группе больных (послеоперационная ЛТ) за время наблюдения развилось 20 (14,5%) локальных и 5 (3,6%) регионарных рецидивов. В группе пациенток, которым ЛТ вообще не проводилась эти показатели составили 26 (23,8%) и 7(6,4%) соответственно. Статистических различий между этими тремя группами выявлено не было ввиду относительно небольшого числа наблюдений, но имелась четкая тенденция к уменьшению количества рецидивов в группах пациенток, кому была проведена ЛТ. Мы провели однофакторный анализ влияния морфологических и клинических факторов прогноза на частоту локальных и регионарных рецидивов у больных, получивших различные варианты ЛТ. В таблице 3 указаны прогностические факторы, влияющие на частоту локальных рецидивов, * указаны достоверные (р<0,05) различия при сравнительном анализе внутри групп лечения.
Таблица 3.
Факторы влияющие на частоту локальных рецидивов.
| Группы по виду лучевого лечения | |||
| Фактор | I | II | III |
| Неблагоприятные факторы присутствуют | 15,4%* | 18%* | 32,8%* |
| Неблагоприятные факторы отсутствуют | 4% | 5,3% | 12,5% |
| Поражение 4-х и более ЛУ | 15,7% | 17,3% | 37,3% |
| Поражение менее 4-х ЛУ | 9,2% | 11,8% | 14,3% |
| Возраст 35 или менее | 20% | 30% | 29,8% |
| Возраст старше 35 лет | 9,2% | 12,1% | 19,3% |
| Стадия 3с | 27%* | 22,7%* | 47,6% |
| Стадия 2в | 8,5% | 5,3% | 19,4% |
| 3-я степень злокачественности | 25,5%* | 25%* | 55,2%* |
| 2 степень злокачественности | 6,25% | 11,3% | 21,1% |
| Отсутствие патоморфоза | 21,6%* | ------- | ------- |
| Патоморфоз 1-2 степени | 9,3% | ------- | ------- |
В отношении регионарных рецидивов достоверных показателей получено не было из-за недостаточного числа наблюдений. Но имелась тенденция к увеличению частоты рецидивирования при таких факторах прогноза как: поражение 4-х и более лимфатических узлов, 3-я степень злокачественности, возраст пациенток до 55 лет, наличие раковых эмболов в просвете лимфатических или кровеносных сосудов, III стадия опухолевого процесса.
3.2 Отдаленные результаты лечения в зависимости от проведенного лучевого воздействия.
Нами проведен однофакторный анализ отдаленных результатов лечения больных РМЖ IIб-III стадий в зависимости от проведенного лучевого лечения и основных прогностических признаков.
На рисунках 2 и 3 показаны кривые общей и безрецидивной выживаемости в зависимости от метода лучевого воздействия. Не выявлено достоверных различий в 5-летних показателях общей и безрецидивной выживаемости в зависимости от характера проведенной ЛТ. 
Рис. 2. Общая выживаемость (ОВ) больных РМЖ в зависимости от вида лечения.
Однако более высокие показатели 10-летней общей и безрецидивной выживаемости достоверно (р<0,05) достигнуты у больных при проведении послеоперационной ЛТ: 74,1% и 71%, соотв. по сравнению с больными, которым ЛТ не проводилась, либо проводилась на предоперационном этапе.

Рис. 3. Безрецидивная выживаемость (БРВ) больных в зависимости от проведенного лучевого лечения.
Мы сравнили пяти- и десятилетнюю выживаемость больных при наличии неблагоприятных морфологических критериев (рис.4,5). Послеоперационная ЛТ достоверно (р<0,05) улучшает отдаленные результаты лечения больных с неблагоприятными прогностическими факторами по сравнению с больными, которым ЛТ не проводилась и кому была проведена предоперационная лучевая терапия. 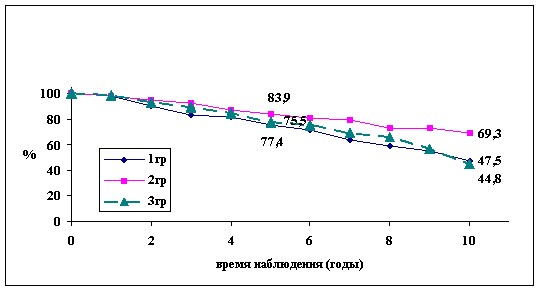
Рис. 4. ОВ больных РМЖ при наличии неблагоприятных морфологических факторов прогноза в зависимости от вида лучевого лечения.

Рис. 5. БРВ больных РМЖ при наличии неблагоприятных морфологических факторов прогноза в зависимости от вида лучевого лечения.
Достоверных различий не получено у больных, имеющих благоприятные морфологические факторы прогноза в зависимости от методики ЛТ.
Мы провели сравнительный анализ результатов лечения больных, имеющих третью степень злокачественности опухоли в зависимости от характера лучевого воздействия (рис. 6, 7). Отмечались достоверно лучшие показатели 10-ти летней общей и безрецидивной выживаемости у больных, кому проводилась послеоперационная ЛТ по сравнению с больными I и III групп. Так 10-летняя ОВ в группе послеоперационной ЛТ составила 73,3%, в предоперационной - 41,5%, а в III группе - 34,7%. Не выявлено достоверных различий по показателям 10 летней ОВ между пациентками, которым ЛТ не проводилась и с предоперационным облучением. Достоверно наихудшие показатели 10-летнй БРВ наблюдались у больных III группы, которым лучевая терапия не проводилась по сравнению с больными, получившими адъювантную и неоадъювантную ЛТ.

Рис. 6. ОВ больных РМЖ с 3 степенью злокачественности опухоли в зависимости от вида лучевого лечения.

Рис. 7. БРВ больных РМЖ с 3 степенью злокачественности опухоли в зависимости от вида лучевого лечения.
Мы провели сравнительный анализ отдаленных результатов лечения больных в зависимости от наличия локальных рецидивов заболевания (рис.8, 9). Рецидивы заболевания снижали показатели ОВ независимо от характера проведенного лечения, в связи с тем, что у этих больных в дальнейшем отмечалось прогрессирование заболевания в виде генерализации процесса.

Рис. 8. ОВ больных РМЖ с рецидивами заболевания по группам.
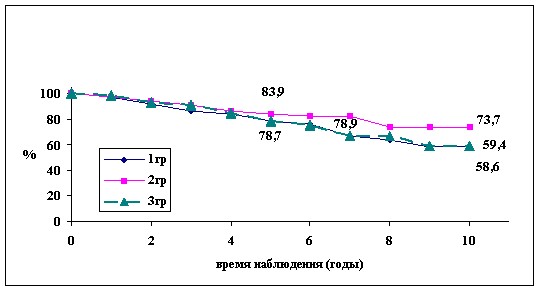
Рис. 9. ОВ больных РМЖ без рецидивов заболевания по группам.
Мы провели сравнительный анализ общей выживаемости больных в группе пациенток, кому была проведена послеоперационная ЛТ в зависимости от режима фракционирования дозы. При этом сравнили классический режим фракционирования ( 2Гр х 5 раз в неделю до СОД 44-46 Гр) и динамический режим ( 5Гр х2 фракции, затем по 2 Гр до СОД 44-46 Гр по изоэффекту) ( Рис. 10). Динамический режим послеоперационной лучевой терапии способствовал увеличению показателей 10-ти летней общей выживаемости до 73,4% по сравнению с классическим режимом фракционирования дозы -59,8% (р >0,05).

Рис. 10. ОВ больных в группе послеоперационной ЛТ в зависимости от режима фракционирования.
Парастернальная лимфаденэктомия была выполнена 248 пациенткам, из них у 65 (26,2%) были выявлены метастазы в парастернальные лимфоузлы. Мы оценили частоту их появления в зависимости от локализации опухоли в молочной железе. Так при локализации опухоли в наружных квадрантах молочной железы частота метастазирования в этот коллектор составила 15,9%, а при нахождении во внутренних и центральных отделах 32,5%. Данные различия недостоверны, но имеется выраженная тендеция к увеличению частоты метастазирования в эту область опухолей, которые расположены в центральных и внутренних отделах, по сравнению с наружными. Выполненная парастернальная лимфаденэктомия таким образом оптимизирует программу облучения за счет включения этой области у 15,9% пациенток с наружной локализацией, и позволяет исключить эту зону из радиационного поля у 67,5% больных, имеющих опухоли внутренней и центральной локализации.
4. МНОГОФАКТОРНЫЙ АНАЛИЗ
Изучение факторов прогноза приобретает в настоящее время все большее значение в силу ряда причин. Основной причиной является стандартизация тактики лечения онкозаболеваний на основании рациональных подходов в зависимости от факторов прогноза. Это
определяется необходимостью оценки в каждом конкретном случае степени адекватности проводимого лечения, так как улучшение показателей выживаемости во многом определяется строгой индивидуализацией лечебной тактики, которую невозможно осуществить без прогнозирования течения опухолевого процесса. Все включенные в анализ прогностические факторы нами были распределены на три основные группы:
• факторы, характеризующие первичную распространенность опухолевого процесса;
• факторы, характеризующие биологические особенности опухоли;
• факторы, характеризующие адекватность и степень радикальности предпринятого лечения.
После проведения монофакторного анализа были выделены факторы, показавшие статистически значимое влияние на выбор метода лечения больных. Для каждого из включенных 392 пациентов в общей сложности определялись значения 56 факторов. Были отобраны наиболее информативные факторы:
стадия опухолевого процесса;
размер опухоли;
число пораженных ЛУ;
локализация опухоли;
возраст;
гистологический вариант;
степень злокачественности опухоли;
уровень РЭ.
Все пациентки разделялись на две ведущие группы:
1) Пациентки, которым была проведена послеоперационная ЛТ – всего 138; 2) Пациентки, которым не проводилась ЛТ – всего 109.
Статистический анализ данных состоял в построении решающих правил (по методу Байеса), использующих различные наборы признаков. Для вычисления коэффициентов решающих правил использовались данные о 165 больных (обучающая выборка). Оставшиеся пациентки были включены в «экзаменационную» выборку, на которой были проверены факторы, выделенные как прогностически значимые при анализе прогностических ранговых величин выделенных факторов. Экзаменационная выборка состояла из 82 пациентов. Для каждого больного, включенного в экзаменационную выборку, с помощью полученных правил определялась принадлежность к группам. Частота правильного определения группы (с учетом 95%-го доверительного интервала) служила оценкой качества решающего правила. Вычислялись коэффициенты информативности Вапника-Червоненкиса (1974,1984). Для проверки достоверности различий значений признаков в группах использовались тесты 2 Пирсона и точный критерий Фишера. Было испытано 4 решающих правила, использующих различные наборы признаков. Лучшим оказалось правило, основанное на 7 признаках, и имеющее точность 79,6% (95%-й доверительный интервал). Доверительные интервалы вычислялись с помощью биноминального распределения. Доверительный интервал для "лучшего правила из N правил" определялся по методу Бонферрони (Учет "многократных сравнений") [Урбах В.Ю., 1975, Гублер Е.В., 1978; Лакин Г.Ф., 1980; Cox DR., 1981; Miller RG., 1981; Armitage P., 1988; Matthews D.E., 1988]. Суммарная по группам частота правильной классификации объектов обучающей и экзаменационной выборки равна 78,0% и 87,2%, соответственно.
На основании полученных результатов было выделено 12 статистически значимых факторов, определяющих выбор метода лечения распространенным РМЖ.
На основании статистически значимых факторов прогноза, были рассчитаны коэффициенты информативности, позволившие определить ранговое место для каждого из представленных факторов. Ранговое место определяет влияние каждого из значимых факторов на выбор метода лечения больных местно-распространенным РМЖ, что определяет весовые значения каждого из них при создании формулы индивидуального прогнозирования. На основании Байесовского решающего правила с учетом продолжительности жизни для всех представленных значимых факторов были рассчитаны коэффициенты, параметры которых позволяли рассчитать индивидуальный прогноз. Положительный знак коэффициента означает, что ЛТ не показана этой группе больных, тогда как отрицательный знак – необходимо проведение послеоперационной ЛТ. Показатели коэффициентов представлены в таблице 4.
Таблица 4.
Коэффициенты Байесовского решающего правила для значимых факторов прогноза
| Факторы прогноза | Коэф |
| Степень злокачественности | |
| 1 | 39 |
| 2 | 11 |
| 3 | -41 |
| Вид операции | |
| Мастэктомия по Пейти | 35 |
| Мастэктомия по Маддену | -44 |
| Опухолевая инвазия капсулы ЛУ | |
| Есть | -45 |
| Нет | 13 |
| Опухолевая инвазия жировой клетчатки аксиллярной области | |
| Есть | -64 |
| Нет | 16 |
| Локализация опухоли в молочной железе | |
| Верхненаружный кв. | 31 |
| Верхневнутренний | -52 |
| Центральная часть | -13 |
| Нижненаружный | 5 |
| Нижневнутренний | 47 |
| Уровень РЭ | |
| Отрицат | -7 |
| Положит | 1 |
| Стадия | |
| IIВ | 85 |
| IIIА | -48 |
| IIIВ | -50 |
| IIIС | -49 |
| Возраст | |
| До 35 лет | -217 |
| 36 – 40 | -82 |
Продолжение таблицы 4.
Коэффициенты Байесовского решающего правила для значимых факторов прогноза.
| Фактор | коэффициент |
| 41- 55 | -30 |
| 56 – 70 | 44 |
| Более 70 | 124 |
| Неблагоприятные морфологические факторы | |
| Есть | -63 |
| Нет | 79 |
| Метастазы в подмышечные лимфоузлы | |
| До 3 ЛУ | -19 |
| 4 – 7 ЛУ | -44 |
| Более 7 ЛУ | -56 |
| Нет пораженных ЛУ | 105 |
| Размер опухоли | |
| До 2 см | 35 |
| 2,1 – 5,0 см | -4 |
| Более 5 см | -33 |
| Гистологический вариант | |
| Смешанный тип | -31 |
| Инфильтративно-протоковый | -11 |
| Инфильтративно-дольковый | -1 |
| Редкие формы | 24 |
| Инф/прот с преоблад инф/дольк | -82 |
| Порог | 0 |
Таким образом, на основании определения коэффициентов каждого из достоверно значимых прогностических факторов можно выделить факторы позволяющие определить методику послеоперационного лечения (адъювантная ЛТ – рис. 11).
К данным факторам относятся:
III стадия опухолевого процесса;
Наличие неблагоприятных морфологических факторов;
размер опухоли более 2 см;
число пораженных ЛУ более 3;
локализация опухоли в верхневнутреннем и центральном квадрантах;
возраст до 55 лет;
гистологический вариант - инфильтративно-протоковый рак;
рецептороотрицательные опухоли.

Рис. 11. Ранговое место каждого из значимых факторов при выборе метода лечения больных РМЖ.
В целом показатели достоверности данных многофакторного анализа позволяют отметить высокую достоверность полученных результатов:
Чувствительность – 70,9%
Специфичность – 87,2%
Общая точность – 79,6%
Таким образом, на основании полученных ранговых величин статистически значимых факторов прогноза, полученных в многофакторном анализе, может быть сделан выбор методики лечения больных местно-распространенным РМЖ, а также позволяет выделить группу риска. В этой группе, с учетом опыта комбинированного лечения, может проводиться дальнейшая специфическая терапия, направленная на улучшение результатов лечения. Эффективность такого лечения будет определяться характером применяемых методов, а также методик его проведения.
5. ВЫВОДЫ
1. Послеоперационная лучевая терапия снижает частоту локальных рецидивов c 23,9% (при отсутствии радиотерапии) до 14,5% и достоверно (р<0,05) улучшает показатели десятилетней общей и безрецидивной выживаемости до 74,1% и 71%, соответственно по сравнению с больными, которым радиотерапия не проводилась (40,5% и 37,7%, соответственно).
2. Послеоперационная ЛТ достоверно (р<0,05) улучшает показатели десятилетней общей и безрецидивной выживаемости у больных с неблагоприятными морфологическими факторами прогноза до 69,3 %, и 66,2 %, соответственно по сравнению с пациентками, получившими предоперационную радиотерапию, где эти показатели были равны 47,5% и 45,3%, соответственно.
3. Выполненная парастернальная лимфодиссекция у 248 (63,3%) больных позволяет оптимизировать программу лучевого воздействия и провести адекватное облучение парастернальной зоны у 32,5% больных с центральной и медиальной локализацией опухоли, и у 15,9% больных с локализацией опухоли в наружных квадрантах молочной железы.
4. Динамический режим послеоперационной лучевой терапии (5 Гр х 2 фракции, 2 Гр х фракций, СОД 44-45 Гр по изоэффекту) способствует увеличению показателей десятилетней общей выживаемости до 73,4% по сравнению с группой больных, получившей стандартный режим фракционирования - 59,8% (р>0,05).
5. Выявлено, что частота постлучевых повреждений нормальных тканей не зависела от режима фракционирования. Поздние постлучевые повреждения нормальных тканей первой и второй степени выявлены у 4,3% больных с послеоперационной лучевой терапий в стандартном режиме фракционирования и у 4,8% после динамического фракционирования.
6. Проведенный многофакторный анализ позволил выделить наиболее значимые прогностические признаки, определяющие показания к проведению послеоперационной лучевой терапии: Ш стадия опухолевого процесса (588), метастазы в 4 и более аксиллярных лимфатических узлов (317), возраст менее 55 лет (272), внутренняя и центральная локализации опухоли в молочной железе (195), III степень злокачественности опухоли (168), инфильтратитвно-протоковый рак (99), опухоли размером более 2 см (39) и рецепторо-отрицательные опухоли (29).
7. Проведенный многофакторный анализ позволил позволил выделить группу больных, которым послеоперационная лучевая терапии не показана: пациентки старше 55 лет, имеющие благоприятные факторы прогноза.
Список работ, опубликованных по теме диссертации:
1. Гладилина И.А., Нечушкин М.И., Курносов А.А. Метастазы в подмышечные лимфатические узлы рака молочной железы. Клиническое значение и прогноз.// II Евразийский конгресс по медицинской физике и инженерии. «Медицинская физика-2005» Москва.- 21-24 июня 2005.- С. 57.
2. Гладилина И.А., Нечушкин М.И., Курносов А.А. Поражение подмышечных лимфатических узлов при раке молочной железы.// «Новые технологии в онкологической практике». Материалы научно-практической конференции с международным участием,.- Барнаул.- 7-8 июня 2005.- С. 366.
3. Гладилина И.А., Нечушкин М.И., Курносов А.А., Монзуль Г.Д. Роль лучевой терапии в программе комплексного лечения больных раком молочной железы.//Опухоли женской репродуктивной системы/Маммология.- 2005.- №1.- С.31-35.

