Комплексный подход к молекулярной диагностике ряда социально значимых заболеваний
На правах рукописи
Пальцева Екатерина Михайловна
КОМПЛЕКСНЫЙ ПОДХОД К МОЛЕКУЛЯРНОЙ ДИАГНОСТИКЕ
РЯДА СОЦИАЛЬНО ЗНАЧИМЫХ ЗАБОЛЕВАНИЙ
14.03.10 – клиническая лабораторная диагностика
Автореферат
диссертации на соискание ученой степени
доктора медицинских наук
Москва – 2010
Работа выполнена в Первом Московском государственном медицинском университете им. И.М. Сеченова Минздравсоцразвития РФ
НАУЧНЫЕ КОНСУЛЬТАНТЫ
- член-корреспондент РАМН,
доктор химических наук, профессор Северин Сергей Евгеньевич
- доктор биологических наук, профессор Залетаев Дмитрий Владимирович
ОФИЦИАЛЬНЫЕ ОППОНЕНТЫ
- член-корреспондент РАМН,
доктор медицинских наук, профессор Кушлинский Николай Евгеньевич
- член-корреспондент РАМН,
доктор медицинских наук, профессор Дурнев Андрей Дмитриевич
- доктор медицинских наук Кишкун Алексей Алексеевич
ВЕДУЩАЯ ОРГАНИЗАЦИЯ
ФГУ «Учебно-научный медицинский центр» Управления делами Президента РФ
Защита состоится « 23» марта 2011 г. в 10.00 на заседании Диссертационного Совета Д 208.071.04 в ГОУ ДПО «Российская медицинская академия последипломного образования» (123995, Москва, Ул. Баррикадная, д. 2/1)
Автореферат разослан « » февраля 2011 г.
С диссертацией можно ознакомиться в библиотеке ГОУ ДПО Российская медицинская академия последипломного образования по адресу: 123445, Москва, ул. Беломорская, д.19.
Ученый секретарь
Диссертационного Совета Д 208.071.04
доктор медицинских наук, профессор Морозова В.Т.
Актуальность проблемы
В настоящее время все большую актуальность приобретает диагностика различных заболеваний на основе биологических маркеров. Набор известных биомаркеров на уровне клеток и субклеточных структур пополняется таковыми на уровне генома. Создание комплекса новых биохимических и молекулярно-генетических маркеров должно дать мощный импульс для развития диагностики, позволяющей прогнозировать риски развития заболеваний, обнаружения заболеваний на ранних стадиях, а также прогнозировать течение болезни.
Усилия ученых направлены на идентификацию и характеристику молекулярных биомаркеров и разработку соответствующих тест-систем и методов оценки. Это одна из актуальных задач, решаемых молекулярной медициной. Определение комплекса биомаркеров позволяет выявить молекулярные механизмы возникновения заболеваний, а также находит применение в клинической практике для диагностики широко распространенных социально значимых мультифакториальных заболеваний, таких как онкологические и сердечно-сосудистые заболевания.
Ранняя диагностика сердечно-сосудистых заболеваний и необходимость создания систем быстрого определения риска их развития приобретают в последнее время все большую актуальность. Сердечно-сосудистые заболевания (ССЗ), в частности ишемическая болезнь сердца (ИБС) и ее осложнение – инфаркт миокарда (ИМ), продолжают оставаться главной причиной смертности мужчин и женщин экономически развитых стран Европы и США (Рагино Ю.И. и соавт., 2008; Шевченко О.П., Мишнев О.Д., 2005; Tsimikas S., Mooser V., 2004). Ежегодно в странах Западной Европы они становятся причиной смерти у 4 млн. человек. У половины, или почти у 2 млн. человек, смерть наступает в результате ИБС (Шевченко О.П., Мишнев О.Д., 2005). Болезнь коронарных сосудов – ведущая причина смертности среди населения США, составляющая более 25% смертей людей старше 35 лет (Kannel W.B., 2005). В Российской Федерации в 90-е гг. в целом заболеваемость ИБС возросла на 24%, заболеваемость стенокардией – на 41%, острым инфарктом миокарда – почти на 16%. Ежегодно в России от ССЗ умирает более 1 млн. человек. По данным ВОЗ, в структуре смертности от ССЗ на долю ИБС приходится 47% (Щепин О.П. и соавт., 2009).
Многочисленные исследования в последние годы ознаменовались определенными достижениями в изучении механизмов развития и прогрессирования ИБС. Создание новых групп фармацевтических препаратов и внедрение их в клиническую практику позволили снизить риск развития острой кардиоваскулярной патологии. Тем не менее, ИБС и прогрессирование коронарного атеросклероза остаются главными причинами смертности и инвалидизации населения. Современная стратегия ведения пациентов с ИБС включает в себя раннюю и точную диагностику заболевания, стратификацию риска и прогноза, что требует поиска новых биологических маркеров и оценки их ассоциации с заболеванием. Наиболее важным представляется поиск ранних чувствительных и специфичных маркеров развития нестабильности атеросклеротических бляшек, изменение уровня которых можно обнаружить до или в отсутствие повреждения клеток миокарда (Bayes-Genis A. et al., 2001).
Частота онкологических заболеваний неуклонно растет и начинает теснить сердечно-сосудистые. Так, показатель заболеваемости злокачественными новообразованиями на 100 тыс. населения в Российской Федерации в 2001 г. составил 312,3 чел., в 2006 г. – 332,2 чел. (Щепин О.П. и соавт., 2009).
Исследование молекулярно-биологических причин возникновения рака - одна из наиболее актуальных проблем современной молекулярной медицины. Основной причиной злокачественной трансформации клетки являются генетические факторы. Молекулярно-генетические исследования генома злокачественной опухоли представляют собой фундаментальную проблему, разрешения которой требует клиническая практика. В связи с тем, что частота онкопатологии постоянно растет, а возраст манифестации заболевания уменьшается, большую актуальность приобретает проспективная диагностика онкопатологии в рамках ежегодных диспансеризаций и в группах риска.
Поиск и характеристика молекулярной патологии в злокачественных опухолях является самостоятельным и очень важным направлением в молекулярной диагностике, так как позволяет расшифровать механизмы канцерогенеза, определить прогноз заболевания, тактику лечения и осуществлять мониторинг рецидивирования. Разработка методов обнаружения молекулярных маркеров дает возможность создавать эффективные диагностические системы. Нами разработаны и описаны в данной работе системы молекулярных маркеров для диагностики рака почки, предстательной железы, цервикальной интраэпителиальной неоплазии и рака шейки матки, увеальной меланомы.
Злокачественная трансформация клетки является процессом многоступенчатым, включающим накопление структурных и функциональных изменений в геноме клетки. К структурным, или генетическим маркерам относят все нарушения, которые изменяют структуру ДНК. В первую очередь, это крупные аномалии, такие как делеции целых хромосомных районов, содержащих гены-супрессоры опухолевого роста и дупликации или амплификации районов, содержащих клеточные протоонкогены, факторы роста и др.; транслокации и инверсии хромосомного материала, в результате которых могут образовываться химерные гены, имеющие онкогенные функции. Другим результатом структурных перестроек может оказаться ситуация, когда клеточный протоонкоген получает дополнительные активирующие регуляторные элементы и начинает гиперэкспрессироваться. И, наконец, к структурным аномалиям относят различные типы мутаций, которые могут активировать протоонкогены или инактивировать гены-супрессоры (Залетаев Д.В. и соавт., 2009).
К функциональным маркерам относят все нарушения, которые не связаны с изменениями структуры ДНК, но приводят к изменениям в уровне экспрессии генов, участвующих в процессах канцерогенеза. Профиль экспрессии генов в опухоли кардинально изменен по сравнению с нормальной тканью, поэтому определенные сочетания генов, теряющих свою экспрессию, или, наоборот, гиперэкспрессирующихся в определенном типе опухоли, могут являться диагностическими и прогностическими маркерами. Изменения в экспрессии гена без изменения его нуклеотидной структуры относятся к эпигенетической регуляции. К таким функциональным нарушениям в первую очередь относят метилирование регуляторных районов генов-супрессоров опухолевого роста, что приводит к их полной инактивации (Залетаев Д.В. и соавт., 2009).
Каждая конкретная опухоль уникальна по набору патологических изменений, так же как и геном каждого конкретного пациента. Для каждой опухоли существуют наиболее характерные пути регуляции и молекулярные маркеры, которые специфичны для начала заболевания, его прогрессии и терминальных стадий. Молекулярные маркеры позволяют четко определить стадию злокачественного процесса и проследить молекулярную эволюцию опухолевого процесса. Для опухолей различных тканей и органов такие маркеры могут значительно отличаться.
Мониторинг молекулярных маркеров, которые обнаруживаются задолго до клинических проявлений, позволяет вовремя начать более тщательную диагностику и превентивную терапию. Определенные биологические и молекулярно-генетические маркеры или их сочетание позволяют определить начальные стадии, прогноз развития заболевания, подобрать оптимальную тактику лечения и разработать таргетные терапевтические средства. Поэтому важнейшей практической задачей является разработка алгоритма исследования диагностических маркеров социально значимых заболеваний.
Цель исследования
Поиск и характеристика ключевых молекулярных маркеров сердечно-сосудистых и некоторых онкологических заболеваний с целью разработки лабораторно-диагностических систем для ранней диагностики, прогноза развития и оценки эффективности терапии этих заболеваний.
Задачи исследования
- Провести сравнительный анализ уровня экспрессии активатора плазминогена урокиназного типа (uPA) и ингибитора активатора плазминогена 1 типа (PAI-1) в моноцитах периферической крови больных со стабильным течением ИБС и больных с острым коронарным синдромом (ОКС) для выявления связи уровня экспрессии этих белков со степенью тяжести заболевания.
- Определить уровни С-реактивного белка (СРБ) и адипонектина в крови больных со стабильным течением ИБС и с ОКС для оценки взаимосвязи этих показателей с риском возникновения ОКС.
- Исследовать аллельные делеции генов-супрессоров VHL, RASSF1 и FHIT и метилирование гена CDH1 при светлоклеточном раке почки (СРП) с целью поиска прогностических критериев этого заболевания; исследовать мутации и метилирование гена VHL для определения эффективности назначения таргетной терапии светлоклеточного рака почки.
- Изучить полиморфные варианты генов ABCB1, TGFBR1, IL10 и VDR для определения предрасположенности к развитию спорадического рака почки.
- Исследовать потери гетерозиготности и микросателлитную нестабильность хромосомных районов 13q14 и 16q23 при раке предстательной железы (РПЖ) с целью поиска диагностических и прогностических критериев данного заболевания.
- Оценить частоту образования химерных транскриптов TMPRSS2/ERG4, TMPRSS2/ETV1 и TMPRSS2/ETV4 при раке предстательной железы и определить их диагностический потенциал.
- Исследовать нарушения эпигенетической регуляции экспрессии генов-супрессоров на ранних стадиях канцерогенеза шейки матки и определить маркеры, имеющие диагностический потенциал.
- Исследовать аллельные делеции в хромосомах 3 и 1р36 при увеальной меланоме с целью разработки диагностических и прогностических критериев данного заболевания.
- Изучить морфологическую и молекулярно-генетическую внутриопухолевую гетерогенность колоректальных аденокарцином.
Научная новизна
Важное значение имеют впервые полученные методом проточной цитофлуориметрии данные о характере изменения уровня экспрессии PAI-1 в моноцитах периферической крови больных ИБС, так как одним из патогенетических факторов ИБС является снижение фибринолитической активности крови.
Впервые разработан метод определения молекулярно-генетических маркеров для оценки прогрессии первичной опухоли при светлоклеточном раке почки, а также метод выявления среди пациентов с метастатическим светлоклеточным раком почки лиц, в отношении которых наиболее эффективно назначение таргетных препаратов, действие которых связано с VHL-зависимыми патогенетическими механизмами.
Нами предложена молекулярно-генетическая методика выявления среди пациентов с различными заболеваниями предстательной железы лиц с РПЖ, а также прогноза гистологически подтвержденного РПЖ. Методика основана на определении потери гетерозиготности и микросателлитной нестабильности хромосомных районов 13q14 и 16q23 в ткани ПЖ. Впервые продемонстрировано, что при раке предстательной железы наличие химерного онкогена TMPRSS2/ERG4 является частым, опухолеспецифическим событием, коррелирует с более агрессивными стадиями заболевания и может служить молекулярным маркером этого рака, а также маркером андрогенчувствительности опухолевых клеток и оценки ответа опухоли на гормональную терапию. Нами предложен способ определения экспрессии химерного онкогена TMPRSS2/ERG4 методом ОТ-ПЦР с использованием специфических праймеров.
Впервые предложены методики определения молекулярных маркеров метилирования при ряде онкологических заболеваний. Нами разработана система ДНК-маркеров (маркеры метилирования генов р16, MLH1 и N33) для ранней диагностики рака шейки матки (РШМ), имеющая высокую чувствительность и специфичность. Полученные результаты позволяют считать, что исследование гиперметилирования генов-супрессоров вместе с цитологическим исследованием и тестированием вируса папилломы человека может служить основой для мониторинга женщин с высоким риском развития рака шейки матки. Разработан метод определения метилирования генов N33 и GSTP1 при аденокарциномах предстательной железы, что может помочь в диагностике данного заболевания.
Нами разработан метод выявления специфических молекулярных маркеров при увеальной меланоме, который может использоваться для верификации диагноза «увеальная меланома», а также метод оценки прогрессии первичной опухоли при данном заболевании.
Впервые продемонстрирована молекулярно-генетическая внутриопухолевая гетерогенность колоректальных аденокарцином.
Работа по определению молекулярно-генетических маркеров перечисленных онкологических заболеваний удостоена премии Правительства РФ 2009 года в области науки и техники для молодых ученых («Разработка и внедрение методов ДНК-диагностики для раннего определения и прогноза некоторых онкологических заболеваний»).
Практическая значимость
Настоящая работа представляет практический интерес для диагностики и оценки прогноза таких социально значимых заболеваний, как ИБС и ряд злокачественных новообразований. Проведенное исследование позволило на основании полученных данных выделить маркер развития острого коронарного синдрома, который можно определить в моноцитах периферической крови, а также биомаркеры, которые можно использовать для дополнительной оценки степени тяжести воспалительного процесса у больных со стабильным течением ИБС. Это позволяет предложить более тщательную программу диагностических мероприятий и своевременно скорректировать проводимую терапию.
Исследование аллельных делеций генов-супрессоров опухолевого роста, расположенных в коротком плече хромосомы 3, и метилирование гена CDH1 представляет собой метод оценки прогрессии и способности к метастазированию первичной опухоли при светлоклеточном раке почки. Полученные результаты легли в основу новой медицинской технологии. Разрешение на применение новой медицинской технологии ФС №2008/150.
Разработанная нами медицинская ДНК-технология позволяет выделять VHL-зависимые и VHL-независимые группы пациентов со светлоклеточным раком почки и, соответственно, оптимизировать тактику и эффективность лечения таргетными препаратами, действие которых связано с VHL-зависимыми патогенетическими механизмами. Разрешение на применение новой медицинской технологии ФС №2008/152.
Для выявления пациентов с начальными стадиями РПЖ, а также для прогноза гистологически подтвержденного РПЖ в целях подбора наиболее оптимальных вариантов терапии нами разработана медицинская ДНК-технология, направленная на определение делеций хромосомных районов 13q14 и 16q23 в биопсийных образцах больных. Разрешение на применение новой медицинской технологии ФС №2008/151.
При РПЖ разработанная методика позволяет определять наличие химерного онкогена в ткани опухоли. Поскольку он служит маркером неблагоприятного прогноза и андрогенчувствительности опухоли, появляется возможность оптимизировать тактику и эффективность лечения рака предстательной железы. Разрешение на применение новой медицинской технологии ФС №2008/153.
Молекулярные маркеры метилирования (при раке шейки матки, раке предстательной железы) позволяют выявить начальные стадии злокачественного процесса еще до того, как обнаруживаются морфологические изменения. Это позволяет начать терапию заболевания на ранних сроках и избежать высокодозной химиотерапии, тяжелой инвалидизации и летального исхода. Разрешение на применение новой медицинской технологии ФС №2008/154 (ранняя диагностика рака шейки матки).
При увеальной меланоме разработанный метод исследования аллельных делеций в хромосоме 3 позволяет выявлять специфические молекулярные маркеры для верификации диагноза «увеальная меланома» в дополнение к применяемым в настоящее время диагностическим методам. Разрешение на применение новой медицинской технологии ФС №2009/319.
Описанное в данной работе исследование потери гетерозиготности в хромосомах 3 и 1р36 представляет собой метод оценки прогрессии первичной опухоли при увеальной меланоме. Разрешение на применение новой медицинской технологии ФС №2009/318.
Личный вклад автора
Автором проведен подбор возможных молекулярных маркеров для диагностики и прогноза исследуемых онкологических заболеваний и ишемической болезни сердца. Автором осуществлены лабораторные исследования с использованием иммуноцитохимического, иммуногистохимического, цитофлуориметрического и иммуноферментного методов определения биомаркеров ишемической болезни сердца. Проведена статистическая обработка всех полученных данных. Автором проанализированы полученные результаты исследования ключевых молекулярных маркеров ишемической болезни сердца и ряда онкологических заболеваний; сформулированы выводы и практические рекомендации.
Внедрение результатов исследования
Результаты исследования внедрены в клинико-диагностическую работу в Московском научно-исследовательском онкологическом институте им. П.А. Герцена, Российском научном центре хирургии им. акад. Б.В. Петровского РАМН.
Полученные практические и теоретические выводы применяются в учебном процессе кафедры биохимии Первого Московского государственного медицинского университета им. И.М.Сеченова, кафедры биохимии МГУ им. М.В. Ломоносова, кафедры клинической лабораторной диагностики Российской медицинской академии последипломного образования.
Апробация работы
Апробация диссертации проведена 18 ноября 2010 г. на совместном заседании кафедры клинической лабораторной диагностики, кафедры биохимии ГОУ ДПО Российская медицинская академия последипломного образования Росздрава, кафедры биохимии, лаборатории молекулярной генетики человека НИИ молекулярной медицины ГОУ ВПО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздравсоцразвития РФ, лаборатории эпигенетики ГУ Медико-генетический научный центр РАМН (протокол № 19).
Материалы диссертации доложены на 20-м Европейском Конгрессе Патологии (Париж, Франция, 2005 г.), Российском медицинском форуме (Москва, 2007), Конференции для молодых ученых, аспирантов и студентов по молекулярной биологии и генетике (Киев, Украина, 2007), на съездах Европейского общества генетиков человека ESHG (Ницца, Франция, 2007 г. и Барселона, Испания, 2008 г.), 7-м Международном симпозиуме по множественным факторам риска сердечно-сосудистых заболеваний (Венеция, Италия, 2008 г.), 6-м Конгрессе по метаболическому синдрому, диабету II типа и атеросклерозу (Берлин, Германия, 2009 г.), 6-й международной конференции «Молекулярная медицина и биобезопасность» (Москва, 2009).
Публикации
По теме диссертационной работы опубликовано 25 печатных работ. Из них - 12 статей и 11 тезисов, глава в книге «Системы генетических и эпигенетических маркеров в диагностике онкологических заболеваний», глава в книге «Введение в молекулярную диагностику». Получено 7 разрешений на применение новых медицинских технологий (ФС №2008/150, ФС №2008/152, ФС №2008/151, ФС №2008/153, ФС №2008/154, ФС №2009/319, ФС №2009/318). Работа «Разработка и внедрение методов ДНК-диагностики для раннего определения и прогноза некоторых онкологических заболеваний» отмечена премией Правительства РФ 2009 года в области науки и техники для молодых ученых (распоряжение Правительства Российской Федерации от 1 марта 2010 года № 248-р г.Москва).
Структура и объем диссертации
Диссертация изложена на 235 страницах и состоит из введения, обзора литературы, описания материала и методов исследования, 2 глав результатов собственных исследований и обсуждения полученных результатов, заключения, выводов, практических рекомендаций и списка использованной литературы. Текст иллюстрирован 24 таблицами и 34 рисунками. Указатель литературы содержит 289 источников, из них 26 - отечественных.
Положения, выносимые на защиту
- Фактором риска развития ОКС у больных ИБС является нарушение регуляции гемостаза, обусловленное ростом уровня экспрессии ключевого компонента системы фибринолиза PAI-1 в моноцитах периферической крови.
- Изменение соотношения уровня СРБ и адипонектина в плазме крови больных со стабильным течением ИБС, а именно рост уровня СРБ при снижении уровня адипонектина свидетельствует о развитии воспаления и, как следствие, осложнений ИБС.
- Структурная и функциональная патология генов-супрессоров VHL, RASSF1, FHIT и CDH1 имеют существенную диагностическую, прогностическую и терапевтическую значимость при СРП.
- Аллельные делеции локуса 16q23, метилирование генов GSTP1 и N33 и экспрессия химерного гена TMPRSS2/ERG4 являются ключевыми нарушениями при РПЖ и могут быть использованы в качестве маркеров для диагностики, прогноза течения и оценки эффективности лечения заболевания.
- Система эпигенетических маркеров (аномальное метилирование Р16, MLH1 и N33) имеет 85%-ю чувствительность и специфичность и может быть использована для ранней диагностики рака шейки матки.
- Моносомия по хромосоме 3 и аллельные делеции хромосомного района 1р36 при увеальной меланоме позволяют определять пациентов с агрессивным течением и высоким риском метастазирования первичной опухоли.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Биомаркеры в диагностике и определении прогноза ишемической болезни сердца.
Было обследовано 162 пациента с ИБС в возрасте от 38 до 87 лет (62.5 ± 34.6 лет), находившихся на стационарном лечении в Клинике кардиологии Первого МГМУ им. И.М.Сеченова с апреля 2006 г. по апрель 2008 г. С учетом цели и задач исследования пациенты были разделены на три основные группы. Группы сравнения составили 31 больной с ОКС (из которых 8 – с инфарктом миокарда (ИМ), остальные больные – с нестабильной стенокардией) и 131 больной со стабильным течением ИБС. Во второй группе (больных со стабильным течением ИБС) были объединены пациенты со стабильной стенокардией. В зависимости от наличия или отсутствия сахарного диабета II типа и ожирения группы сравнения были поделены на две подгруппы. В третью (контрольную) группу включили 20 пациентов, которые в целом не отличались по возрасту от больных и у которых диагноз ИБС был отвергнут на основании данных стационарного обследования.
Критериями исключения из исследования были злокачественные новообразования, воспалительные заболевания в стадии обострения, признаки острого или обострения хронического инфекционного заболевания.
Клиническое исследование включало изучение анамнеза и данных объективного исследования с использованием лабораторно-инструментальных методов.
Все пациенты проходили обследование по схеме поэтапного ведения пациентов с возможной ишемической болезнью сердца, включающей в себя: общий анализ крови и мочи, биохимический анализ крови, анализ липидного спектра, анализ активности кардиоспецифических ферментов, а также электрокардиографию покоя, эхокардиографическое исследование, суточное мониторирование ЭКГ по Холтеру, нагрузочный тест (тредмил тест или велоэргометрия), сцинтиграфию миокарда (по показаниям), дуплексное сканирование артерий, коронароангиографию (по показаниям).
Диагноз острого ИМ и нестабильной стенокардии ставили на основании жалоб пациента, данных клинического обследования, характерных изменений на ЭКГ, ЭхоКГ, определения уровня маркеров некроза миокарда в крови.
У всех обследуемых пациентов однократно при госпитализации производили взятие венозной крови в рамках стандартного исследования крови при поступлении в стационар. Общее содержание глюкозы, холестерина и триглицеридов в плазме крови определяли ферментативными методами.
Помимо общеклинических исследований, у каждого пациента получали фракцию мононуклеарных лейкоцитов периферической крови (МЛПК), а также определяли уровень биологических маркеров (С-реактивного белка и адипонектина) в сыворотке крови иммуноферментным методом (ИФА).
Получение моноцитов из венозной крови.
Фракцию МЛПК получали с помощью градиентного центрифугирования цельной крови в растворе фиколл-пак (Pharmacia). Далее клетки фиксировали 4% параформальдегидом (ПФ) и исследовали уровень экспрессии ингибитора активатора плазминогена 1 типа и активатора плазминогена урокиназного типа в моноцитах с помощью метода проточной цитофлуориметрии.
Для исследования содержания белков PAI-1 и uPA в моноцитах методом иммуноцитохимии, полученную фракцию МЛПК культивировали в течение суток, затем отделяли от поверхности чашек Петри с помощью раствора Версена (раствор натриевой соли этилендиаминотетрауксусной кислоты) и проводили иммуноцитохимическое окрашивание.
Исследование экспрессии PAI-1 и uPA в моноцитах человека с помощью иммуноцитохимического метода.
Иммуноцитохимическое окрашивание проводили с использованием моноклональных антител мыши к белку PAI-1 (Santa Cruz Biotechnology, клон С-9) и поликлональных антител кролика к белку uPA (Santa Cruz Biotechnology, клон H-140) в разведении 1:50. Затем клетки инкубировали с FITC-конъюгированными вторичными антителами. Препараты исследовали с помощью флуоресцентной микроскопии. Стекла с контрольными клетками окрашивали с использованием системы визуализации Super Sensitive Polymer-HRP IHC Detection Sysytem/DAB (BioGenex). В качестве первичных антител использовали моноклональные мышиные антитела к CD68 (DAKO Cytomation, клон PG-M1, разведение 1:700).
Исследование экспрессии PAI-1 и uPA в моноцитах человека с помощью метода проточной цитофлуориметрии.
Окрашивание проводили с использованием первичных моноклональных антител мыши к белку PAI-1 и поликлональных антител кролика к uPA в разведении 1:20. Затем добавляли к суспензии клеток FITC-конъюгат козьих антител к IgG мыши и FITC-конъюгат антител козы к IgG кролика (Santa Cruz Biotechnology) в разведении 1:500; инкубировали с моноклональными антителами мыши к CD14, меченными фикоэритрином (CD14-РЕ) ("Сорбент"). Интенсивность флуоресценции измеряли с помощью проточного цитофлуориметра EPICS-XL (Вeckman Coulter).
Исследование экспрессии PAI-1 и uPA в атеросклеротических бляшках (АСБ) коронарных артерий с помощью иммуногистохимического метода и в моноцитах крови с помощью метода проточной цитофлуориметрии.
Было обследовано 7 пациентов с ИБС в возрасте от 47 до 72 лет, находившихся на стационарном лечении в отделении кардиохирургии Клиники сердечно-сосудистой и общей хирургии Первого МГМУ им. И.М. Сеченова с марта 2009 г. по май 2010 г. Группы сравнения составили 4 пациента со стабильным течением ИБС (стенокардия напряжения) и 3 пациента с ОКС (2 из них – с острым ИМ, 1 – с нестабильной стенокардией). У всех пациентов, за исключением одного из группы ОКС+, отмечался в анамнезе ИМ.
Взятие венозной крови производился перед операцией в стандартных условиях утром через 12-14 часов после приёма пищи. Выделение моноцитов и исследование экспрессии PAI-1 и uPA проводили с помощью метода проточной цитофлуориметрии по описанной выше методике.
Фрагменты коронарных артерий, полученных во время операции маммарокоронарного шунтирования/аортокоронарного шунтирования, фиксировали в 10% забуференном формалине в течение суток. В качестве контроля взяли фрагмент лучевой артерии одного из пациентов, полученный также во время операции.
Морфологическое исследование проводили на срезах толщиной 3-4 мкм, окрашенных гематоксилином и эозином. Иммуногистохимическое исследование проводили с использованием системы визуализации Super Sensitive Polymer-HRP IHC Detection Sysytem/DAB (BioGenex) в соответствии с прилагаемой инструкцией. В качестве первичных антител использовали кроличьи поликлональные антитела к урокиназе (abcam, разведение 1:50) и мышиные моноклональные антитела к PAI-1 (Santa Cruz, клон TJA6, разведение 1:50).
Определение биохимических маркеров атерогенеза в сыворотке крови методом ИФА.
В работе для сэндвич-ИФА использовали наборы «ИФА СРБ» и «ИФА Адипонектин» на основе антител, полученных в совместных исследованиях Московским НИИ Медицинской Экологии, МГУ им. М.В. Ломоносова и лабораторией электронной микроскопии и иммуногистохимии Централизованного патологоанатомического отделения Первого Московского государственного медицинского университета им. И.М. Сеченова.
Статистическая обработка данных.
Статистическая обработка результатов проводилась с помощью компьютерной обработки данных в программах STATISTICA 6.0 и SPSS statistics 17.0. Статистические различия выборок оценивали по критерию Манна-Уитни (Mann-Whitney U-test). ROC-анализ проводили с помощью программы "SPSS statistics 17.0". Получали графические изображения характеристических кривых (ROC-curves, Receiver-Operator Characteristic curve) и площадь под кривой - AUC (Area Under Curve). Качество модели (диагностическая эффективность показателя) оценивалась по общепринятой экспертной шкале для значений AUC.
Поиск ключевых маркеров и разработка ДНК-диагностических протоколов для ряда онкологических заболеваний.
Клинический материал.
С целью оценки прогрессии первичной опухоли при светлоклеточном раке почки исследованы аллельные делеции генов VHL, RASSF1, FHIT и CDH1 на материале 94 парных образцов (опухоль-норма) светлоклеточного рака почки, полученных от пациентов, проходивших лечение в Клинике урологии им. Р.М. Фронштейна Первого МГМУ им. И.М.Сеченова; а также аномальное метилирование генов-супрессоров на материале 98 парных образцов светлоклеточных карцином и 29 парафиновых блоков СРП, полученных от пациентов, проходивших лечение в той же клинике. Для разработки молекулярно-генетической методики определения эффективности таргетной терапии при светлоклеточном раке почки использовали материал 123 удаленных первичных опухолей, полученных от пациентов, проходивших лечение в той же клинике. Для анализа полиморфных вариантов генов ABCB1, TGFBR1, IL10 и VDR в норме и при спорадическом раке почки исследовано 98 парных образцов рака почки (РП) (опухоль-норма), предоставленных Медицинским радиологическим научным центром РАМН и Клиникой урологии им. Р.М. Фронштейна Первого МГМУ им. И.М.Сеченова. В качестве популяционного контроля использовали 151 образец крови здоровых доноров, предоставленный донорским пунктом Первого МГМУ им. И.М.Сеченова.
Для определения потери гетерозиготности и микросателлитной нестабильности хромосомных районов 13q14 и 16q23 у пациентов с подозрением на рак предстательной железы исследован 51 микродиссекционный образец больных с аденокарциномой предстательной железы (АКПЖ), 25 – с простатической интраэпителиальной неоплазией (ПИН), и 24 – с доброкачественной гиперплазией предстательной железы (ДГПЖ). Для исследования экспрессии химерного гена TMPRSS2/EGR4 при раке предстательной железы образцы ткани предстательной железы (ПЖ) были получены от 63 пациентов с диагнозом «рак предстательной железы», подвергшихся радикальной простатэктомии. Также 10 образцов ПЖ были получены от пациентов с диагнозом «ДГПЖ». Образцы ткани предстательной железы для определения маркеров метилирования представляли собой операционный материал больных с аденокарциномой, ПИН и ДГПЖ, а также был получен аутопсийный материал нормальной ПЖ. Все пациенты проходили лечение в отделении онкоурологии Московского научно-исследовательского онкологического центра им. П.А. Герцена.
Для определения аномального метилирования генов при раке шейки матки были исследованы образцы дисплазий шейки матки (97 образцов), морфологически неизмененных тканей, прилегающих к дисплазии (51 образец), и образцы крови больных. Цервикальные мазки здоровых женщин (35 образцов) и женщин с фоновыми заболеваниями, которые представлены эрозией шейки матки и цервикальной эктопией с выраженным воспалительным процессом (93 образца), были взяты в женской консультации.
С целью выявления специфических молекулярных маркеров и оценки прогрессии первичной опухоли при увеальной меланоме были исследованы 107 парных образцов (норма-опухоль), полученных при операции энуклеации, и 17 образцов биоптатов, взятых методом тонкоигольной аспирационной биопсии (ТИАБ), с соответствующими образцами периферической крови. Образцы получены от пациентов, проходивших обследование и лечение в Московском НИИ глазных болезней им. Гельмгольца.
Для молекулярно-генетического анализа клональной внутриопухолевой гетерогенности в колоректальных карциномах образцы опухолей получены от 11 пациентов отделения колопроктологии Научного центра хирургии им. Б.В. Петровского РАМН. Все пациенты с первичными опухолями толстой кишки, представленными аденокарциномами без гематогенных метастазов, не получавших ранее химиотерапевтического и лучевого лечения, без других онкологических заболеваний в анамнезе. Все опухоли после морфологического исследования классифицированы по TNM в зависимости от глубины инвазии опухоли и наличия пораженных лимфатических узлов. Также для генетического анализа дополнительно брали венозную кровь больных.
Методы выделения ДНК и РНК.
Выделение ДНК из парафиновых блоков проводили с гистологических срезов, полученных с помощью микротома. Проводили их депарафинизацию, опухолевые клетки и строму инкубировали с экстракционным буфером. Полученный лизат клеток, содержащий геномную ДНК, использовали для постановки ПЦР. Данную методику использовали для оценки прогрессии первичной опухоли и разработки молекулярно-генетической методики определения эффективности таргетной терапии при СРП, а также исследования клональной внутриопухолевой гетерогенности колоректальных карцином.
Выделение ДНК из свежего операционного и биопсийного материала, а также МЛПК проводили при исследовании спорадического рака почки, увеальной меланомы, РШМ (только биоптаты и соскобы). Геномную ДНК из МЛПК и замороженных тканей выделяли методом обработки образцов протеиназой К с последующей фенол-хлороформной экстракцией.
Лазерную микродиссекцию проводили на ткани рака предстательной железы для определения потери гетерозиготности и микросателлитной нестабильности хромосомных районов 13q14 и 16q23, а также определения маркеров метилирования, с помощью системы лазерной микродиссекции ASLMD (Leica microsystems, Германия). Клетки, полученные с помощью микродиссекции, обрабатывали буфером, содержащим протеиназу К. Полученный после инкубации раствор использовали для ПЦР.
Выделение РНК из операционного материала выполняли на ткани рака предстательной железы для исследования экспрессии химерного гена TMPRSS2/EGR4. Выделение РНК проводили методом кислофенольной экстракции с использованием набора “РИБО-золь-А” (фирма АмплиСенс, Россия) по протоколу фирмы-производителя.
Потерю гетерозиготности в опухолевом материале определяли методом микросателлитного анализа. При исследовании ПГ в образцах СРП использовали по два динуклеотидных микросателлита на каждый из анализируемых генов: делеции VHL выявляли с помощью STR-маркеров D3S1317 и D3S1038, RASSF1 – D3S1568 и D3S966, FHIT – D3S1300 и D3S1234. При исследовании РПЖ для идентификации ПГ и МН в хромосомных районах 13q14 и 16q23 использовали 3 высокополиморфных маркера: RB20int (внутригенный маркер RB1), D16S534, D16S422. Для выявления специфических молекулярных маркеров и оценки прогрессии первичной опухоли при увеальной меланоме проводили ПЦР микросателлитных маркеров D1S3669, D1S407, D1S1635, D1S2145, D1S243, D3S2398, D3S3520, 16xTG_3q26.31, D3S2459, D3S1234, D3S1300, D3S966, D3S1568, D3S1317, D3S1038. При исследовании колоректального рака определяли ПГ локусов 9p21 (D9S942), 13p14 (RB1int20), 10q23 (D10S1761) и 17p13 (PT53).
Методы анализа мутаций.
Для оценки эффективности таргетной терапии при СРП анализ мутаций в кодирующей части гена VHL проводили с помощью SSCP-анализа (анализ конформационного полиморфизма однонитевой ДНК) ПЦР-продуктов и секвенирования. Мутации гена K-RAS при исследовании колоректального рака определяли аналогично.
Секвенирование ПЦР-продуктов проводили с использованием набора BigDye® Terminator v 3.1. Cycle Sequencing Kit фирмы “Applied Biosystems”. с последующим анализом на генетическом анализаторе ABI PRISM 3100 по протоколам фирмы “Applied Biosystems”, США.
Исследование полиморфных вариантов генов.
Мультилокусную ПЦР полиморфизмов генов ABCB1, TGFBR1, IL10 и VDR при спорадическом РП проводили с использованием праймеров, фланкирующих исследуемые однонуклеотидные полиморфизмы (SNP - single nucleotide polymorphism) в каждом из генов. Определение SNP проводили методом мини-секвенирования.
Методы анализа химерных генов.
Для исследования экспрессии химерного гена TMPRSS2/EGR4 при РПЖ образцы РНК, растворенные в РНК-элюэнте (АмплиСенс, Россия), обрабатывали ДНКазой. Обратную транскрипцию РНК проводили методом случайного праймирования с использованием High-Capacity cDNA Archive kit (Applied Biosystems, США) по протоколу фирмы-производителя в термоциклере GeneAmp2700. Затем проводили ПЦР и прямое секвенирование для определения химерных генов.
Методы анализа метилирования.
При СРП для анализа метилирования промоторов генов CDH1 и VHL проводили обработку геномной ДНК метилчувствительной рестриктазой BstHHI («СибЭнзим», Новосибирск), которая служила матрицей для метилчувствительной ПЦР (МЧ-ПЦР). При РШМ для анализа метилирования промоторных областей генов Р16, MLH1 и N33 проводили обработку геномной ДНК метилчувствительной рестриктазой HpaII. Метилирование генов определяли с помощью МЧ-ПЦР.
Электрофорез ПЦР-продуктов в 8%-ном полиакриламидном геле (ПААГ).
Разделение ПЦР-продуктов по молекулярному весу при анализе метилирования проводили с помощью вертикального электрофореза в 8%-ном ПААГ. ПГ определяли с помощью электрофореза в 10%-ом денатурирующем ПААГ. Визуальный контроль миграции ПЦР-продуктов осуществляли относительно положения красителей бромфенолового синего и ксиленцианола. Затем проводили окрашивание ПААГ нитратом серебра.
Статистическая обработка данных.
Статистическую обработку данных проводили при помощи программы Graph Pad Instant 3.05. Уровень значимости был принят равным 0,05. Многофакторный регрессионный анализ проводили с помощью программы Statistica v. 6.0.
Для анализа клинических ассоциаций химерного гена с прогрессией РПЖ были выбраны следующие критерии: степень дифференцировки опухоли по классификации Глисона, стадия процесса и наличие гормонального лечения перед простатэктомией. Пациентов делили на три группы по выбранному критерию и сравнивали в этих группах частоты химерного гена с помощью критерия Фишера.
Для изучения возможной связи между метилированием каждого из исследуемых генов и гистологическим критерием (степень диспластического процесса шейки матки; РПЖ, простатическая интраэпителиальная неоплазия или ДГПЖ) использовали сравнение групп с помощью критерия 2. Чувствительность маркера рассчитывали как отношение истинно положительных результатов к сумме истинно положительных и ложноотрицательных результатов. Специфичность маркера рассчитывали по формуле: отношение истинно отрицательных результатов к сумме ложноположительных и истинно отрицательных результатов.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ.
БИОМАРКЕРЫ В ДИАГНОСТИКЕ И ПРОГНОЗИРОВАНИИ РАЗЛИЧНЫХ ФОРМ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА.
Сравнительная характеристика больных ИБС с ОКС и без ОКС по основным метаболическим параметрам.
В группах больных ИБС с ОКС (n=31) и без ОКС (n=131) было проведено сопоставление основных метаболических параметров (табл. 1).
Таблица 1. Характеристика и основные метаболические параметры больных ИБС.
| Показатель | ОКС+ (n=31) | ОКС- (n=131) | р |
| Возраст (лет) | 69.26±11.33 | 66.02±10.02 | 0.12 |
| Индекс массы тела (кг/м2) | 29.88±5.11 | 30.25±5.15 | 0.80 |
| Глюкоза плазмы крови (мг/дл) | 107.83±42.96 | 107.27±42.75 | 0.95 |
| Триглицериды (мг/дл) | 173.52±85.37 | 169.31±83.43 | 0.82 |
| Общий холестерин (мг/дл) | 205,67±63,33 | 210,07±57,22 | 0.72 |
| Холестерин ЛПВП (мг/дл) | 49.62±13.40 | 52.10±12.87 | 0.38 |
| Холестерин ЛПНП (мг/дл) | 121.18±46.43 | 135.80±97.78 | 0.45 |
| Холестерин ЛОНП (мг/дл) | 34.67±17.05 | 32.99±15.29 | 0.62 |
Примечание: * - отличия достоверны при значении р менее 0,05
Анализ данных по содержанию липидов в плазме крови показал, что уровень липопротеинов низкой плотности (ЛПНП) выходил за пределы рекомендуемых (норма 100 мг/дл), содержание триглицеридов (норма 150 мг/дл) и общего холестерина (норма 200 мг/дл) было повышено, а содержание липопротеинов высокой плотности (ЛПВП) (норма 45 мг/дл), липопротеинов очень низкой плотности (ЛОНП) (норма 200 мг/дл) у лиц обеих групп не выходило за пределы нормы. При этом достоверных различий по этим параметрам между группами больных с ОКС и без ОКС выявлено не было. Среднее содержание глюкозы в плазме крови у больных обеих групп было близким и практически нормальным (норма 110 мг/дл). Также не было статистически значимых различий между этими группами по таким показателям, как средний возраст и индекс массы тела пациентов.
Таким образом, стандартные показатели липидного спектра и уровня глюкозы в сыворотке крови больных со стабильным и нестабильным течением ИБС статистически не различались, что исключает возможность их использования в качестве критериев, с помощью которых можно определять риск возникновения ОКС у больных со стабильным течением ИБС. Поэтому далее проводили исследование и оценку ассоциации с заболеванием биохимических маркеров, в соответствии с изменениями уровней которых в клетках или сыворотке венозной крови можно было бы проводить дифференциальную диагностику сложных форм ИБС и прогнозировать риск развития осложнений.
Характеристика уровня u-PA и PAI-1 в моноцитах периферической крови методами иммуноцитохимического окрашивания и проточной цитофлуориметрии.
Изменение содержания в крови компонентов фибринолитической системы является одним из факторов риска развития ОКС у больных ИБС. На поздних стадиях атерогенеза увеличение экспрессии u-PA приводит к повышенному протеолизу в атеросклеротических бляшках коронарных артерий и, в конечном итоге, к их разрыву с последующим образованием тромботических наслоений в просвете сосуда (Brown N.J. et al., 2002). PAI-1, инактивируя урокиназу, ограничивает фибринолитическую активность местом расположения гемостатической пробки и предотвращает преждевременный лизис фибрина (Folsom A.R., 2001). Однако высокое содержание PAI-1 блокирует миграцию гладкомышечных клеток и способствует формированию нестабильных бляшек со сниженным содержанием этих клеток в сосудистой интиме, поэтому повышение концентрации этого белка в плазме крови больных ИБС также ассоциируется с плохим прогнозом заболевания (Lijnen H.R., 2002).
В основе патогенеза атеросклероза лежит хроническое воспаление сосудистой стенки, протекающее с преобладанием пролиферативного компонента, основными клеточными эффекторами которого являются моноциты циркулирующей крови. Учитывая также тот факт, что макрофагальные «пенистые» клетки, образовавшиеся из моноцитов, являются типичным компонентом атеросклеротической бляшки, уровень экспрессии u-PA и PAI-1 определяли в моноцитах периферической крови больных со стабильным течением ИБС и больных с ОКС. В группы сравнения из общего числа обследованных больных вошли 15 пациентов с ОКС (из них 6 человек с инфарктом миокарда, остальные больные с нестабильной стенокардией) и 27 больных со стабильным течением ИБС.
Для характеристики уровня uPA и PAI-1 в моноцитах периферической крови определяли количество клеток, окрашенных антителами к исследуемым белкам и содержание этих белков в клетках с помощью двух различных методов: иммуноцитохимического окрашивания и проточной цитофлуориметрии.
По данным, полученным с помощью иммуноцитохимического метода, все CD68-положительные клетки окрашивались антителами к uPA и PAI-1. Процент клеток в популяции, окрашенных антителами к исследуемым антигенам, не различался во всех группах и составлял от 77% до 99%. Однако интенсивность окрашивания и локализация окраски была различна в случае uPA и PAI-1: наиболее интенсивно клетки окрашивались антителами к PAI-1, что свидетельствует о более высоком уровне этого белка в клетках по сравнению с uPA.
Цитофлуориметрический анализ, преимуществом которого является возможность не только рассчитать процент клеток в популяции, экспрессирующих исследуемые белки, но и оценить их количество, с одной стороны, подтвердил полученные с помощью иммуноцитохимического окрашивания результаты, а с другой, позволил количественно охарактеризовать содержание uPA и PAI-1 в клетках.
Данные, полученные с помощью метода проточной цитофлуориметрии и представленные на рис. 1, показывают, что среди CD14-положительных клеток, процент окрашенных антителами к uPA и PAI-1 очень высок и обнаруживается в 81.9-99.9% клеток. При этом плотность экспрессии uPA и PAI-1, оцениваема по значению средней интенсивности флуоресценции (MFI) клеток, была различна в каждом случае, причем плотность экспрессии PAI-1 оказалась более высокой, чем uPA.

Рис. 1. Исследование плотности экспрессии белков uPA и PAI-1 в CD14+ моноцитах методом проточной цитофлуориметрии. А – выявление популяции CD14+ моноцитов после окрашивания CD14-РE (красная флуоресценция). По оси абсцисс – структура клеток, усл. ед., по оси ординат – размер клеток, усл.ед. Б, В, Г – гистограммы окрашивания FITC-меченными антителами к uPA (пик 2) и PAI-1 (пик 3) CD14+ моноцитов здорового добровольца (Б), больного со стабильным течением ИБС (В) и больного с ОКС (Г). Пик 1 – флуоресценция клеток, окрашенных только CD14-РE. По оси абсцисс – интенсивность зеленой флуоресценции, усл.ед., по оси ординат – количество клеток, усл.ед.
При сравнительном анализе плотности экспрессии uPA и PAI-1 в моноцитах крови больных оказалось, что плотность экспрессии PAI-1 достоверно более высокая у больных с ОКС, чем у больных без ОКС и чем в группе контроля (соответственно 49.11±16.64, 37.95±18.43 (р<0.05) и 14.82±6.09 (р<0.0001)) (рис. 2А). По плотности экспрессии uPA не было обнаружено достоверных различий между группами больных с ОКС и без ОКС, однако она оказалась достоверно более высокой по сравнению с контрольной группой (соответственно 5.04±1.30, 4.84±1.92 (р>0.05) и 2.25±0.88 (р<0.0001)) (рис. 2 Б).
Рис. 2. Плотность экспрессии белков PAI-1 (А) и uPA (Б) в моноцитах периферической крови здоровых добровольцев (1), больных со стабильным течением ИБС (2) и больных с ОКС (3).
Полученные данные свидетельствуют о том, что плотность экспрессии исследуемых маркеров у больных ИБС достоверно более высокая, чем в контрольной группе, причем при стабильном течении ИБС плотность экспрессии PAI-1 в моноцитах периферической крови достоверно ниже, а при развитии нестабильной стенокардии и инфаркте миокарда наблюдается ее повышение.
Таким образом, выявление более высокого уровня экспрессии PAI-1 в моноцитах периферической крови больных с ОКС позволяет предположить, что высокая локальная концентрация этого белка в атеросклеротических бляшках, независимо от уровня uPA, может приводить к их дестабилизации с развитием клинической картины острого коронарного синдрома.
Исследование экспрессии PAI-1 и uPA в атеросклеротических бляшках коронарных артерий с помощью иммуногистохимического метода и в моноцитах крови с помощью метода проточной цитофлуориметрии.
При морфологическом исследовании в 6 из 7 гистологических препаратов стенок коронарных артерий отмечались стабильные АСБ, в одном случае (группа ОКС-) АСБ была классифицирована как нестабильная (уязвимая).
При иммуногистохимическом (ИГХ) исследовании экспрессия uPA и PAI-1 отмечалась в клетках воспалительного инфильтрата и ГМК АСБ, интенсивность иммунопероксидазного окрашивания колебалась от слабого до выраженного (табл. 2). Более выраженная экспрессия uPA отмечалась в группе больных с ОКС по сравнению с группой больных без ОКС. При этом экспрессия uPA в ГМК в обеих группах была повышена по сравнению с нормой. Содержание PAI-1 в АСБ пациентов со стабильной формой ИБС, напротив, было выше, чем у пациентов с ОКС. При этом в норме экспрессия PAI-1 в ГМК не наблюдалась (табл. 2). Повышенный уровень PAI-1 отмечается у пациентов со стабильной ИБС и ОКС в стенках пораженных атеросклерозом коронарных артерий, что подтверждает тот факт, что PAI-1 может служить фактором риска развития тромбоза коронарных артерий (Salame M.Y. et al., 2000).
При сравнении содержания uPA и PAI-1 в моноцитах этих больных иммуноцитофлуориметрическим методом не было обнаружено достоверных различий между группами больных с ОКС и без ОКС по плотности экспрессии uPA и PAI-1. В то же время во всех случаях плотность экспрессии PAI-1 оказалась более высокой, чем uPA, и также процент окрашенных антителами к PAI-1 клеток был гораздо выше.
Таблица 2. Экспрессия uPA и PAI-1 в атеросклеротических бляшках коронарных артерий больных с ОКС и со стабильным течением ИБС.
| № препарата | uPA | PAI-1 | ||
| восп. инфильтрат | ГМК | восп. инфильтрат | ГМК | |
| ла-1 (контр.) | отсутствует | + | отсутствует | - |
| ОКС+ | ||||
| ка-1 | ++ | +++ | + | - |
| ка-4 | ++ | + | +++ | + |
| ка-5 | отсутствует | +++ | отсутствует | + |
| ОКС- | ||||
| ка-2 | + | ++ | + | + |
| ка-3 | отсутствует | ++ | отсутствует | + |
| ка-6 | ++ | +++ | ++ | ++ |
| ка-7 | + | +++ | ++ | +++ |
Примечание: «-» - иммунопероксидазное окрашивание отсутствует; «+» - слабое иммунопероксидазное окрашивание и/или окрашивание части клеток; «++» - умеренное иммунопероксидазное окрашивание; «отсутствует» - воспалительный инфильтрат отсутствует.
Таким образом, можно предположить, что нестабильность АСБ и, соответственно, развитие ОКС может определяться повышением уровня экспрессии PAI-1 в воспалительном инфильтрате АСБ, приводящим к снижению фибринолитической активности в области АСБ.
В то же время, выявленная более выраженная экспрессия uPA по сравнению с PAI-1 в группе ОКС+ в ГМК, возможно, тоже влияет на стабильность АСБ. По литературным данным, на поздних стадиях атерогенеза увеличение экспрессии uPA приводит к повышенному протеолизу в атеросклеротических бляшках коронарных артерий. Превалирование содержания активатора плазминогена над содержанием его ингибитора делает возможным усиление активности данной протеиназы. Это, в свою очередь, приводит к разрыву АСБ с последующим образованием пристеночных тромбов в просвете сосуда (Brown N.J. et al., 2002).
Полученные данные позволяют заключить, что повышение экспрессии PAI-1 в моноцитах крови и также в воспалительном инфильтрате АСБ больных со стабильным течением ИБС может приводить к дестабилизации АСБ. А повышенная экспрессия uPA в ГМК - определять нестабильность АСБ на поздних стадиях атеросклероза.
Изучение уровня биохимических маркеров атерогенеза в сыворотке крови больных со стабильным течением ишемической болезни сердца и с острым коронарным синдромом.
Маркеры воспаления – одно из важных направлений поиска биомаркеров сердечно-сосудистых заболеваний. Важную роль в атерогенезе, включая развитие повреждения сосудистой стенки, нестабильность АСБ и возникновение тромботических осложнений, играет воспаление, степень которого возможно оценивать по изменению уровня СРБ и адипонектина. Уровень гормона жировой ткани адипонектина также связан с большинством метаболических проявлений и наиболее полно отражает тяжесть гормональных и метаболических нарушений у больных с атеросклерозом коронарных сосудов.
В связи с этим, для установления связи развития осложнений ИБС в виде ОКС с механизмами развития атеросклероза, сравнивали уровень адипонектина и СРБ в сыворотках крови больных со стабильным течением ИБС (n=131) и больных с ОКС (n=31).
Таблица 3. Сравнительная характеристика уровня биохимических маркеров в группах больных ИБС и в контрольной группе.
| Показатель | ОКС+ (n=31) | ОКС- (n=131) | Контрольная группа (n=20) | р |
| СРБ, мкг/мл | 14.99±19.96 | 7.93±9.44 | 2.03±1.81 | 0.004* 0.005** |
| Адипонектин, мкг/мл | 8.86±3.55 | 11.58±5.92 | 14.83±1.81 | 0.01* 0.001** |
Примечание: * - отличия достоверны между показателями группы ОКС- и контрольной группы; ** - отличия достоверны между показателями группы ОКС- и ОКС+
Проведенные исследования показали, что содержание изучаемых маркеров в сыворотке крови контрольной группы соответствует норме и статистически отличается от содержания медиаторов в крови больных, выявлены также статистически значимые различия между группами больных с ОКС и без ОКС (табл. 3).
По результатам исследований уровня СРБ и адипонектина в исследуемых группах больных установлено достоверное увеличение концентрации СРБ в сыворотке крови больных с ОКС по сравнению с его концентрацией у больных без ОКС и по сравнению с контрольной группой (соответственно 14.99±19.96, 7.93±9.44 (р=0.004) и 2.03±1.81 (р<0.005)) (рис. 3А). А уровень адипонектина оказался достоверно более низким у больных с ОКС, чем у больных без ОКС и по сравнению с контрольной группой (соответственно 8.86±3.55, 11.58±5.92 (р=0.01) и 14.83±1.81 (р<0.001)) (рис. 3Б).
Анализ характеристической кривой для СРБ показал, что данный маркер имеет хорошую диагностическую эффективность в отношении ИБС и в группе больных ОКС,- и в группе ОКС+. Площадь под кривой (AUC) равна 0.74 и 0.78, соответственно, рассчитанное программой оптимальное пороговое значение «cut-off» составило > 4.4 и 5.5 мкг/мл, чувствительность 57% и 61%, специфичность 95% и 90%, соответственно. При использовании порогового значения, указанного производителем диагностикума и равного 4 мкг/мл, чувствительность составила 61%, специфичность – 90%, диагностическая точность – 76% для обеих групп.


Рис. 3. Уровень С-реактивного белка (А) и адипонектина (Б) в периферической крови здоровых добровольцев, больных со стабильным течением ИБС и больных с ОКС.
В отношении адипонектина как потенциального маркера для оценки состояния больных со стабильной ИБС, следует отметить, что при значении «cut-off» < 11 мкг/мл, этот маркер обладает специфичностью 95%, показатель чувствительности равен 54%, AUC = 0.6. В отношении группы ОКС+ этот маркер показал очень хорошую диагностическую эффективность AUC = 0.85, специфичность – 95%, чувствительность – 83%.
Учитывая тот факт, что у части больных в обеих группах было выявлено ожирение или СД II, в рамках проведенного исследования было изучено влияние наличия или отсутствия этих заболеваний у больных с ОКС и без ОКС на показатели уровня СРБ и адипонектина в сыворотке крови.
В зависимости от наличия или отсутствия ожирения или СД II, больные с ОКС+ и ОКС- были разделены на две подгруппы. Хотя уровень СРБ и был несколько выше в случае наличия ожирения или СД II, однако достоверных отличий между подгруппами больных I и II обнаружено не было. Также не наблюдалось достоверных отличий по уровню адипонектина между этими подгруппами, хотя можно отметить несколько более низкие средние значения концентрации этого гормона у больных подгруппы I по сравнению с больными подгруппы II (соответственно, 10.78±4.86 и 11.85±1.54 у больных без ОКС, 8.27±2.95 и 9.26±3.94 с ОКС) (рис. 4). В то же время средние значения этих показателей достоверно различались с показателями контрольной группы (рис. 4). Возможно, отсутствие статистически значимых различий исследуемых параметров между сравниваемыми подгруппами объясняется недостаточной выборкой.
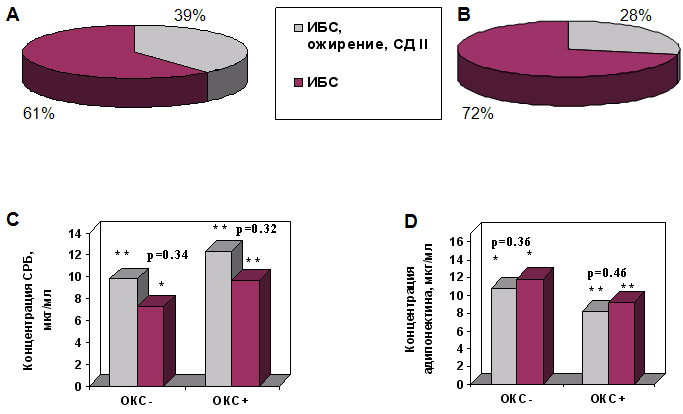
Рис. 4. Распределение больных ИБС (n=162) по наличию ожирения и СД II (подгруппа I, (n=12)) среди больных с ОКС (n=31) (А) и среди больных без ОКС (n=131) (подгруппа I, (n=37)) (Б) и связь наличия ожирения и СД II с уровнем СРБ (С) и адипонектина (Д) в группах больных с ОКС и без ОКС.
* - отличия достоверны по отношению к показателям контрольной группы (р<0,05)
** - отличия достоверны по отношению к показателям контрольной группы (р<0,001)
Полученные данные позволяют нам присоединиться к мнению Shetty G.K. et al. (2004), которые считают, что снижение содержания адипонектина и повышение уровня СРБ может явиться не только важным маркером риска, но также и фактором риска прогрессирования ИБС, в особенности у лиц с ожирением и сахарным диабетом II типа.
Вышеизложенные результаты, а также тот факт, что при сопоставлении уровня адипонектина в сыворотке крови с метаболическими параметрами оказалось, что четкой зависимости содержания адипонектина в сыворотке крови от массы тела больных ИБС не было выявлено, указывают на то, что при сердечно-сосудистых патологиях адипонектин является в большей степени маркером воспаления, а не метаболических проявлений, и также фактором риска прогрессии воспалительных процессов у больных ИБС. А также полученные данные позволяют заключить, что наличие ожирения и СД II, часто сопровождающее ИБС, не может приводить к появлению ложноотрицательных результатов при использовании адипонектина в качестве биомаркера.
Таким образом, можно предположить, что наряду с СРБ, уже применяемым для оценки риска по критериям Рейнольдса (Ridker P.M., Buring J.E. et al., 2007; Ridker P.M., Paynter N.P. et al., 2008) и включенным в список маркеров риска сердечно-сосудистых заболеваний Европейской ассоциацией кардиологов (Graham I. et al., 2007), исследование уровня адипонектина может являться дополнительным критерием риска осложнений ИБС.
Анализ результатов парного корреляционного анализа разрешил нам обнаружить взаимосвязь между содержанием адипонектина в сыворотке крови и концентрацией СРБ: обнаружена обратная статистически значимая корреляция уровня адипонектина с уровнем СРБ в общей группе больных без ОКС (r = – 0.21, p = 0.01, у = 12,65 – 0,13 x) (рис. 5).

Рис. 5. Анализ корреляции уровня адипонектина с концентрацией СРБ в сыворотке крови больных со стабильным течением ИБС.
Обнаруженная обратная статистически значимая корреляция концентрации адипонектина с уровнем СРБ указывает о влиянии адипонектина на течение болезни путем активации воспалительного процесса, поэтому взаимосвязанное изменение этих показателей в сыворотке крови при стабильном течении ИБС может являться дополнительным критерием для оценки степени риска отдаленных неблагоприятных исходов у таких больных.
Анализируя полученные данные с учетом биологической роли исследуемых маркеров, можно заключить, что высокий уровень СРБ и низкий уровень адипонектина могут являться значимыми показателями тяжести воспаления и, соответственно, важными критериями риска развития ОКС у больных ИБС. Наличие ожирения или СД II у этих больных, возможно, ассоциировано с более высокой вероятностью развития ОКС.
ПОИСК КЛЮЧЕВЫХ МАРКЕРОВ И РАЗРАБОТКА ДНК-ДИАГНОСТИЧЕСКИХ ПРОТОКОЛОВ ДЛЯ РЯДА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ
Ключевые маркеры и ДНК-диагностические протоколы для светлоклеточного рака почки.
Связь аллельных делеций генов VHL, RASSF1, FHIT с прогнозом заболевания.
Для СРП характерны аллельные делеции генов-супрессоров, локализованных в области хромосомы 3р, которые могут оказывать влияние на развитие злокачественного новообразования. Для определения прогностической значимости аллельных делеций генов-супрессоров в настоящем исследовании определена ПГ областей локализации генов VHL (подавляет экспрессию генов, активируемых при гипоксии), RASSF1 (негативный регулятор клеточного цикла, участвует в индукции апоптоза), FHIT (негативный регулятор клеточного цикла) (рис. 6).

Рис. 6. Выявление потери гетерозиготности.
А – результат электрофореза в 8% ПААГ маркера D3S1234 гена FHIT (T и N – опухолевая и нормальная ткани, соответственно), 1 – гомозигота, 2 – ПГ в опухолевой ткани, 3 – нормальная гетерозигота; В – результат денатурирующего электрофореза в ПААГ микросателлита D3S1568 (образцы нанесены на гель в обратном порядке), 4 – гомозигота, 5 – ПГ в опухолевой ткани (область гена RASSF1), 6 – нормальная гетерозигота.
ПГ гена RASSF1 обнаружена в 27.5% (22/80), FHIT – 35.6% (32/90) и VHL – 27.9% (24/86) информативных образцов СРП. Аллельные делеции хотя бы одного гена на 3р наблюдали в 56.4% (53/94), а в совокупности из трех исследованных генов – в 60.6% (57/94) информативных случаев. Проведен сравнительный анализ встречаемости ПГ в парных клинических группах: по стадии заболевания, степени дифференцировки первичной опухоли, распространению первичной опухоли за пределы капсулы почки, наличию/отсутствию метастазов. Выявлена ассоциация аллельных делеций по двум и более генам-супрессорам, локализованным на коротком плече хромосомы 3, только с наличием метастазов на момент постановки диагноза: p = 0.036, OR = 1.49 (95% CI: 1.01-2.33). По всей видимости, ПГ двух и более генов-супрессоров, наиболее часто делетируемых при СРП, оказывает непосредственное влияние на способность первичной опухоли к метастазированию при этом типе почечно-клеточных карцином.
Связь аномального метилирования генов-супрессоров VHL, RASSF1, FHIT и CDH1 с прогнозом заболевания.
В образцах гистологически не измененной почечной паренхимы гиперметилирование генов-супрессоров, локализованных в области 3р (VHL, RASSF1 и FHIT), а также гена CDH1, кодирующего Е-кадгерин, не выявлено, что позволило рассматривать метилирование в образцах опухолевой ткани как аберрантное. В опухолях аберрантное метилирование VHL определено в 14.2% (18/127), RASSF1 – 52.8% (67/127), FHIT – 54.3% (69/127) и CDH1 – 41.7% (53/127) случаев, что совпадает с данными литературы (рис. 7).

Рис. 7. Определение метилирования генов-супрессоров МЧ-ПЦР.
М – маркер молекулярной массы (pUC19/MspI), ОК – отрицательный контроль амплификации, ПК – положительный контроль амплификации, К+ – внутренний контроль ПЦР (экзон 2 гена VHL), N и Т – нормальная и опухолевая ткани соответственно, 1-3 (А) и 1-4 (В) – анализируемые образцы.
А – МЧ-ПЦР гена FHIT, аберрантное метилирование выявлено в образцах опухолей 1 и 2; В – МЧ-ПЦР гена CDH1, аберрантное метилирование выявлено в образце опухоли 3.
Проведен сравнительный анализ частот метилирования в парных клинических группах в зависимости от стадии заболевания, степени дифференцировки первичной опухоли и метастазирования. Показана ассоциация метилирования CDH1 с прорастанием опухолью капсулы почки (p = 0.024, OR = 2.40 95% CI: 1.13-5.08) и наличием метастазов на момент постановки диагноза (p = 0.001, OR = 5.98 95% CI: 2.03-17.59). Продукт гена CDH1, Е-кадгерин, участвует в обеспечении контактного торможения пролиферации в эпителиальных тканях, в том числе, в эпителии почечных канальцев. Инактивацию гена CDH1 вследствие метилирования можно рассматривать как событие, способствующее инвазивному росту и метастазированию первичной опухоли. Также установлено, что метилирование RASSF1 чаще встречается в умеренно-, чем в высокодифференцированных первичных опухолях (p = 0.047, OR = 2.58, 95% CI: 1.04-6.35). Это дает возможность предположить, что аберрантное метилирование RASSF1 ассоциировано с прогрессией первичной опухоли и может считаться потенциальным неблагоприятным маркером на ранних стадиях РП.
Таким образом, при светлоклеточном раке почки множественные аллельные делеции генов-супрессоров, локализованных на коротком плече хромосомы 3, и метилирование гена CDH1 свидетельствуют о неблагоприятном влиянии на прогноз заболевания. В случае выявления потери гетерозиготности двух или трех исследуемых генов вместе с аберрантным метилированием промотора CDH1 можно сделать вывод о высоком риске метастазирования первичной опухоли, что должно быть учтено при назначении адьювантной иммунотерапии.
Определение мутаций и метилирования гена VHL, как предпосылка для таргетной терапии светлоклеточного рака почки.
В последние годы при лечении метастатического рака почки применяют таргетные препараты, представляющие собой ингибиторы определенных тирозинкиназ или факторов роста. Наиболее универсальным в классе таргетных препаратов является «Нексавар» (Сорафениб), который обладает активностью мультикиназного ингибитора (Алексеев Б.Я. и др., 2007).
Инактивация гена VHL встречается при наиболее распространенном гистологическом варианте рака почки – светлоклеточной карциноме. Показано, что более выраженный эффект применения таргетных препаратов достигается у пациентов с мутациями VHL в первичной опухоли, чем у пациентов без мутаций (Личиницер М.Р. и др., 2007). Мутации VHL были определены нами в 31.7% (39/123) светлоклеточного рака почки. Все выявленные мутации соматические, т.е. присутствовали только в опухолевой ткани и не обнаружены в соответствующих им образцах нормальной почечной паренхимы (рис. 8). Среди мутаций наиболее часто выявлялись делеции, протяженность которых варьировала от 1 до 42 п.н., а также выявлены инсерции и дупликации, однонуклеотидные замены, комплексные мутации. Метилирование промотора гена VHL определено также только в образцах светлоклеточных карцином и не выявлено в гистологически нормальной ткани. Частота аберрантного метилирования составила 14.6% (18/123) случаев светлоклеточного рака почки.
У больных светлоклеточным раком первой стадии соматические мутации в гене VHL выявлены в 35.4% случаев, потери гетерозиготности – в 28.2% информативных случаев и аберрантное метилирование – в 20.0% образцов. В целом, хотя бы одно из нарушений гена VHL обнаружено у 53.8% больных. Полученные данные указывают на раннюю инактивацию VHL в светлоклеточных карциномах, что согласуется с предположением о ключевой роли этого события в раннем канцерогенезе при светлоклеточном раке почки. По различным оценкам, около 40% спорадических светлоклеточных карцином развиваются без ранней инактивации VHL, что позволяет условно разделять опухоли почки на VHL-зависимые и VHL-независимые.

Рис. 8. Вверху – результат SSCP-анализа экзона 3 гена VHL.
1–6 – образцы; N и T - соответственно нормальная и опухолевая ткани;
ПЦР-продукт с аномальной подвижностью в образце 5Т.
Внизу - прямое секвенирование ПЦР-продукта 5Т с обратного праймера.
Таким образом, разработанная нами медицинская технология позволяет выделять VHL-зависимые и VHL-независимые группы пациентов со светлоклеточным раком почки и, соответственно, оптимизировать тактику и эффективность лечения. Показано, что пациенты с соматическими мутациями гена VHL обладают более выраженным ответом на терапию Сорафенибом, чем пациенты без мутаций, что демонстрирует целесообразность определения инактивации VHL при назначении подобных препаратов (Алексеев Б.Я., 2007).
Исследование полиморфных вариантов генов ABCB1, TGFBR1, IL10 и VDR в норме и при спорадическом раке почки.
Предрасположенность к РП может быть обусловлена аллельными вариантами ряда генов, участвующих в регуляции клеточного цикла, метаболизме ксенобиотиков и противоопухолевом иммунитете. Исходя из данных о полиморфных вариантах различных генов при РП, для настоящего исследования предрасположенности к РП были выбраны SNP в четырех генах – ABCB1 (ген множественной лекарственной устойчивости), TGFBR1 (ген, кодирующий рецептор первого типа трансформирующего фактора роста ), IL10 (ген, кодирующий интерлейкин 10) и VDR (ген рецептора витамина D3). Сравнивали частоты аллелей и генотипов в группах контроля и больных РП, а также в различных клинических группах у пациентов со злокачественными опухолями почек, в том числе в многофакторном анализе.
Анализ полиморфизмов генов ABCB1, TGFBR1, IL10 и VDR в лейкоцитах периферической крови и гистологически не измененной почечной паренхиме.
При анализе полиморфизмов генов ABCB1, TGFBR1, IL10 и VDR использовали геномную ДНК, выделенную из лейкоцитов периферической крови (группа контроля) и гистологически не измененной почечной паренхимы (группа РП). Наблюдаемые частоты генотипов в контрольной группе соответствовали закону Харди-Вайнберга. Достоверных различий в частотах аллелей (генотипов) между представителями обоих полов в контрольной группе и среди больных РП не выявлено.
Сравнительный анализ абсолютных частот аллелей, генотипов и частот встречаемости аллелей между исследуемыми группами.
Выявлены достоверные различия частот генотипов VDR у больных РП относительно контроля (p = 0,025). В то же время различий между группами по частотам аллелей и встречаемости аллелей этого гена не обнаружено. Однако в группе РП наблюдали тенденцию к увеличению частоты встречаемости аллеля Т и снижению – аллеля С (генотип С/С – почти в 1,85 раза; 6% против 11,3%). Чувствительность критерия Фишера при оценке различий частот встречаемости аллелей составила 0,89 (95% CI: 0,83 – 0,93) для аллеля Т и 0,50 (95% CI: 0,42 – 0,59) - для аллеля С. Следовательно, объем выборок мог быть недостаточным для выявления снижения аллеля С.
Аллель Т ассоциирован со сниженным уровнем активного витамина D3 в сыворотке крови больных РП и считается фактором предрасположенности к РП в некоторых популяциях. Возможно, снижение частоты протективного аллеля С и/или генотипа С/С связано с предрасположенностью к развитию РП в исследуемой популяции. Данные, подтверждающие протективную роль аллеля С, при наличии фактора риска – онкологического заболевания у родственников, получены также и для популяций центральной и восточной Европы (Karami S. et al., 2008).
При сравнительном анализе других исследуемых локусов различий в группах контроля и РП не выявлено.
Определение влияния полиморфных вариантов исследуемых генов на клинические особенности заболевания и характеристики первичной опухоли.
Для определения возможного влияния полиморфных вариантов исследуемых генов на клинические особенности заболевания и характеристики первичной опухоли проведен сравнительный анализ частот аллелей (генотипов) и частот встречаемости аллелей ABCB1, TGFBR1, IL10 и VDR в различных клинических группах пациентов. Парные клинические группы были сформированы по следующим признакам: начальным (I и II) и поздним (III и IV) стадиям заболевания, по степени дифференцировки первичной опухоли – группы GI-II и GIII-IV, по наличию (любое положительное N и/или М) и отсутствию (TXN-M0) метастазов на момент постановки диагноза.
Показано, что частота аллеля А гена TGFBR1 снижена у пациентов с регионарными и/или отдаленными метастазами: p = 0,012, OR = 0,80 (95% CI: 0,72 – 0,89). Также достоверно уменьшена в группе больных с метастазами встречаемость этого аллеля в составе гомо- и гетерозиготных носителей: p = 0,016, OR = 0,81 (95% CI: 0,70 – 0,93). Полученные данные не вполне согласуются с обнаруженной ранее ассоциацией аллеля А с повышенным риском РП относительно контроля (Chen T. et al., 2004). Это может быть обусловлено, в частности, межпопуляционными различиями в частотах аллелей TGFBR1.
Выявление сочетаний аллелей исследуемых генов, влияющих на риск развития спорадического рака почки или прогрессию опухоли.
С целью выявления сочетаний аллелей исследуемых генов, которые могут влиять на риск развития спорадического РП или прогрессию опухоли, проведен многофакторный регрессионный анализ встречаемости аллелей ABCB1, TGFBR1, IL10 и VDR. Рассматривали комбинации из 2–4 полиморфизмов в группах контроля и РП, а также в парных клинических группах. Ассоциации сочетаний аллелей с риском развития РП и прогрессией первичной опухоли не выявлены.
Таким образом, в исследовании полиморфных вариантов генов ABCB1, TGFBR1, IL10 и VDR в норме и при спорадическом РП показаны достоверные различия в частотах генотипов полиморфизма Taq1 гена VDR между группами контроля и РП, а также снижение частоты аллеля А полиморфизма int7G24A гена TGFBR1 у больных с метастазами на момент постановки диагноза. Результаты проведенного исследования могут способствовать формированию системы прогностических маркеров для спорадического РП.
Исследование молекулярной патологии при раке предстательной железы и разработка ДНК-диагностических протоколов.
Исследование потери гетерозиготности и микросателлитной нестабильности хромосомных районов 13q14 и 16q23 при раке предстательной железы.
Гомозиготные и гетерозиготные делеции являются одними их самых частых генетических патологий эпителиальных опухолей, в том числе, и рака предстательной железы, и для их детекции широко применяется микросателлитный анализ потери гетерозиготности и микросателлитной нестабильности. Для оценки частоты генетических нарушений в опухолевом эпителии были выбраны хромосомные районы 13q14 и 16q23, как наиболее часто повреждаемые при РПЖ. Делеции 13q14 характерны для ранних стадий РПЖ, а потери хромосомного района 16q23 чаще встречаются на более поздних стадиях.
Высокая гетерогенность и мультифокальная природа РПЖ наряду с небольшим размером железы составляют серьезную проблему для исследователей. В настоящей работе трудности в получении гомогенного материала опухоли в достаточном количестве для молекулярного анализа решены с помощью лазерной микродиссекции ткани.
По полученным нами данным, 46 образцов опухолевого эпителия (91%) имели ПГ/МН, по крайней мере, по одному из маркеров. Частоты аллельных нарушений в эпителии составили: 51% для маркера D16S534, 57% для D16S422 (72% для локуса 16q23 по совокупности двух маркеров) и 37% для локуса 13q14. В эпителиальном компоненте ПИН был обнаружен меньший процент молекулярных перестроек (от 24 до 28%) (табл. 4). При ДГПЖ структурных перестроек не выявлено.
Таблица 4. Частота аллельных нарушений у пациентов с аденокарциномой ПЖ, ПИН и ДГПЖ.
| Маркер | Частота ПГ/МН в аденокарциноме | Частота ПГ/МН в ПИН | Частота ПГ/МН в ДГПЖ |
| D16S534 | 26/51 (51%) | 7/25 (28%) | 0/24 |
| D16S422 | 29/51 (57%) | 6/25 (24%) | 0/24 |
| RB1.20 | 19/51 (37%) | 7/25 (28%) | 0/24 |
Для сравнения частот ПГ/МН изученных локусов с прогрессией РПЖ были выбраны следующие клинические критерии: степень дифференцировки опухоли по классификации Глисона, стадия процесса и наличие метастазов в регионарных лимфоузлах. Обнаружены статистически достоверные ассоциации аллельных потерь в эпителии локуса 16q23 (маркер D16S534) со степенью дифференцировки опухоли, стадией злокачественного процесса и наличием метастазов в регионарных лимфоузлах. Положительные ассоциации со стадией заболевания показаны также для микросателлитов RB20int и D16S422 (табл. 5).
Таблица 5. Ассоциации аллельных нарушений в опухолевом эпителии с клиническими параметрами.
| Маркер | Корреляции | ||
| степень дифференцировки по классификации Глисона, p | метастазирование, р | стадия РПЖ р | |
| D16S534 | 0.01 | 0.04 | 0.02 |
| D16S422 | НД | НД | 0.04 |
| RB1.20 | НД | НД | 0.02 |
Примечание: p - вероятность, НД – недостоверное различие (р>0,05).
Использование системы прогностических маркеров ПГ/МН как дополнительного метода к гистологическому исследованию может помочь в диагностике и прогнозе РПЖ.
Таким образом, разработанная нами медицинская ДНК-технология направлена на определение делеций хромосомных районов 13q14 и 16q23 в биопсийных образцах больных с заболеваниями предстательной железы с целью выявления пациентов с начальными стадиями РПЖ, а также для прогноза гистологически подтвержденного РПЖ.
Исследование экспрессии химерного гена TMPRSS2/EGR4 при раке предстательной железы.
Особенностью канцерогенеза РПЖ являются образование химерных онкогенов, приводящих к активации факторов транскрипции семейства ETS. Исследования последних лет привели к открытию химерных генов при РПЖ, образованных слиянием 5’-нетраслируемой области гена TMPRSS2 и генов семейства транскрипционных факторов ETS, таких как ERG4 (21q22.1), ETV1(7p21.2) и ETV4 (17q21). Конечным результатом всех перестроек ETS является аномальная гиперэкспрессия измененных вариантов транскрипционных факторов (Winnes M. et al., 2007). Активация факторов транскрипции семейства ETS вследствие хромосомных перестроек осуществляется при помощи андрогеночувствительных промоторных и энхансерных элементов и является особенностью канцерогенеза при РПЖ. Идентификация андрогеночувствительных и андрогенрезистентных генов-участников химерных онкогенов может помочь в определении мишеней для антигормональной терапии РПЖ.
В ткани ДГПЖ, взятой в качестве контрольных образцов, химерных транскриптов обнаружено не было (0/10), что согласуется с результатами работы Wang J. et al., 2006. Частота химерного транскрипта TMPRSS2/ERG4 в ткани РПЖ составила 50% (32/63). Подлинность химерного гена TMPRSS2/ERG4 подтверждена секвенированием исследуемого фрагмента кДНК (рис. 9).

Рис. 9. Результаты секвенирования химерного гена TMRPSS2/ERG4.
Для анализа клинических ассоциаций перестройки TMPRSS2/ERG4 с прогрессией РПЖ были выбраны следующие критерии: степень дифференцировки опухоли по классификации Глисона, стадия процесса и наличие гормонального лечения перед простатэктомией. При делении пациентов на 2 группы, проходящих и не проходящих гормональное лечение, частота перестройки у пациентов без гормонального лечения составила 56% (25/45), а после него – 17% (2/12), что статистически достоверно различается (p = 0,023). К сожалению, в представленной выборке не было гормонально независимых опухолей для оценки частоты экспрессии TMPRSS2/ERG4 в андрогенрезистентных опухолевых клетках. Таким образом, экспрессия химерного гена TMPRSS2/ERG4 может служить маркером оценки ответа опухолевых клеток на гормональную терапию и андрогеночувствительности опухолевых клеток.
Также нами обнаружено достоверное различие в группах пациентов с РПЖ с поражением одной либо обеих долей ПЖ, т.е. между стадиями Т2а и Т2b. В группе пациентов с локализацией РПЖ в одной доле химерных перестроек не обнаружено (0/10), у пациентов с поражением обеих долей – 48% (14/27; p = 0,005). В целом, частота химерного гена увеличивается с прогрессированием заболевания: частота TMPRSS2/ERG4 на стадии II составила 38% (14/37), на стадии III – 59% (13/22) и на стадии IV – 71% (5/7) (табл. 6).
Достоверных ассоциаций между наличием химерного транскрипта и степенью дифференцировки опухоли по Глисону обнаружено не было.
Табл. 6. Распределение частот химерной перестройки TMPRSS2/ERG4 на различных стадиях РПЖ.
| Стадия | Кол-во пациентов | Частота TMPRSS2/ERG4, % |
| ДГПЖ | 15 | 0 |
| I | 0 | - |
| II | 37 | 38 |
| III | 22 | 59 |
| IV | 7 | 71 |
Таким образом, было показано, что образование химерного гена TMPRSS2/ERG4 является частым опухолеспецифическим событием РПЖ. Экспрессия данного гена коррелирует с более агрессивными стадиями заболевания и может служить молекулярным маркером РПЖ, а также маркером оценки ответа опухолевых клеток на гормональную терапию и андрогенчувствительности опухолевых клеток. Преимуществом данного метода является возможность работать с образцами опухоли без выполнения микродиссекции, несмотря на выраженную гетерогенность РПЖ. Поиск других способов активации онкогенов и выявление возможных перестроек на стадии гормонрезистентного РПЖ позволит объяснить механизмы резистентности опухолевых клеток к гормональной терапии и выработать новые стратегии лечения поздних стадий РПЖ.
Клинически значимые маркеры метилирования при раке предстательной железы.
Был проведен анализ метилирования промоторных областей генов Р16 (ген-супрессор опухолевого роста), HIC1 (транскрипционный фактор), N33 (ген-супрессор) и GSTP1 (глутатион-S-трансфераза) в образцах ткани аденокарциномы ПЖ, ПИН разной степени, ДГПЖ и нормальной ПЖ, а также в смежных соединительнотканных образцах, расположенных рядом с фокусами аденокарциномы, ПИН высокой степени и ДГПЖ. Высокие частоты метилирования были найдены для аденокарциномы: HIC1 – 8/9 (89%); Р16 – 7/9 (78%); GSTP1 – 6/6 (100%); N33 – 2/6 (33%). Для ПИН высокой степени показаны следующие частоты: HIC1 – 5/7 (71%); Р16 – 4/7 (57%); GSTP1 – 5/7 (71%); N33 – 0/7. В близлежащей строме практически во всех анализируемых образцах показано наличие метилирования, кроме гена N33: HIC1 – 4/4; Р16 – 4/4; GSTP1 – 2/4; N33 – 0/4. В гиперпластически измененных и нормальных железистых структурах, в близлежащей строме метилирования не было обнаружено, за исключением гиперплазированных ацинусов на гистологических препаратах пациентов с метастазами. Для генов N33 и GSTP1 было показано статистически достоверное различие между группами пациентов с ПИН и с аденокарциномами.
Для исследования возможной неинвазивной диагностики проведен анализ метилирования генов Р16, CD44 (участвует в клеточной адгезии), CDH1, N33 и GSTP1 в 64 образцах плазмы крови пациентов с РПЖ и пациентов с ДГПЖ, чтобы оценить диагностический потенциал выбранных эпигенетических маркеров. Достоверные различия в плазме между пациентами с предраковым состоянием и РПЖ обнаружены только для гена GSTP1, хотя чувствительность данного маркера составляет только 28%. Действительно, по данным литературы, в сыворотке/плазме крови прогностическим маркером пока можно назвать только метилирование GSTP1, которое выявляется в 13 – 72% случаев РПЖ.
Таким образом, для генов N33 и GSTP1 было показано статистически достоверное различие между группами пациентов с ПИН и с аденокарциномами. Использование системы прогностических маркеров метилирования, в частности генов N33 и GSTP1, как дополнительного метода к гистологическому исследованию может помочь в диагностике и прогнозировании РПЖ.
Разработка системы эпигенетических маркеров для ранней диагностики рака шейки матки.
Одним из самых распространенных механизмов инактивация генов-супрессоров опухолевого роста является аномальное метилирование CpG-островков промоторных и регуляторных областей этих генов. Идентификация гиперметилирования различных генов может служить молекулярным маркером ранней диагностики, мониторинга и клинического прогноза опухолей.
При фоновых изменениях шейки матки метилирование генов Р16, MLH1 (участвует в репарации неспаренных участков ДНК) и N33 не менялось по сравнению с образцами, полученными от женщин без гинекологической патологии. Высокая частота гиперметилирования определена для генов Р16 (58%), MLH1 (51%) и N33 (27%) при цервикальной интраэпителиальной неоплазии II – III степени (CIN II-III) (рис. 10).

1р 1н 2р 2н 3р 3н 4р 4н м
Рис. 10. Пример определения аномального метилирования генов Р16 и N33 при дисплазии шейки матки.
р - ДНК после гидролиза HpaII, н – ДНК негидролизованная Hpa II, м – маркер молекулярной массы;
дорожки 1 и 3 – наличие аномального метилирования генов N33 и Р16, соответственно; дорожки 2 и 4 – отсутствие аномального метилирования; XL3.2 – внутренний контроль гидролиза метилчувствительной рестриктазой и ПЦР.
В образцах ткани шейки матки, смежных с дисплазией, но морфологически не отличающихся от нормы, выявлены частоты метилирования, близкие к таковым в диспластических образцах (Р16 – 50%, MLH1 – 36%, N33 – 10%). Достоверных различий между частотами метилирования этих генов при CIN II-III и в морфологически неизмененной ткани не обнаружено. Высокий уровень метилирования в морфологически неизмененной ткани подтверждает данные, что метилирование является наиболее ранним маркером начавшихся злокачественных процессов в клетке, хотя ее морфология еще не изменилась.
Наибольшая чувствительность определена для гена Р16 – 54%, а наибольшая специфичность – для гена N33 – 100%. Панель из трех генов имеет чувствительность и специфичность до 85%, т.е. наличие гиперметилирования по крайней мере одного из трех генов обеспечивает 85% чувствительность и специфичность детекции СIN2/СIN3 в исследуемом материале шейки матки.
Таким образом, определение гиперметилирования генов Р16, MLH1 и N33 может использоваться для молекулярной диагностики злокачественного потенциала цервикальных интраэпителиальных неоплазий II и III степени. Полученные результаты позволяют считать, что исследование генов-супрессоров вместе с цитологическим исследованием и тестированием вируса папилломы человека может служить основой для скрининга тяжелых дисплазий при мониторинге женщин с риском развития рака шейки матки.
Исследование молекулярной патологии при увеальной меланоме и разработка ДНК-диагностических протоколов.
Исследование аллельных делеций в хромосоме 3 при увеальной меланоме.
Дифференциальной диагностике УМ способствует обнаружение потери копии хромосомы 3, так как это нарушение является специфическим, не характерным для другой онкопатологии. Оптимальным методом в данном случае является микросателлитный анализ, выявляющий аллельный дисбаланс в опухоли.
Потеря гетерозиготности по маркерам хромосомы 3 определена в 51 (48%) из 107 исследованных УМ, из них 48 (45%) имели ПГ по всем информативным локусам хромосомы 3 (рис. 11).

Рис. 11. Оценка состояния некоторых микросателлитных маркеров в различных образцах УМ.
н - норма, о – опухоль; ПГ-потеря гетерозиготности по указанному маркеру, гет – маркер гетерозиготен (потери гетерозиготности нет), гом – маркер гомозиготен (не информативен).
Клиническая чувствительность метода составляет 45-55%, так как моносомия 3 присутствует в 45-55% увеальных меланом. Клиническая специфичность метода чрезвычайно высока в связи с тем, что, в отличие от множества других опухолей, для которых характерна потеря только короткого плеча хромосомы 3 или структурные нарушения 3р, наиболее распространенным нарушением в увеальных меланомах считается моносомия 3.
Аналитическая чувствительность системы (наличие как минимум одного информативного маркера на каждом плече хромосомы 3) составляет 99,5%. Аналитическая специфичность оценивалась при использовании образцов условно-нормальной хориоидеи, где ПГ выявлена не была.
Таким образом, разработанная методика предполагает исследование потери гетерозиготности в ряде локусов короткого и длинного плеча хромосомы 3 с целью выявления потери одной копии хромосомы 3 (моносомия 3), характерной для меланом увеального тракта.
Исследование потери гетерозиготности для оценки прогрессии первичной опухоли при увеальной меланоме.
Выявление в опухолевых клетках потери одной копии хромосомы 3 (моносомия 3), делеций локусов 3р25, 3(p14.2-p13) и 3(q24-q26), изодисомии 3 (результат потери одной из хромосом и дупликации оставшейся) является наиболее характерными нарушениями в УМ и показало наибольшую прогностическую точность по отношению к развитию метастазов (Harbour J.W., 2007). Также отмечено, что наличие перестроек в 1p, встречающееся примерно у трети пациентов с УМ, является признаком опухолевой прогрессии.
Информативность исследуемых маркеров составила соответственно D1S438 - 0,570, D1S3669 – 0,731, D1S407 – 0,769, D1S1635 – 0,600, D1S2145 – 0,778, D1S243 – 0,817. Моносомия хромосомы 3 выявила ассоциацию (р < 0,0001) с наличием в опухоли эпителиоидных клеток (смешанноклеточные и эпителиоидноклеточные УМ), а также с локализацией меланомы в цилиарном теле (р = 0,001), что играет важную роль в развитии метастазов.
ПГ по маркерам, локализованным на коротком плече хромосомы 1, определена в 32 УМ (29,9%). В 25 (23,4%) образцах ПГ была определена для всех информативных маркеров 1р36. Наибольшие частоты аллельных потерь определены для маркеров, расположенных в наиболее дистальных из изучаемых локусов (D1S243 (1р36.33) и D1S2145 (1р36.31)).
С помощью критерия Манна-Уитни была выявлена ассоциация аллельных потерь в 1р36 с размером опухоли (р = 0,012). Статистически значимая ассоциация была обнаружена между экстрасклеральной инвазией меланомы и ПГ по всем информативным маркерам 1p36 (р = 0,012). Экстрасклеральная инвазия считается характерным признаком агрессивности УМ, и ассоциация ее с нарушениями в хромосоме 1 свидетельствует о связи нарушений в 1р с опухолевой прогрессией.
Аналитическая чувствительность системы (наличие как минимум одного информативного маркера на каждом плече хромосомы 3) составляет 99,5% для маркеров хромосомы 3 и 99,9% для системы маркеров 1р36. Аналитическая специфичность оценивалась при использовании образцов условно-нормальной хориоидеи, где ПГ по указанным маркерам выявлена не была.
Таким образом, разработанная нами методика, основанная на исследовании аллельных делеций в хромосомах 3 и 1р36, представляет собой молекулярно-генетическое исследование для выявления молекулярных маркеров прогрессии УМ в дополнение к применяемым в настоящее время диагностическим методам.
Молекулярно-генетический анализ клональной внутриопухолевой гетерогенности в колоректальных карциномах.
По данным морфологического анализа, 9 из 11 аденокарцином толстой кишки имели различную степень дифференцировки в разных участках. Опухолевые железистые комплексы в каждом из четырех сегментов одной и той же опухоли отличались по степени дифференцировки: в 8 случаях наблюдались фрагменты с умеренной и высокой дифференцировкой, в одном – с умеренной и низкой. Кроме того, один и тот же фрагмент опухоли зачастую содержал атипичные железистые комплексы как умеренной, так и высокой степени дифференцировки.
В результате микросателлитного анализа полиморфных маркеров в локусах расположения генов-супрессоров Р16, Р15, Р19 (9p21), RB1 (регулирует переход G1S фазы клеточного цикла) (13p14), PTEN (10q23), P53 (17p13) в девяти из 11 образцов колоректального рака удалось определить аллельные делеции (81%). В семи случаях найдены делеции одного или более маркеров во всех четырех сегментах. В четырех опухолях делеции выявлены не во всех сегментах, что указывает на внутриопухолевую гетерогенность.
МН считали подтвержденной при появлении аллелей, длина которых отличалась от нормальных, определяемых в ДНК лимфоцитов периферической крови. К проявлению нестабильности отнесено три случая, в которых нестабильны два или более маркеров (27%).
Изучение разных сегментов одной опухоли помимо внутриопухолевой гетерогенности позволяет определить очередность появления и распространения молекулярно-генетических повреждений при возникновении колоректального рака. Если повреждение присутствует во всех сегментах опухоли, то оно имеет более раннее происхождение. Повреждение первоначально возникает в материнском клоне, а позже к нему присоединяются другие геномные нарушения, давая начало новым субклонам. В 5 случаях делеции локуса 9p21 (гены Р16, Р15, Р19) найдены во всех сегментах опухоли, так же как и аллельная потеря гена RB1, что позволяет сделать вывод о первичности повреждения регуляторного пути Р16-RB1-циклин D в генезе опухолей у этих больных и о более позднем присоединении делеций гена PTEN, которые выявлены лишь в части сегментов. Во всех сегментах других опухолей (2 случая) определена потеря гена Р53, что можно рассматривать как более раннее событие, а делеции в других локусах – как более поздние события в генезе опухоли. При этом не было выявлено опухолей, содержащих делеции 9p21 и 17p13 (Р53) одновременно. Полученные результаты позволяют считать присоединение МН вторичным, более поздним событием. В одном из образцов присутствует как аллельная делеция локуса 13q14 (RB1), так и высокая степень МН, при этом нестабильность имеет более позднее происхождение, так как выявлена не во всех сегментах. В другом случае делеция гена PTEN является ранним событием канцерогенеза.
Активирующие мутации гена K-RAS (протоонкоген) (кодоны 12, 13) во всех сегментах опухоли выявлены у 4 из 11 больных, что подтверждает их более раннее появление.
Таким образом, при молекулярно-генетическом анализе клональной внутриопухолевой гетерогенности в колоректальных карциномах подтверждена гетерогенность 9 из 11 опухолей (81%) не только молекулярными методами, но и морфологическим исследованием. Исследуя внутриопухолевую гетерогенность, можно определить очередность молекулярно-генетических событий, происходящих при развитии колоректального рака, проследить его механизм и связать молекулярные повреждения с клиническим поведением опухоли – агрессивностью, способностью к инвазии, метастатическим потенциалом, ответом на лекарственную терапию и т.д.
Выводы
- Биологические и молекулярно-генетические маркеры сердечно-сосудистых и онкологических заболеваний или их сочетание позволяют определить начальные стадии, прогноз развития и подобрать оптимальную тактику лечения этих заболеваний.
- Высокий уровень экспрессии ингибитора активатора плазминогена 1 типа в моноцитах периферической крови больных ишемической болезнью сердца, независимо от уровня активатора плазминогена урокиназного типа, является показателем нестабильности атеросклеротических бляшек и маркером развития острого коронарного синдрома.
- Установлено, что для больных как со стабильным течением ишемической болезни сердца, так и с острым коронарным синдромом характерно увеличение концентрации С-реактивного белка и снижение концентрации адипонектина. Выявленные взаимосвязи между показателем метаболических нарушений - адипонектином и маркером воспаления С-реактивным белком позволяют использовать этот гормон для дополнительной оценки степени тяжести воспалительного процесса у больных со стабильным течением ишемической болезни сердца, особенно при наличии метаболического синдрома.
- Показано, что потеря гетерозиготности более чем одного из генов-супрессоров (VHL, RASSF1, FHIT) ассоциирована с наличием метастазов (p = 0.036), а метилирование гена CDH1 ассоциировано с прорастанием опухолью капсулы почки (p = 0.024) и наличием метастазов на момент постановки диагноза (p = 0.001) у больных со светлоклеточным раком почки. В случае обнаружения мутаций и метилирования гена VHL целесообразно назначение таргетных препаратов (Сорафениб).
- При спорадическом раке почки показано достоверное снижение частоты протективного аллеля С и генотипа С/С полиморфизма Taq1 гена VDR (р<0,025), а также снижение частоты аллеля А полиморфизма int7G24A гена TGFBR1 (p<0,012) у больных с метастазами на момент постановки диагноза.
- Установлено, что потеря гетерозиготности локуса 13q14 ассоциирована с более ранними стадиями рака предстательной железы, а аллельные потери локуса 16q23 достоверно коррелируют со степенью дифференцировки опухоли, стадией злокачественного процесса и наличием метастазов в регионарных лимфоузлах. Для аномального метилирования генов N33 и GSTP1 показано статистически достоверное различие между группами пациентов с простатической интраэпителиальной неоплазией и с аденокарциномами предстательной железы.
- Установлено, что образование химерного гена TMPRSS2/ERG4 является частым опухолеспецифическим событием рака предстательной железы, а его экспрессия коррелирует с более агрессивными стадиями заболевания и может служить молекулярным маркером рака предстательной железы, оценки ответа опухолевых клеток на гормональную терапию и андрогенчувствительности опухолевых клеток.
- Исследование маркеров метилирования позволило разработать систему для ранней диагностики рака шейки матки; панель из трех генов (Р16, MLH1 и N33) имеет чувствительность и специфичность равную 85%.
- Разработана методика выявления аллельных делеций в хромосоме 3, являющихся специфическим молекулярным маркером увеальной меланомы; моносомия 3 и потеря гетерозиготности хромосомы 1р36 коррелируют с агрессивным течением и высоким риском метастазирования первичной опухоли.
- Исследование разных сегментов одной опухоли, помимо внутриопухолевой гетерогенности, позволяет определить очередность появления и распространения молекулярно-генетических повреждений в генезе колоректального рака; мутации гена K-RAS и повреждение регуляторного пути Р16-RB1-циклин D в генезе опухоли происходят раньше, чем развитие микросателлитной нестабильности и делеций гена PTEN.
Практические рекомендации
- При обследовании больных ишемической болезнью сердца целесообразно определять уровень экспрессии PAI-1 в моноцитах периферической крови, т.к. данный биомаркер является показателем нестабильности атеросклеротических бляшек и маркером развития острого коронарного синдрома.
- Выявленные взаимосвязи между показателем метаболических нарушений - адипонектином и маркером воспаления СРБ позволяют использовать этот гормон для дополнительной оценки степени тяжести воспалительного процесса у больных со стабильным течением ишемической болезни сердца, особенно при наличии метаболического синдрома.
- Исследование аллельных делеций генов-супрессоров опухолевого роста, расположенных в коротком плече хромосомы 3, и метилирования гена CDH1, представляет собой метод оценки прогрессии и способности к метастазированию первичной опухоли при светлоклеточном раке почки.
- При светлоклеточном раке почки разработанная система молекулярно-генетических маркеров позволяет оптимизировать таргетную терапию. Для пациентов, у которых имеются мутации и/или метилирование гена VHL, терапия таргетным препаратом Сорафениб, обладающим активностью мультикиназного ингибитора, представляется оптимальной.
- Разработанная система молекулярных маркеров для определения потери гетерозиготности и микросателлитной нестабильности хромосомных районов 13q14 и 16q23 в биопсийных образцах больных с заболеваниями предстательной железы позволяет выявлять пациентов с начальными стадиями РПЖ, а также прогнозировать развитие гистологически подтвержденного РПЖ.
- При раке предстательной железы разработанная методика позволяет определять наличие химерного онкогена TMPRSS2/EGR4 в ткани опухоли. Поскольку он является маркером неблагоприятного прогноза и андрогенчувствительности опухоли, появляется возможность оптимизировать тактику и эффективность лечения рака предстательной железы.
- Использование системы прогностических маркеров метилирования, в частности генов N33 и GSTP1, как дополнительного метода к гистологическому исследованию, может помочь в диагностике и прогнозировании рака предстательной железы.
- Молекулярные маркеры метилирования при раке шейки матки позволяют выявить начальные стадии злокачественного процесса еще до того, как обнаруживаются морфологические изменения. Это дает возможность начать терапию заболевания на ранних сроках и избежать высокодозной химиотерапии, тяжелой инвалидизации и летального исхода.
- Разработанная медицинская технология, основанная на исследовании потери гетерозиготности в хромосоме 3, представляет собой молекулярно-генетическое исследование для диагностики увеальной меланомы в дополнение к применяемым в настоящее время диагностическим методам.
- Исследование структурных и численных нарушений хромосомы 3 и 1р с помощью микросателлитного анализа может быть использовано вместе с другими необходимыми тестами при верификации диагноза «увеальная меланома» и для оценки прогрессии опухоли. Разработки легли в основу новой медицинской технологии.
Список работ, опубликованных по теме диссертации
- Пальцева Е.М. Уязвимая атеросклеротическая бляшка: факторы, обусловливающие ее нестабильность. // Мол. мед. – 2005. - № 1. – С. 17-22.
- Paltseva E.M., Lysenko A.I., Belov Iu.V., Ivanov A.A., Paltsev M.A. Peculiarities of vulnerable plaque formation. // Virch. Arch. – 2005. – Vol. 447, # 2. – P. 464.
- Gusev D., Paltseva E. Serologic infection and inflammatory markers in coronary artery disease. // Atherosclerosis supplements. – 2006. – Vol. 7, issue 3. – P. 287.
- Kekeeva T.V., Popova O.P., Zavalishina L.E., Paltseva E.M., Andreeva Y.Y., Zaletaev D.V., Nemtsova M.V. Molecular genetic alterations in tumor epithelium and tumor-associated stromal cells of prostate cancer. // Eur. J. Hum. Genet. - 2007. - Vol. 15, Suppl. 1. - P. 168.
- Mikhaylenko D., Kurynin R., Popov A., Karyakin O., Paltseva E., Enikeev M., Alyaev Y., Nemtsova M., Zaletayev D. Inactivation of the VHL gene in sporadic clear cell renal cancer. // Eur. J. Hum. Genet. – 2007. – Vol. 15, suppl. 1. - P.173.
- Mikhaylenko D.S., Kurynin R.V., Paltseva E.M., Popov A.M., Zaletayev D.V. Molecular genetic aberrations of the genes VHL, RASSF1, FHIT in patients with renal cancer. // Conference for young scientists, PhD students and students on molecular biology and genetics (Kiev, Ukraine). Abstract book. – 2007. - P. 177.
- Kekeeva T.V., Andreeva Y.Y., Frank G. A., Paltseva E.M., Zaletaev D.V., Nemtsova M.V. TMPRSS2/ERG4 fusion gene is a novel hormone refractory marker of prostate cancer. // Eur. J. Hum. Genet. – 2008. - Vol. 16. - P. 233.
- Mikhaylenko D.S., Popov A.M., Paltseva E.M., Kurynin R.V., Zaletayev D.V. Analysis of the molecular-genetic alterations in the genes VHL, RASSF1, and FHIT in clear cell renal carcinomas. // Eur. J. Hum. Genet. – 2008. - Vol. 16, suppl. - P. 2235.
- Paltseva E., Rodina A., Andreev D., Ponomar E., Gusev D., Severin S., Syrkin A. Hypoadiponectinemia and increased C-reactive protein related to the progression of acute coronary syndrome. // J. Clin. Lipidology. – 2008. – Vol. 2, # 5S. – P. S59-S60.
- Аляев Ю.Г., Курынин Р.В., Пальцева Е.М., Михайленко Д.С., Залетаев Д.В. Молекулярные маркеры в диагностике и лечении рака почки. // Мол. мед. – 2008. - № 4. – С. 24-28.
- Залетаев Д.В., Немцова М.В., Стрельников В.В., Бабенко О.В., Пальцева Е.М., Землякова В.В., Кузнецова Е.Б., Кекеева Т.В., Михайленко Д.С., Манохина И.К. Эпигенетическая регуляция экспрессии генов в процессах канцерогенеза. // Мол. мед. – 2008. - № 4. – С. 46-51.
- Кекеева Т.В., Андреева Ю.Ю., Франк Г.А., Пальцева Е.М., Попова О.П., Залетаев Д.В., Немцова М.В. Экспрессия химерного гена TMPRSS2/ERG4 при раке предстательной железы. // Мол. мед. – 2008. - № 5. – С. 29-34.
- Стрельников В.В., Землякова В.В., Белецкий И.П., Грановский И.Э., Пальцева Е.М., Залетаев Д.В. ДНК-микрочипы в диагностике онкологических заболеваний. // Мол. мед. – 2008. - № 5. – С.4-11.
- Немцова М.В., Пальцева Е.М., Бабаян А.Ю., Михайленко Д.С., Бабенко О.В., Самофалова О.Ю., Царьков П.В., Залетаев Д.В. Молекулярно-генетический анализ клональной внутриопухолевой гетерогенности в колоректальных карциномах. // Мол. биол. – 2008. – Т. 42, № 6. – С. 1040-1047.
- Михайленко Д.С., Попов А.М., Карякин О.Б., Курынин Р.В., Аляев Ю.Г., Пальцева Е.М, Любченко Л.Н., Немцова М.В., Залетаев Д.В. Полиморфные варианты генов ABCB1, TGFBR1, IL10 и VDR в норме и при спорадическом раке почки. // Мол. мед. – 2009. - № 2. – С. 39-43.
- Гусев Д.Е., Пальцева Е.М., Потиевский Б.Г., Родина А.В., Никифорова Е.В.. Пономарь Е.Г., Раичевич Н., Сыркин А.Л. Молекулы адгезии sVCAM-1 и sICAM-1 при различных формах ишемической болезни сердца. // Кардиология и сердечно-сосудистая хирургия. – 2009. - № 2.
- Валитова Р.М., Сыркин А.Л., Гусев Д.Е., Пальцева Е.М. Исследование С-реактивного белка и адипонектина у больных с различными формами ишемической болезни сердца. // Тезисы итоговой научной студенческой конференции с международным участием «Татьянин день», посвященной 250-летию ММА им. И.М. Сеченова. Москва, 2009. – С. 38-39.
- Rodina A.V., Paltseva E.M., Andreev D.A., Ponomar E.G., Gusev D.E., Severin S.E., Syrkin A.L. Distribution of adiponectin in patients with coronary artery disease and its association with systemic inflammation, obesity and diabetes type 2. // 6th Metabolic Syndrome, Type II Diabetes and Atherosclerosis congress. Abstract book. – Berlin, 2009. – P. 74.
- Пальцева Е.М., Родина А.В., Андреев Д.А., Ермаков Н.В., Пономарь Е.Г., Гусев Д.Е., Северин С.Е., Сыркин А.Л. Взаимосвязь уровней адипонектина и С-реактивного белка в крови при стабильном течении ишемической болезни сердца и остром коронарном синдроме. // Мол. мед. – 2009. - № 4. – С. 33-37.
- Пальцева Е.М., Константинова С.В., Северин С.Е. Новые биомаркеры: адипонектин в современной диагностике сердечно-сосудистых заболеваний. // Кардиология. – 2009. - № 10. – С. 65-74.
- Пальцева Е.М., Родина А.В., Попова О.Н., Андреев Д.А., Гусев Д.Е., Северин С.Е., Сыркин А.Л. Повышение уровня ингибитора активатора плазминогена 1 типа в моноцитах периферической крови больных ишемической болезнью сердца отражает степень тяжести заболевания. // VI международная конференция «Молекулярная медицина и биобезопасность». Научная программа, тезисы. – Москва, 2009. – С. 175-177.
- Пальцева Е.М., Родина А.В., Константинова С.В., Ермаков Н.В., Андреев Д.А., Сыркин А.Л., Северин С.Е. Прогностические, диагностические и терапевтические перспективы применения адипонектина в качестве биомаркера при сердечно-сосудистых заболеваниях. // Российский физиологический журнал. – 2009. – Т.95, № 10. – С. 1024-1040.
- Пальцева Е.М., Кекеева Т.В., Залетаев Д.В., Немцова М.В. Системы молекулярных маркеров в диагностике тяжелых дисплазий шейки матки. В: Системы генетических и эпигенетических маркеров в диагностике онкологических заболеваний. Под ред. М.А. Пальцева и Д.В. Залетаева. // М.: ОАО «Издательство «Медицина», 2009. – С. 215-224.
- Пальцева Е. М., Родина А. В., Андреев Д. А., Попова О. Н., Гусев Д. Е., Северин С. Е., Сыркин А. Л. Активатор плазминогена урокиназного типа и его ингибитор 1-го типа в диагностике развития осложнений ишемической болезни сердца. // Клин. лаб. диагностика. – 2010. - № 6. – С. 51-56.
- Пальцева Е.М., Родина А.В., Северин С.Е. Возможность применения адипонектина в качестве биомаркера для клинической диагностики. В: Введение в молекулярную диагностику. Под ред. М.А. Пальцева. // М.: «Медицина», 2010. – Т. 1. – С. 300-318.

