Влияние дифференцированной гиполипидемической терапии на степень сердечно-сосудистого риска у больных метаболическим синдромом
На правах рукописи
Гладышева Екатерина Алексеевна
Влияние дифференцированной гиполипидемической терапии на степень сердечно-сосудистого риска у больных метаболическим синдромом
14.00.06 - кардиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва 2008
Работа выполнена в ГОУ ВПО
Московская медицинская академия им. И.М.Сеченова Росздрава
Научный руководитель:
доктор медицинских наук, профессор Подзолков Валерий Иванович
Официальные оппоненты:
доктор медицинских наук, профессор Сыркин Абрам Львович
доктор медицинских наук, профессор Чазова Ирина Евгеньевна
Ведущая организация: ГОУ ВПО Российский государственный медицинский университет Росздрава
Защита состоится «__»_________2008 г. в _____ часов на заседании диссертационного совета Д.208.040.05 при ГОУ ВПО Московской медицинской академии имени И.М.Сеченова Росздрава (119991, Москва, ул. Трубецкая, д.8 стр.2).
С диссертацией можно ознакомиться в библиотеке при ГОУ ВПО Московская медицинская академия им. И.М.Сеченова Росздрава (117998, Москва, Нахимовский проспект, д. 49)
Автореферат разослан «__»_________2008 г.
Ученый секретарь
диссертационного совета,
доктор медицинских наук, профессор Волчкова Елена Васильевна
Актуальность проблемы. Сердечно-сосудистые заболевания (ССЗ) остаются по-прежнему одной из основных причин инвалидности и смертности наиболее трудоспособной части населения, унося ежегодно в мире около 17 млн. жизней. В России от ишемической болезни сердца (ИБС) и цереброваскулярной патологии умирает около 1 млн. 300 тыс. человек [Оганов Р.Г. и др., 2007; Шальнова С.А., 2001].
В последнее время возрастает интерес врачей различных специальностей к проблеме метаболического синдрома (МС), что обусловлено его значительной распространенностью в общей популяции (10-28%) и многократным увеличением риска ССЗ и смертности у этих пациентов [Чазова И.Е., Мычка В.Б., 2004; Оганов Р.Г., Перова Н.В., 2004]. В 1988 г. Reaven G.М. предложил объединить такие факторы как инсулинорезистентность, артериальная гипертония (АГ) и дислипидемия (ДЛ) под термином «метаболический синдром Х». Предложенный N.M.Kaplan в 1989 г. термин «смертельный квартет» (АГ, абдоминальное ожирение, нарушение толерантности к глюкозе (НТГ), гиперинсулинемия) в своём названии отражает наличие очень высокого риска развития фатальных сердечно-сосудистых осложнений у данной группы пациентов, что, в свою очередь, вносит значительную лепту в уровень смертности и инвалидности от ССЗ во всем мире.
Результаты эпидемиологических исследований позволяют сделать вывод о том, что МС следует рассматривать, с одной стороны, как многокомпонентное нарушение обмена веществ, а с другой – как важнейший фактор, значительно повышающий риск развития ИБС. В исследованиях 4S и AFCAPS/TexCAPS [Downs J.R., 1998] показано, что риск коронарных осложнений у пациентов с МС (без сахарного диабета 2 типа) был в 1,5 раза выше, чем при его отсутствии. По данным исследования ARIC, отмечается прогредиентное возрастание риска ИБС особенно в женской популяции при увеличении количества компонентов МС [Lakka H.M., 2002]. Таким образом, пациенты с МС имеют высокий риск развития сахарного диабета 2 типа (СД), ССЗ, общей и сердечно-сосудистой смертности.
В настоящее время существуют терминологические и диагностические проблемы, дискутируется нозологическая самостоятельность МС. Крупным достижением следует считать включение МС в Европейские рекомендации по диагностике и лечению АГ в качестве самостоятельного ФР как и СД. Большое значение для практикующих врачей имеют первые отечественные рекомендации по диагностике и лечению МС (2007 г.), в которых представлены классификация, критерии диагностики, а также намечены пути оптимизации лечения МС.
Важной проблемой является терапия такого значимого компонента МС, как дислипидемия, причем практически отсутствуют работы по лечению гипертриглицеридемии (ГТГ) при МС. В этой связи появление новых поколений статинов и фибратов может способствовать эффективному выбору оптимальной гиполипидемической терапии.
Цель работы – сравнительная оценка влияния гиполипидемической терапии (ГЛТ) препаратами различных фармакологических классов на показатели липидного спектра и сердечно-сосудистый риск (ССР) у пациентов с МС.
Задачи исследования:
- Изучить особенности нарушений липидного обмена у пациентов с МС.
- Изучить эффективность и безопасность комбинированной терапии МС с учетом особенностей суточного профиля АД и типа нарушений липидного обмена.
- Изучить гиполипидемическую эффективность и безопасность микронизированного фенофибрата у пациентов с МС.
- Изучить гиполипидемическую эффективность и безопасность пролонгированной формы флувастатина для лечения пациентов с ДЛ в рамках МС.
- Оценить влияние гиполипидемических препаратов на степень абсолютного и относительного ССР у пациентов с МС.
Научная новизна исследования. В работе выявлена гетерогенность нарушений липидного обмена в рамках МС, обоснованы дифференцированные подходы к ГЛТ у пациентов с МС и тактика выбора гиполипидемических средств различных фармакологических классов, с учетом гендерных особенностей. Впервые в России применен микронизированный фенофибрат для лечения пациентов с ГТГ в рамках МС. Определены преимущества ранней коррекции метаболических нарушений у пациентов с различными типами ДЛ в рамках МС. Доказана эффективность применения метаболически нейтральных антигипертензивных препаратов, в рамках комбинированной терапии пациентов с МС. Показана эффективность применяемых гиполипидемических препаратов, как в отношении показателей липидного обмена, так и для снижения показателей абсолютного и относительного ССР, в том числе с учетом гендерных особенностей.
Практическая значимость работы. Разработаны и обоснованы схемы дифференцированной ГЛТ у пациентов с различными типами ДЛ в рамках МС. В план обследования пациентов с МС, помимо физикального осмотра, контроля уровня АД, оценку состояния органов-мишеней, углеводного, липидного и пуринового обменов, должен быть включен обязательный расчет степени ССР. На фоне применения различных гиполипидемических средств продемонстрировано улучшение показателей липидного, углеводного, и пуринового обменов, а также достоверное снижение абсолютного и относительного ССР. Показано, что комбинация ГЛТ с агонистом имидазолиновых рецепторов 1 типа – моксонидином может рассматриваться как один из вариантов лечения МС, позволяющий достоверно снизить степень ССР.
Положения, выносимые на защиту.
- Нарушения липидного обмена у пациентов с МС гетерогенны, что требует дифференцированного подхода к выбору ГЛТ.
- Прием флувастатина и, в особенности его пролонгированной формы, в течение 24 недель достоверно улучшает показатели липидного обмена и снижает степень ССР у пациентов с МС.
- Прием микронизированного фенофибрата при изолированной ГТГ в течение 24 недель достоверно снижал уровень триглицеридов и увеличивал уровень липопротеинов высокой плотности, а также снижал показатели ССР, как у мужчин, так и у женщин.
- Прием микронизированного фенофибрата в течение 24 недель достоверно снижает уровень МК у пациентов с МС.
- Сочетание моксонидина и микронизированного фенофибрата достоверно снижает уровень тощаковой глюкозы у пациентов с МС.
Апробация работы. Проведена 27 сентября 2007 года на заседании кафедры факультетской терапии №1 лечебного факультета ММА имени И.М.Сеченова. Материалы работы доложены на конференции молодых ученых, посвященной 160-летию факультетской терапевтической клиники им. В.Н.Виноградова и 75-летию члена-корреспондента РАМН, профессора В.И.Маколкина (Москва, 2006), а также на I Национальном конгрессе терапевтов (Москва, 2006), на конгрессе «Человек и лекарство» (Москва 2005, 2006 гг.).
Внедрение результатов исследования. Результаты исследования внедрены в практику факультетской терапевтической клиники и клиники интервенционной кардиологии имени В.Н. Виноградова ММА имени И.М.Сеченова.
Публикации. По теме диссертационного исследования опубликовано 4 печатных работы.
Структура и объем диссертации. Диссертационная работа изложена на 147 страницах машинописного текста и включает в себя следующие разделы: введение, обзор литературы, материалы и методы, результаты исследования и обсуждение, заключение, выводы и практические рекомендации, библиографический список использованной литературы, включающий 177 источников, в том числе 45 отечественных. Диссертация иллюстрирована 26 таблицами и 29 рисунками.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследование проведено в период с января 2002 по сентябрь 2007 г. на базе клиники факультетской терапии и интервенционной кардиологии им. В.Н. Виноградова, межклинической биохимической лаборатории, межклинического отделения ультразвуковой диагностики ММА имени И.М.Сеченова.
В исследование, продолжавшееся 24 недели, включено 98 пациентов в возрасте 30-75 лет (54 мужчины и 44 женщины). До включения в исследование у всех больных получали добровольное информированное согласие на участие. Контроль исследуемых показателей осуществлялся трехкратно: исходно, через 12 недель и 24 недели. Критерии включения соответствовали критериям, разработанным экспертами АТР III (2001г.), согласно которым наличие у пациента МС можно предположить, если имеется 3 и более из указанных ниже симптомов: объем талии (ОТ) >88 см для женщин и >102 см для мужчин; уровень глюкозы натощак 6,1 ммоль/л (110 мг/дл); уровень триглицеридов (ТГ) 1,7 ммоль/л (150 мг/дл); уровень холестерина липопротеинов высокой плотности (ХС ЛПВП) <1,3 ммоль/л (<50 мг/дл) для женщин и <1 ммоль/л (<40мг/дл) для мужчин; повышение уровня АД 130 и 85 мм рт.ст.
Критериями исключения из исследования являлись: возраст моложе 30 лет и старше 75 лет; симптоматические АГ; СД 1 типа; печеночная и почечная недостаточности; желчнокаменная болезнь; недостаточность кровообращения III-IV функционального класса (по NYHA); клинически выраженные формы ИБС; злокачественные и аутоиммунные заболевания; нарушения ритма сердца с выраженными расстройствами гемодинамики; заболевания центральной нервной системы.
Пациентам 1 и 2 групп в качестве ГЛТ был назначен флувастатин. Пациентам 3 группы был назначен микронизированный фенофибрат в суточной дозе 200 мг.
Пациенты всех групп получали комбинированную антигипертензивную терапию следующими препаратами, обладающими метаболической нейтральностью: индапамид-ретард 1,5 мг/сут, ИАПФ в дозе 10 мг/сут. Моксонидин в дозе 200 мг/сут добавлялся в схему терапии на первых неделях исследования при недостаточной антигипертензивной эффективности препаратов. На 12 неделе в случае недостаточной гиполипидемической эффективности флувастатин 40 мг/сут заменялся на пролонгированную форму препарата - флувастатин 80 мг/сут. Доза фенофибрата оставалась постоянной на протяжении всего исследования.
Всем пациентам проводилось стандартное общеклиническое обследование с расчетом антропометрических параметров: вес, рост, ОТ и объем бедер (ОБ), индекс массы тела (ИМТ) и отношение объема талии к объему бедер (ИТБ).
Лабораторные исследования включали определение липидного спектра, уровня МК и фибриногена в плазме; ПТТГ с определением концентрации глюкозы капиллярной крови; уровня печеночных трансаминаз (АСТ, АЛТ) и креатинфосфокиназы (КФК).
Уровни ОХС, ТГ и ХС ЛПВП определяли энзиматическим методом на автоанализаторе «Техникон». Уровень ОХС расценивали как нормальный <5,2 ммоль/л, умеренно повышенный 5,2-6,2 ммоль/л, и высокий >6,2 ммоль/л. Остальные показатели липидного спектра рассчитывались по формулам: ХС ЛПОНП = ТГ/2,2 (ммоль/л); ХС ЛПНП = ОХС – (ХС ЛПВП + ЛПОНП) (ммоль/л); КА = (ОХС – ХС ЛПВП)/ХС ЛПВП.
СМАД проводили с использованием портативных регистраторов АВРМ-04 ("Meditech", Венгрия), осуществляющих регистрацию АД и ЧСС в фазу декомпрессии осциллометрическим методом. Программирование регистратора и расшифровку данных производили с помощью специализированной компьютерной программы MEDIBASE v. 1.38 (1999). Определяли средние величины систолического (САД), диастолического (ДАД) и ЧСС за 24 часа, в периоды бодрствования и сна; индекс времени (ИВ) САД и ДАД в дневные, ночные часы и за сутки в целом; степень ночного снижения (СНС) АД; вариабельность САД, ДАД и ЧСС в целом за 24 часа, а также в периоды бодрствования и сна. Степень ночного снижения АД (СНС) рассчитывалась по формуле: СНС = (АДдень - АДночь) / АДдень 100%.
Степень абсолютного ССР определяли по европейской шкале SCORE (2003 г.), позволяющей оценить 10-летний риск смерти от заболеваний, связанных с атеросклерозом. Калькуляция баллов производилась по таблице с учетом следующих параметров: пола, возраста, статуса курения, уровня САД, уровня ОХС (ммоль/л). По системе SCORE критерием высокого ССР служит величина 5% и выше.
Относительный ССР рассчитывался как отношение абсолютного ССР каждого обследованного пациента к ССР пациента той же возрастной категории, не курящего, с нормальным уровнем ОХС и оптимальным уровнем САД.
Характеристика препаратов:
Фенофибрат (микронизированный фенофибрат, препарат «Липантил 200 М»®, Solvay Pharma, Германия) суточная доза 200 мг.
Флувастатин (40 мг/сут, препарат «Лескол®», Novartis, Швейцария). «Лескол® ЭЛ» -лекарственная форма флувастатина 80 мг/сут в виде таблеток на основе матрикса, обеспечивающего замедленное высвобождение активного вещества.
Моксонидин (препарат «Физиотенз»®, Solvay Pharma, Германия, суточная доза 200 мг) антигипертензивный препарат, избирательно связывающийся с I1-имидазолиновыми рецепторами 1 типа нижнего отдела ствола ГМ, приводя к снижению активности симпатической нервной системы.
2.5. Статистическая обработка данных
Статистическую обработку данных проводили с использованием пакета программ SPSS (10,0). Результаты представлены в виде средней арифметической значения и ее среднеквадратичного отклонения (М±), или в виде медианы, или в виде % от анализируемой группы. Для оценки достоверности различий между независимыми переменными при нормальном распределении выборки использовали дисперсионный анализ, между группами до и после лечения — парный и непарный критерии Стьюдента. В случаях ненормального распределения выборки, для оценки достоверности различий между независимыми переменными использовали непараметрический критерий Крускала-Уоллиса, между зависимыми (до и после лечения) — критерий Вилкоксона. Для сравнения достоверности различий между дискретных переменных использовали критерий 2 для таблицы 2х2, в точном решении Фишера. Для выявления взаимосвязей между показателями рассчитывали коэффициент корреляции Пирсона (r), а при ненормальном распределении выборки или для оценки качественных признаков — коэффициент ранговой корреляции Спирмена (rs). Различия считали достоверными при уровне значимости р0,05, тенденцией – при 0,05<р0,1.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ.
Выявленные исходно изменения в липидном спектре и величина абсолютного ССР по таблице SCORE, позволили подразделить пациентов на 4 группы (рис.1).

Рисунок 1. Схема распределения пациентов.
1 группу составили пациенты, у которых отмечалось сочетание повышенного уровня общего холестерина (ОХС) и холестерина липопротеинов низкой плотности (ХС ЛПНП). 2 группу составили пациенты, у которых было выявлено сочетание повышенного уровня ОХС, ХС ЛПНП, липопротеинов очень низкой плотности (ЛПОНП), а также ТГ. 3 группу составили пациенты с сочетанием повышенного уровня ТГ и ЛПОНП при сниженном уровне ХС ЛПВП. У всех пациентов абсолютный риск ССЗ был выше 5%. В качестве группы контроля (4 группа) были отобраны пациенты с МС, у которых величина абсолютного ССР по таблице SCORE составляла <5%. Пациентам данной группы не назначалась медикаментозная коррекция ДЛ, они придерживались только гиполипидемической диеты.
Шесть пациентов выбыли из исследования досрочно: четверо в связи с добровольным отказом от дальнейшего приема препаратов, двое в связи с развитием нежелательных явлений в виде диспепсии и кожного зуда на фоне приема микронизированного фенофибрата.
Таблица 1. Общая характеристика обследованных пациентов
| Характеристики, абс., (%) | Группа 1 (n=21) | Группа 2 (n=26) | Группа 3 (n=30) | Группа 4 (n=21) | |
| Возраст, лет | 60,71±10,19* | 54,81±10,10 | 53,53±11,60 | 50,19±12,91 | |
| Курение, абс.(%) | 3 (14,3) | 13 (50,0) | 17 (56,7) | 8 (38,1) | |
| Длительность АГ, лет | 10,43±2,75 | 12,46±5,16 | 10,03±2,1 | 10,38±3,8 | |
| Сопутств.заб-я, абс.(%) - хр. холецистит - хр. гастрит - язвенная болезнь желудка/12-перстной кишки - хр. бронхит - остеохондроз - остеоартроз | 2 (9,5) 6 (28,6) 11(52,4) 7 (33,3) 10 (47,6) 7 (33,3) | 1 (3,8) 5 (19,2) 10 (38,5) 14 (53,8) 9 (34,6) 7 (26,9) | 0 (0) 4 (13,3) 12 (40,0) 21 (70,0) 5 (16,7) 4 (13,3) | 1 (4,8) 3 (14,3) 9 (42,9) 8 (38,1) 5 (23,8) 2 (9,5) | |
* - р<0,05, ** - р<0,001 при сравнении с исходным значением
В исследовании принимали участие 54 мужчины и 44 женщины. Средний возраст у мужчин составил 52,67±12,53 лет, у женщин 57,20±9,91 лет. Возраст пациентов 1 группы был достоверно выше, чем в остальных группах (р<0,05). Пациенты всех исследуемых групп были сопоставимы по длительности АГ. Все пациенты достоверно не различались по частоте сопутствующих заболеваний желудочно-кишечного тракта, дыхательной и опорно-двигательной систем (табл. 1).
Таблица 2. Частота встречаемости компонентов МС в изучаемых группах.
| Характеристики, абс., (%) | Группа 1 (n=21) | Группа 2 (n=26) | Группа 3 (n=30) | Группа 4 (n=21) |
| Абдоминальное ожирение | 11 (57,5) | 16 (60,8) | 21 (69,3)* | 7 (33,6) |
| Нарушение углеводного обмена | 8 (38,4) | 13 (49,4)* | 12 (39,6) | 3 (14,4) |
| НТГ | 1 (4,8) | 1 (3,8) | 2 (6,6) | 0 (0) |
| Гиперурикемия | 5 (24) | 10 (38) | 16 (52,8)* | 7 (33,6) |
| Гиперфибриногенемия | 8 (38,2) | 4 (15,2) | 8 (26,4) | 0 (0) |
| Избыточный вес (ИМТ=25,0-29,9) | 9 (43,2) | 10 (38,0) | 16 (52,8)* | 4 (19,2) |
| Ожирение I ст. (ИМТ=30,0-34,9) | 4 (19,2) | 6 (22,9) | 9 (29,7) | 8 (38,4) |
| Ожирение II ст. (ИМТ=35,0-39,9) | 2 (9,6) | 2 (7,7) | 0 (0) | 1 (4,8) |
| Ожирение III ст. (ИМТ >40) | 2 (9,6) | 1 (3,8) | 2 (6,7) | 0 (0) |
* - р<0,05
В каждой группе мы оценивали частоту встречаемости отдельных компонентов МС (табл. 2). Нарушения в углеводном статусе достоверно чаще встречались у пациентов 2 группы. В 3 группе достоверно чаще, чем в остальных встречалось абдоминальное ожирение, гиперурикемия, а также избыточный вес. Количество пациентов с ожирением различных степеней достоверно не различалось между группами.
Известно, что избыточная масса тела и ожирение являются важными, алиментарно корригируемыми ФР развития и прогрессирования ССЗ [Перова Н.В., 2005; Медведева И.В., 2001; Соловьева Е.Ю., 1992 ]. Среди наших пациентов у 68% имелась наследственная отягощенность по наличию избыточной массы тела у близких родственников, преимущественно у матерей (56%).
Через 24 недели в 1, 2, 3 и 4 группах у мужчин была отмечена недостоверная динамика исследуемых антропометрических показателей: ИМТ уменьшился на 3%, ОТ на 3,1%, ИТБ на 2%. У женщин было отмечено достоверное снижение лишь ИМТ на 3,8% (р<0,05).
При анализе липидных показателей в 1 группе к концу 12 недели на фоне терапии флувастатином 40 мг/сут была получена достоверная динамика, однако не был достигнут целевой уровень (табл. 3), в этой связи флувастатин был заменен на флувастатин ЭЛ. Отмечался достоверный рост показателя ХС ЛПВП, который к 24 неделе достиг целевых значений у мужчин и женщин, отличаясь от исходного на 16% (табл. 3).
Во 2 группе (табл. 3) получена достоверная динамика на фоне терапии флувастатином в дозе 40 мг/сут, однако, как и в 1 группе в течение 12 недель не были достигнуты целевые значения липидов. В результате замены флувастатина на флувастатин ЭЛ, уровни ОХС и ХС ЛПНП к 24 неделе достигли целевых значений, снизившись на 28,2% и 38,5% соответственно. Уровень ТГ к концу исследования снизился на 16,7%, но оставался выше целевых значений. Уровень ХС ЛПВП исходно был нормальным и достоверно не изменился за время исследования.
Таблица 3. Показатели липидного обмена у пациентов исследуемых групп.
| Показатель, ммоль/л | Исходно | 12 недель | 24 недели |
| 1 группа | |||
| ОХС, ммоль/л | 7,30±1,08 | 6,43±1,07** | 6,55±1,52* |
| ТГ, ммоль/л | 1,40±0,31 | 1,63±0,53* | 1,62±0,68* |
| ХСЛПНП, ммоль/л | 5,48±1,20 | 4,40±1,12** | 4,48±1,58* |
| ХС ЛПВП, ммоль/л | 1,18±0,44 | 1,29±0,46** | 1,37±0,43** |
| ЛПОНП, ммоль/л | 0,64±0,14 | 0,74±0,24* | 0,74±0,31* |
| КА | 6,30±1,09 | 5,43±1,07** | 5,55±1,52* |
| 2 группа | |||
| ОХС, ммоль/л | 7,21±0,78 | 5,74±1,10** | 5,18±1,15** |
| ТГ, ммоль/л | 2,63±0,63 | 1,97±0,83** | 2,19±0,16** |
| ХС ЛПНП, ммоль/л | 4,93±0,73 | 3,70±1,14** | 3,03±1,18** |
| ХС ЛПВП, ммоль/л | 1,09±0,29 | 1,14±0,27 | 1,15±0,25 |
| ЛПОНП, ммоль/л | 1,20±0,29 | 0,90±0,38** | 1,00±048** |
| КА | 6,21±0,78 | 5,05±1,04** | 5,32±0,63** |
| 3 группа | |||
| ОХС, ммоль/л | 5,77±0,96 | 5,69±0,73 | 5,64±0,90 |
| ТГ, ммоль/л | 3,08±0,16 | 2,25±0,97** | 2,07±0,74** |
| ХС ЛПНП, ммоль/л | 3,41±0,92 | 3,61±0,80* | 3,51±0,83 |
| ХС ЛПВП, ммоль/л | 0,96±0,33 | 1,06±0,31** | 1,18±0,40** |
| ЛПОНП, ммоль/л | 1,40±0,53 | 1,02±0,44** | 0,94±0,34** |
| КА | 4,77±0,96 | 4,69±0,73 | 4,64±0,90 |
| 4 группа | |||
| ОХС, ммоль/л | 6,50±1,17 | 6,39±1,32 | 6,48±1,19 |
| ТГ, ммоль/л | 1,88±0,56 | 1,97±0,57 | 1,87±0,61 |
| ХС ЛПНП, ммоль/л | 4,36±1,23 | 4,20±1,38 | 4,32±1,19 |
| ХС ЛПВП, ммоль/л | 1,28±0,39 | 1,30±0,37 | 1,31±0,37 |
| ЛПОНП, ммоль/л | 0,86±0,26 | 0,90±0,26 | 0,85±0,28 |
| КА | 5,50±1,17 | 5,39±1,32 | 5,48±1,19 |
* - р<0,05, ** - р<0,001 при сравнении с исходным значением
В 3 группе на фоне терапии микронизированным фенофибратом в течение 12 недель уровень ТГ достоверно уменьшился на 26,9%, уровень ЛПОНП на 27% по уподоблению с исходным. Уровень ХС ЛПНП увеличился по сравнению с исходным на 5,87%. Уровень ХС ЛПВП за 12 недель увеличился на 10,4%, продолжая достоверно увеличиваться с 12 по 24 неделю. К 24 неделе он был выше исходного показателя на 22%, достигнув целевых значений. Уровень ТГ к 24 неделе был достоверно ниже исходных показателей на 32,7%, но так и не достиг целевого значения (1,7 ммоль/л). За время наблюдения у пациентов 3 группы не отмечено достоверной динамики уровня ОХС (рис. 2).

* - р<0,05, ** - р<0,001
Рисунок 2. Динамика показателей липидного спектра пациентов 3 группы.
Низкий уровень ХС ЛПВП обладает самостоятельным неблагоприятным прогностическим значением в отношении развития осложнений ИБС, даже при нормальном уровне ХС ЛПНП. На фоне применения флувастатина в 1 группе отмечалась достоверная динамика показателя ХС ЛПВП, однако в 3 группе на фоне применения микронизированного фенофибрата была отмечена наибольшая достоверная динамика уровня ХС ЛПВП по сравнению с другими группами, причем, к концу исследования данный показатель был достоверно выше у женщин, чем у мужчин (рис.3).

Рисунок 3. Динамика уровня ХС ЛПВП у мужчин и женщин 3 группы. (*- р<0,05)
В 4 группе исходно и на протяжение всего исследования, не было выявлено существенной достоверной динамики показателей липидного спектра (табл.3). Наиболее существенным наблюдением за весь период было то, что в целом по группе к 12 неделе наметилась тенденция к нарастанию уровня ТГ и ЛПОНП (р=0,060).
АГ является основным компонентом МС и одним из важнейших стратификационных ФР ССЗ. Во всех группах к 24 неделе мы получили достоверную положительную динамику параметров СМАД на фоне комбинированной антигипертензивной терапии. Большинство пациентов (85%) через 24 недели достигли целевых цифр АД, которыми мы считали, с учетом количества и качества ФР.


Рисунок 4. Структура АГ исходно и через 24 недели.
Исходно в нашей выборке преобладали пациенты с изолированной систолической АГ (ИСАГ) (60%) и систоло-диастолической АГ (35,5%). Через 24 недели у 85% пациентов уровень АД находился в нормальных пределах (рис.4).
При анализе суточного профиля АД исходно (рис.5), было отмечено преобладание прогностически неблагоприятных типов, так в 1 и 4 группах преобладающим был тип «нон-диппер», во 2 группе лишь у 1/3 больных был нормальный тип суточного профиля АД, а 2/3 составляли «овер-дипперы» и «нон-дипперы». В 3 группе в отличие от всех групп, нормальный тип суточного профиля встречался реже всего (16,5%), доминировал тип «нон-диппер».

Рисунок 5. Исходные типы суточного профиля исходно.
Через 24 недели в 1 и 2 группах количество «дипперов» увеличилось и превзошло 50%. В первых трех группах уменьшилось количество «нон-дипперов», особенно во 2 группе. В 3 группе увеличилось количество «овер-дипперов», отмечены единичные случаи ночного повышения АД (тип «найт-пикер»). В 4 группе преобладающим типом оставался тип «нон-диппер», как и в 3 группе отмечены единичные случаи ночного повышения АД (рис.6).
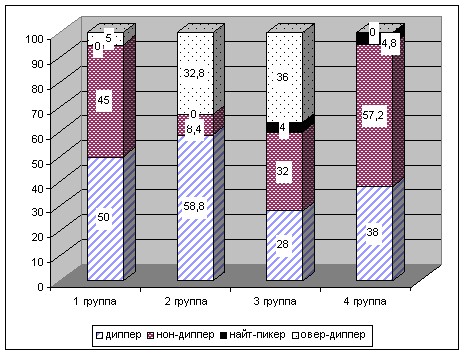
Рисунок 6. Типы суточного профиля через 24 недели.
Большой интерес вызывало применение моксонидина для лечения пациентов с МС, так как данный препарат, в рамках недавно завершившегося национального исследования АЛМАЗ [Чазова И.Е., 2006], помимо хорошего гипотензивного эффекта, показал свое позитивное влияние на углеводный и липидный статус. По нашим данным включение в схему комбинированной антигипертензивной терапии моксонидина в дозе 200 мг/сут достоверно влияет на уровень среднего САД за сутки и дневной период. Трехкомпонентная терапия, включающая моксонидин, индапамид и ингибитор АПФ в среднетерапевтических дозировках, способствует стойкому антигипертензивному эффекту, сохраняющемуся на протяжении 24 недель.
Многие современные исследователи рассматривают МС как прелюдию СД 2 типа: риск развития СД 2 типа у лиц с МС в среднем в 5-9 раз выше, чем при его отсутствии [Isomaa B.,2001; Pagotto U.,2002]. В этой связи большой интерес представляют результаты перорального теста на толерантность к глюкозе (ПТТГ) у пациентов с МС. Результаты и динамика показателей ПТТГ представлены в табл. 4.
Таблица 4. Динамика показателей ПТТГ.
| Показатель, мг/дл | Исходно | 12 недель | 24 недели |
| 1 группа | |||
| Глюкоза натощак, мг/дл | 99,86±17,77 | 100,86±13,43 | 105,35±25,97 |
| Глюкоза ч/з 1 час, мг/дл | 137,86±19,19 | 138,52±13,52 | 145,45±37,18 |
| Глюкоза ч/з 2 часа, мг/дл | 96,14±19,48 | 98,29±16,53 | 102,90±26,66 |
| 2 группа | |||
| Глюкоза натощак, мг/дл | 112,88±18,47 | 105,73±12,55* | 105,46±11,02* |
| Глюкоза ч/з 1 час, мг/дл | 146,04±29,89 | 142,77±14,88 | 143,00±11,13 |
| Глюкоза ч/з 2 часа, мг/дл | 106,15±19,84 | 103,54±16,57 | 102,25±14,74 |
| 3 группа | |||
| Глюкоза натощак, мг/дл | 100,63±18,41 | 99,97±18,72 | 102,28±14,14 |
| Глюкоза ч/з 1 час, мг/дл | 135,47±21,34 | 139,63±13,90 | 136,92±14,15 |
| Глюкоза ч/з 2 часа, мг/дл | 110,47±30,61 | 105,77±20,09 | 103,68±19,00 |
| 4 группа | |||
| Глюкоза натощак, мг/дл | 103,57±9,59 | 105,19±9,9 | 103,33±12,02 |
| Глюкоза ч/з 1 час, мг/дл | 129,14±14,56 | 130,29±12,28 | 132,24±17,22 |
| Глюкоза ч/з 2 часа, мг/дл | 100,33±9,84 | 97,10±10,71 | 95,71±14,68 |
* - р<0,05, ** - р<0,01, *** - р<0,001 при сравнении с исходными данными во 2 группе.
В 1, 3 и 4 группах, по данным ПТТГ, за период исследования не получено статистически значимого снижения уровня тощаковой глюкозы крови. Лишь во 2 группе через 12 недель отмечено достоверное снижение уровня глюкозы натощак на 6,33% по сравнению с исходным, а через 24 недели на 6,57% по сравнению с исходным (р<0,05).
Через 12 недель лечения получена достоверная корреляция между приемом моксонидина в дозе 200 мг/сут и уровнем глюкозы через 2 часа после приема 75,0 глюкозы у женщин во всех изучаемых группах (r=0,350, р=0,020). В 1, 2 и 4 группах было отмечено, что прием моксонидина в течение 24 недель достоверно не ухудшал углеводный обмен, в 3 группе на 12 неделе приема моксонидина уровень тощаковой глюкозы был на 14,2% ниже, чем в группах не принимавших данный препарат (р=0,033).
У больных МС часто встречается гиперурикемия, в последнее время считающаяся вероятностным ФР развития ИБС. В нашем исследовании гиперурикемия встречалась преимущественно у пациентов 3 группы.
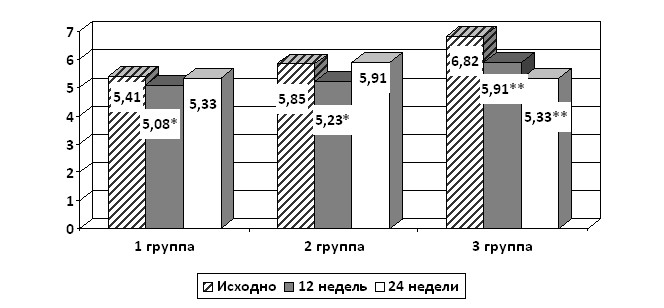
Рисунок 7. Динамика уровня МК. (* р<0,05, **р<0,001)
В 1 и 2 группах на фоне приема флувастатина 40 мг/сут, в условиях исходно нормального уровня МК, к концу 12 недель наблюдения отмечено его достоверно снижение. Лишь в 3 группе на фоне приема микронизированного фенофибрата уровень МК достоверно снижался на протяжении всего исследования (рис.7). В 4 группе достоверной динамики уровня МК за время исследования выявлено не было.
При исследовании взаимосвязи между показателями липидного спектра и уровнем МК была отмечена достоверная корреляция между исходным уровнем ТГ и исходным уровнем МК (r=0,435, p<0,001). Подобная корреляция сохраняется между показателями через 12 недель наблюдения (r=0,310, p=0,002) и через 24 недели наблюдения (r=0,310, p=0,003). Достоверная отрицательная корреляция наблюдалась между исходным уровнем МК и исходным уровнем ХС ЛПВП (r=-0,303, p=0,004). Данная взаимосвязь отмечалась через 12 недель (r=-0,213, p=0,035) и через 24 недели наблюдения (r=-0,229, p=0,030).
Фибриноген является независимым фактором ССР, неблагоприятная прогностическая значимость которого увеличивается при сочетании с ГХС и высоким САД. В этой связи следует отметить как позитивный факт, что за время наблюдения ни в одной из групп достоверной динамики уровня фибриногена отмечено не было, что со своей стороны дополнительно не увеличивает ССР.
Абсолютный ССР (суммарный) оценивался по таблице SCORE. Одиннадцать пациентов не принимали участие в оценке риска по таблице SCORE в связи с возрастными ограничениями. Абсолютный риск расценивался как низкий (0-4%), средний (4-5%), высокий (5-8%) и очень высокий (8% и выше). В нашей выборке до начала лечения преобладали пациенты с высоким и средним абсолютным риском. Это, вероятно, связано с тем, что средний возраст пациентов превышал 50 лет, преобладали мужчины, большинство из которых были курильщики с АГ и ГХС.
Исходно показатели абсолютного ССР достоверно не отличались у пациентов первых трех групп (табл.5). В течение 12 недель на фоне приема флувастатина в дозе 40 мг/сут было отмечено достоверное снижение показателя абсолютного ССР на 30% от исходного уровня. У пациентов 1 и 2 групп удвоение дозы флувастатина не привело к существенной динамике уровня абсолютного ССР.
Таблица 5. Динамика показателей ССР у мужчин и женщин в группах сравнения.
| 1 группа | 2 группа | 3 группа | ||||
| М | Ж | М | Ж | М | Ж | |
| АР исх. | 9,20±2,83 | 4,33±0,78 | 5,50±1,11 | 4,60±0,71 | 6,44±2,09 | 4,20±0,92 |
| ОР исх. | 3,28±1,21 | 3,63±1,28 | 2,65±0,80 | 3,63±1,50 | 4,18±1,54 | 3,50±1,63 |
| АР 12 нед. | 7,00±1,30* | 1,67±0,78* | 4,36±0,98 | 2,56±0,67^ | 4,17±1,29 | 2,00±1,41 |
| ОР 12 нед. | 2,10±1,02* | 1,38±0,74* | 2,25±1,02 | 1,96±0,53^ | 2,35±0,61 | 1,55±0,63 |
| АР 24 нед. | 7,80±1,14 | 1,36±0,50* | 4,78±0,26 | 2,25±0,83^ | 2,79±0,93 | 1,89±0,45 |
| ОР 24 нед. | 2,38±1,04 | 1,14±0,60* | 2,29±1,30 | 1,52±0,40^ | 1,85±0,16 | 1,44±0,45 |
АР – абсолютный риск; ОР- относительный риск.* - р<0,05, ** - р<0,001 при сравнении результатов для 1 группы; ^ - р<0,05, ^^- р<0,001 при сравнении результатов для 2 группы; - р<0,05, - р<0,001 при сравнении результатов для 3 группы;
В 3 группе на фоне приема микронизированного фенофибрата в течение 12 недель показатель абсолютного ССР достоверно снизился на 40%, а к 24 неделе на 57% от исходного уровня. В 4 группе за все время наблюдения достоверной динамики показателей абсолютного ССР получено не было.

Рисунок 8. Динамика показателей абсолютного риска у мужчин. * р<0,05, **р<0,001
Показатели абсолютного ССР у мужчин только в 3 группе на фоне приема микронизированного фенофибрата достоверно снижались на протяжении всего исследования. В 1 и 2 группах на фоне приема флувастатина, нестойкая положительная динамика показателя отмечалась только в течение первых 12 недель (рис.8). У женщин, в 1, 2, 3 группах за период исследования отмечено достоверное снижение показателя абсолютного риска (рис.9).

Рисунок 9. Динамика показателей абсолютного риска у женщин. * р<0,05, **р<0,001
В 4 группе за все время наблюдения достоверной динамики показателей абсолютного и относительного ССР получено не было (табл. 5).
Для изучения переносимости проводимой гиполипидемической терапии на каждом визите оценивалась динамика уровней печеночных трансаминаз и КФК. Исходные показатели печеночных трансаминаз и КФК достоверно не отличались между группами (табл.6).
Таблица 6. Динамика уровня печеночных трансаминаз и КФК.
| Показатель | Исходно | Через 12 недель | Через 24 недели |
| 1 группа | |||
| КФК, ед/л | 78,52±10,11 | 121,05±31,82** | 179,50±66,68** |
| АСТ, ед/л | 26,01±5,97 | 25,88±9,98 | 27,57±9,07 |
| АЛТ, ед/л | 27,92±8,67 | 27,06±4,60 | 31,09±15,28 |
| 2 группа | |||
| КФК, ед/л | 77,08±7,71 | 105,85±45,57^^ | 165,46±65,89^^ |
| АСТ, ед/л | 24,75±8,85 | 24,75±9,7 | 26,68±10,2 |
| АЛТ, ед/л | 27,82±8,57 | 28,63±4,67 | 33,69±7,2 |
| 3 группа | |||
| КФК, ед/л | 85,13±35,67 | 214,12±82,4 | 123,57±56,89 |
| АСТ, ед/л | 25,85±7,98 | 28,21±4,5 | 26,20±9,13 |
| АЛТ, ед/л | 29,78±5,48 | 32,23±8,2 | 30,47±10,62 |
| 4 группа | |||
| КФК, ед/л | 62,90±15,32 | 66,97±13,66† | 64,92±13,43 |
| АСТ, ед/л | 27,48±9,59 | 25,60±8,61 | 27,06±7,39 |
| АЛТ, ед/л | 24,03±7,72 | 26,34±9,47 | 28,90±7,12 |
* - р<0,05, ** - р<0,001 при сравнении результатов для 1 группы; ^ - р<0,05, ^^- р<0,001 при сравнении результатов для 2 группы; - р<0,05, - р<0,001 при сравнении результатов для 3 группы; †- р<0,05, ††- р<0,001 при сравнении результатов для 4 группы
На фоне терапии микронизированным фенофибратом, как и на фоне терапии стандартной и пролонгированной формами флувастатина на протяжении всего исследования была выявлена достоверная динамика КФК, не превысившая 3-х норм, что не потребовало отмены препаратов. Достоверной динамики печеночных трансаминаз во всех группах терапии за время исследования не отмечалось (табл.6).
ВЫВОДЫ
- У больных метаболическим синдромом выявлена гетерогенность нарушений липидного обмена: у 30% - дислипидемия IIa типа, у 36 % - дислипидемия IIb типа, и у 34% дислипидемия IV типа.
- Показано, что прием флувастатина наиболее эффективен при комбинированной дислипидемии (IIb тип). Причем уже к 12 неделе отмечено достоверное снижение уровня общего холестерина на 20,4%, уровня триглицеридов на 25%.
- Выявлено, что при изолированной гипертриглицеридемии (IV тип) прием микронизированного фенофибрата достоверно снижал уровень триглицеридов на 32,7%, при этом достигалось повышение ХС ЛПВП на 22%. Плейотропным действием препарата являлось снижение на 23% уровня мочевой кислоты.
- Показано, что исходно нормальный тип суточного профиля АД определяется лишь у 1/3 пациентов с метаболическим синдромом, преобладают прогностически неблагоприятные типы суточного профиля, такие как «нон-диппер» и «овер-диппер».
- Добавление моксонидина в качестве третьего препарата к двухкомпонентной схеме комбинированной антигипертензивной терапии позволяет к концу 12 недели достичь целевого уровня АД у 85% пациентов с метаболическим синдромом.
- Абсолютный сердечно-сосудистый риск на фоне приема флувастатина достоверно снижался на 32%, на фоне приема микронизированного фенофибрата на 57%. Относительный сердечно-сосудистый риск на фоне приема флувастатина достоверно снижался на 44%, на фоне приема микронизированного фенофибрата на 57%.
- Выявлены гендерные различия уровня снижения абсолютного и относительного сердечно-сосудистого риска на фоне приема флувастатина. Абсолютный сердечно-сосудистый риск снизился у женщин на 61%, у мужчин на 14%. Относительный сердечно-сосудистый риск снизился на 64% и 18% соответственно. Подобных различий в группе микронизированного фенофибрата отмечено не было.
- Наличие в схеме комбинированной терапии сочетания моксонидина и микронизированного фенофибрата достоверно снижает уровень тощаковой глюкозы уже к 12 неделе на 14,2 %.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Всем пациентам с метаболическим синдромом необходимо проводить расчет степени абсолютного и относительного риска развития фатальных сердечно-сосудистых осложнений.
- Пациентам с метаболическим синдромом при сочетании изолированной гипертриглицеридемии (дислипидемия IV типа), нарушения толерантности к глюкозе и гиперурикемии показано назначение микронизированного фенофибрата.
- Пациентам с метаболическим синдромом при наличии комбинированной гиперлипидемии (IIb тип) может быть рекомендован прием флувастатина в дозе 80 мг/сут.
- Моксонидин в дозе 200 мг/сут рекомендуется включать в схему комбинированной антигипертензивной терапии у больных метаболическим синдромом. Моксонидин может быть назначен данным пациентам в том числе для улучшения углеводного обмена.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Маколкин В.И., Осадчий К.К., Гладышева Е.А. Влияние низкодозовой комбинации антигипертензивных препаратов на состояние микроциркуляции // Кардиология, 2005. т.45. №2. С.24-25.
- Подзолков В.И., Гладышева Е.А., Панферов А.С. Метаболический синдром: современные возможности лечения //Обзоры клинической кардиологии, 2006. №8. С.16-23.
- Подзолков В.И., Гладышева Е.А. Клинический случай успешного применения моксонидина у пациентки с постменопаузальным метаболическим синдромом // Ожирение и метаболизм, 2007. №1(10). С.37-40.
- Подзолков В.И., Гладышева Е.А., Брагина А.Е. Роль моксонидина в комбинированной антигипертензивной терапии пациентов с метаболическим синдромом //Артериальная гипертензия, 2007. т.13. №4. С.246-249.
СПИСОК СОКРАЩЕНИЙ
АГ – артериальная гипертензия
АД – артериальное давление
АЛТ – аланиновая трансаминаза
АСТ – аспарагиновая трансаминаза
ГТГ - гипертриглицеридемия
ГХС - гиперхолестеринемия
ДАД –диастолическое артериальное давление
ИАПФ – ингибиторы ангиотензин-превращающего фермента
ИБС - ишемическая болезнь сердца
ИМТ - индекс массы тела
ИТБ – отношение объема талии к объему бедер
КА – коэффициент атерогенности
КФК - креатинфосфокиназа
ЛПНП – липопротеины низкой плотности
ЛПВП – липопротеины высокой плотности
ЛПОНП – липопротеины очень низкой плотности
МС – метаболический синдром
ОХС – общий холестерин
ПТТГ – пероральный тест на толерантность к глюкозе
САД – систолическое артериальное давление
СД – сахарный диабет
СМАД – суточное мониторирование артериального давления
ССЗ – сердечно-сосудистые заболевания
ССР – сердечно-сосудистый риск
ТГ - триглицериды
ФР – фактор риска
ЧСС – частота сердечных сокращений

