Неврологические и когнитивные проявления хронических расстройств мозгового кровообращения у больных сахарным диабетом 2 типа
На правах рукописи
БАССЭ ДАРЬЯ АНАТОЛЬЕВНА
НЕВРОЛОГИЧЕСКИЕ И КОГНИТИВНЫЕ ПРОЯВЛЕНИЯ ХРОНИЧЕСКИХ РАССТРОЙСТВ МОЗГОВОГО КРОВООБРАЩЕНИЯ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 2 ТИПА
14.00.13 – Нервные болезни
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва - 2009
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель:
академик РАМН, доктор
медицинских наук, профессор
Гусев Евгений Иванович
Официальные оппоненты:
доктор медицинских наук, профессор
Максимова Марина Юрьевна
доктор медицинских наук, профессор
Савин Алексей Алексеевич
Ведущая организация:
Московская Медицинская Академия имени И.М. Сеченова
Защита состоится «21» сентября 2009 года в 14.00 часов на заседании диссертационного совета Д 208.072.09 при ГОУ ВПО РГМУ Росздрава по адресу: 117997, г. Москва, ул. Островитянова, д. 1.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО РГМУ Росздрава по адресу: 117997, г. Москва, ул. Островитянова, д. 1
Автореферат разослан «16» июня 2009 года
Ученый секретарь диссертационного совета
кандидат медицинских наук, профессор Л.В. Губский
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования
Сахарный диабет 2 типа (СД 2 типа) является одним из важных факторов риска развития сосудистой патологии головного мозга. Для пациентов с СД 2 типа характерно повышение вероятности возникновения ишемического инсульта, широкое распространение хронических форм расстройств мозгового кровообращения (Гусев Е.И., Скворцова В.И., 2001Vermeer S. E., Koudstaal P. J. et al, 2002). Исследования последних лет предоставляют сведения о достоверной связи между наличием СД 2 типа и риском возникновения сосудистой деменции (Biessels, G.J., Staekenborg, S., et al, 2006; Peila, R., Rodrguez, B.L., Launer, L.J., 2002).
Проблема деменции в современной медицине становится одной из наиболее актуальных на сегодняшний день, что связано с выраженным ухудшением качества жизни пациентов, страдающих этим заболеванием, их инвалидизацией. Немаловажным является и экономическая составляющая проблемы.
В последние годы большой интерес вызывают ранние, додементные нарушения - легкие или умеренные когнитивные расстройства (УКР; mild cognitive impairment) (Peterson RS., Touchon J., 2005). Клиническая значимость этих расстройств определяется повышенным риском развития деменции (Ritchie K., et al, 2001; Shankle WR., 2005).
Учитывая, что при СД 2 типа отмечается повышенный риск развития микро- и макрососудистых осложнений, а также имеются дисметаболические расстройства (гипергликемия и инсулинорезистентность), которые могут являться независимыми факторами риска развития когнитивной дисфункции (Biessels GJ, Staekenborg S, Brunner E, et al, 2006), изучение ранних проявлений сосудистой мозговой недостаточности у этого контингента больных представляет особую значимость.
Несмотря на активное изучение роли СД 2 типа в развитии когнитивных нарушений, в рамках этой проблемы остается множество вопросов. Недостаточно изучена роль когнитивных расстройств как симптомов поражения головного мозга у пациентов, страдающих СД 2 типа. В отечественной литературе отсутствуют комплексные исследования, посвященные качественному и количественному нейропсихологическому анализу семиотики когнитивных расстройств, не достигающих степени деменции, при СД 2 типа. Не выработано единого мнения о факторах, влияющих на развитие когнитивной дисфункции при СД 2 типа.
Актуальность проблемы определяется также вопросами лечения пациентов с СД 2 типа. Адекватный контроль уровня глюкозы в крови обладает выраженным защитным действием в отношении развития микроангиопатии. Однако вероятность макрососудистых осложнений у больных СД 2 типа остается высокой даже при адекватной коррекции углеводного обмена (UK Prospective Diabetes Study (UKPDS) Group, 1998). Поэтому поиск возможных путей медикаментозного лечения когнитивных нарушений и предупреждения прогрессирования сосудистых, метаболических поражений головного мозга у больных СД 2 типа является важной задачей.
Цель исследования
Изучение неврологических и когнитивных проявлений хронических расстройств мозгового кровообращения у больных СД 2 типа.
Задачи исследования
- Изучить проявления хронической сосудистой мозговой патологии у пациентов с различной длительностью СД 2 типа на основании клинико-неврологического и нейропсихологического исследований.
- Оценить влияние факторов – возраста, уровня артериального давления, выраженности атеросклероза, инсулинорезистентности, гипергликемии – на состояние когнитивных функций у этих больных.
- Изучить состояние вещества головного мозга по данным полуколичественной оценки МРТ и оценить связь выявленных изменений с нарушением когнитивных функций у больных СД 2 типа.
- Выявить связь клинико-неврологических и нейровизуализационных проявлений хронического сосудистого поражения головного мозга у больных СД 2 типа с концентрациями молекул клеточной адгезии, сосудистой адгезии, Е-селектина, hs-CРБ, фибриногена в сыворотке крови.
- Изучить значимость содержания аутоантител к нейронспецифическим белкам (глиальному фибриллярному кислому белку, глияспецифическому белку S-100) у больных СД 2 типа и оценить их связь с выраженностью когнитивных нарушений.
Научная новизна
Впервые проведена комплексная оценка додементных когнитивных расстройств у пациентов с СД 2 типа без выраженного очагового неврологического дефицита. Изучена роль таких факторов как возраст, повышение АД, длительность АГ, липидные и метаболические нарушения на возникновение когнитивной дисфункции при СД 2 типа.
Установлено, что когнитивные нарушения представляют наиболее ранний признак хронического сосудистого поражения головного мозга при СД 2 типа. Выявлена высокая частота когнитивных расстройств у пациентов с длительным течением заболевания.
Проведена оценка связи когнитивных нарушений с изменениями вещества головного мозга по данным МРТ. Изучено влияние длительности течения диабета, сосудистых факторов и метаболических расстройств на выраженность диффузных изменений белого вещества головного мозга по данным МРТ. Установлена связь между выраженностью перивентрикулярного лейкоареоза и длительностью СД 2 типа.
Впервые изучена роль молекул адгезии, hs-CРБ, фибриногена, наличия мозгоспецифических аутоантител в сыворотке крови в качестве биохимических маркеров сосудистого поражения вещества головного мозга при СД 2 типа.
Практическая значимость
Выявленные клинические особенности хронического сосудистого поражения головного мозга при СД 2 типа позволяют обратить внимание врачей неврологов и эндокринологов на повышенный риск возникновения у больных с диабетом когнитивных расстройств. Это делает необходимым проведение эффективной диагностики когнитивной дисфункции на стадии додементных расстройств для адекватной профилактики развития тяжелого когнитивного дефицита у пациентов с СД 2 типа. Использованные в работе шкалы и тесты могут применяться с целью ранней диагностики когнитивных нарушений при проведении нейропсихологического тестирования.
Изучение роли молекул адгезии, hs-CРБ, фибриногена, мозгоспецифических аутоантител в сыворотке крови в качестве возможных биохимических маркеров сосудистого поражения головного мозга при СД 2 типа является важным для разработки методов лабораторной диагностики хронической сосудистой мозговой патологии.
Уточнение факторов патогенеза поражения головного мозга и развития когнитивных нарушений у пациентов с СД 2 типа имеет значение в разработке вопросов лечения. Выявление патогенетической роли ряда сосудистых факторов риска в развитии когнитивной дисфункции при СД 2 типа делает обоснованным применение сосудистых препаратов у данного контингента пациентов.
Положения, выносимые на защиту
- Клиническая картина хронической сосудистой мозговой патологии у больных СД 2 типа без инсульта в анамнезе характеризуется жалобами неврологического и когнитивного характера на ухудшение памяти, рассеянность, трудности подбора слов в разговоре, утомляемость; минимальной очаговой неврологической симптоматикой в виде рефлексов орального автоматизма и вестибулярно-атактических расстройств и негрубой когнитивной дисфункцией.
- Когнитивные нарушения у пациентов с СД 2 типа с признаками хронических расстройств мозгового кровообращения заключаются в ослаблении внимания, снижении темпа психической и речевой активности, нарушении зрительно-пространственных функций и вторичных нарушений памяти. Данные расстройства укладываются в рамки легких когнитивных расстройств нейродинамического характера. Их нарастание при увеличении длительности СД 2 типа происходит независимо от возраста, длительности АГ и показателей липидных нарушений.
- Наличие СД 2 типа ассоциировано с большой частотой выявления диффузного поражения белого вещества головного мозга. Наиболее выраженные изменения отмечаются в области перивентрикулярного белого вещества в виде лейкоареоза и расширения периваскулярных пространств. Прогрессирование поражения белого вещества головного мозга в перивентрикулярных областях у больных с СД 2 типа ассоциировано со снижением темпа психической активности и концентрации внимания.
- Выраженность изменений в веществе головного мозга нарастает с возрастом. Наряду с этим, на состояние мозгового вещества при СД 2 типа оказывают влияние сосудистые факторы (артериальная гипертензия) и метаболические нарушения (хроническая гипергликемия). В патогенезе поражения головного мозга при СД 2 типа определенную роль играет развитие эндотелиальной дисфункции.
- Повышение концентрации молекул сосудистой адгезии может использоваться в качестве биохимического маркера хронического сосудистого поражения головного мозга у пациентов с СД 2 типа.
- Выраженность диффузного поражения белого вещества головного мозга (субкортикальный, перивентрикулярный лейкоареоз, РПВ) ассоциирована с повышением концентрации аутоантител к глияспецифическому белку S-100.
Внедрение результатов работы
Предложенные рекомендации по ранней диагностики когнитивной дисфункции у пациентов с СД 2 типа с признаками хронических расстройств мозгового кровообращения применяются в работе неврологических отделений ГКБ №1 им. Н.И. Пирогова и ГКБ №12 г. Москвы. Полученные результаты работы используются для преподавания студентам, ординаторам, аспирантам.
Апробация работы
Основные положения диссертации доложены на совместной научно-практической конференции коллектива сотрудников кафедры неврологии и нейрохирургии лечебного факультета РГМУ и сотрудников отделений № 12 и 13 ГКБ № 1 от 14.04.2009 г.
Публикации по теме диссертации:
По материалам диссертации опубликовано 6 печатных работ, в том числе, 3 – в ведущих рецензируемых научных журналах, определённых ВАК.
Объем и структура диссертации
Работа изложена на 150 страницах машинописного текста и состоит из введения, обзора литературы, описания материала и методов исследования, результатов собственных наблюдений, корреляционного анализа, а также заключения, выводов, практических рекомендаций и списка литературы, включающего ссылки на 53 отечественных и 287 зарубежных источника. Работа содержит 34 таблицы, 3 рисунка.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Общая характеристика больных
Было обследовано 102 пациента с СД 2 типа в возрасте от 46 до 77 лет (средний возраст 61±7 лет), среди них 26 мужчин, 76 женщин (основная группа) и 21 пациент без диабета, в возрасте от 51 до 70 лет (в среднем 60±6 лет), среди них 5 мужчин, 16 женщин (группа сравнения). Длительность течения заболевания (СД 2 типа) у пациентов в основной группе варьировала от 1 года до 24 лет. Пациенты обеих групп имели высшее образование. Группы были сопоставимы между собой по возрасту и гендерному составу.
Из исследования исключались больные с перенесенным инсультом, деменцией (суммарный балл менее 24 баллов), терминальной стадией соматических заболеваний, полиорганной недостаточностью, воспалительными и травматическими поражениями и новообразованиями ЦНС, психическими заболеваниями, исключающими возможность оценки когнитивных функций, выраженными эмоциональными и поведенческими расстройствами (депрессия, тревога).
Методы исследования
Всем больным было проведено комплексное клинико-неврологическое, нейропсихологическое, лабораторное и инструментальное обследование на базе неврологических отделений ГКБ №1 и отделений ФГУ ЭНЦ.
Клиническо-неврологическое исследование включало структурированный сбор жалоб, анамнестических сведений, осмотр, исследование неврологического статуса.
Лабораторные исследования. Биохимический анализ крови проводился на биохимическом анализаторе «Hitachi» («Boehring Mannheim», Германия) энзиматическим методом по стандартным методикам с использование реагентов производителя. Уровень гликированного гемоглобина HbA1с определялся иммунотурбометрическим методом.
Определение высокочувствительного С-реактивного белка (hs-СРБ) проводилось твердофазным иммуноферментным методом с использованием латексных систем с помощью наборов «Roshe Diagnostics» на аппарате «Hitachi» («Boehring Mannheim», Германия) по методике производителя. Уровень фибриногена оценивали с помощью анализатора гемокоагуляции STA Compact (Diagnostica STAGO, Франция).
Количественное определение уровня молекул адгезии и растворимой формы Е-селектина проводилось методом ELISA с использованием диагностических наборов «Human sICAM (BSM2010», «Human sE-selection (BMS 205)», «Human sVCAM-1 (BMS232)» («Bender MedSystems») по методике производителя.
Аутоантитела к нейроспецифическим антигенам исследовали с помощью твердофазного иммуноанализа при разведениях исследуемых сывороток и сыворотки-страндарта 1:25. Концентрация антигенов для сорбции на планшет составляла 5 мкг/мл. В качестве внутреннего стандарта использовали одну и ту же сыворотку клинически здорового взрослого донора 34 лет, у которого не было признаков соматических, неврологических, эндокринных, инфекционных и воспалительных заболеваний. Уровень аутоантител рассчитывали как отношение оптической плотности исследуемого образца сыворотки крови к оптической плотности сыворотки-стандарта и выражали в относительных единицах.
Инструментральное исследование включало проведение суточного мониторирования АД и МРТ головного мозга.
Суточное мониторирование с определением средних значений систолического АД (САД) и диастолического АД (ДАД) проводилось на аппарате MEDITECH ABPM 04 (Венгрия).
Локализация, характер и выраженность очаговых и диффузных изменений головного мозга исследовались на МР-томографе «Harmony» («Siemens Magnetom Impact», Германия), с напряженностью поля в 1 Тл и следующими диагностическими последовательностями:
- Т1-SE (TR=400мс, ТЕ=12мс, FA=70 град.), сагиттальные срезы толщиной 3 мм, матрица 256Х256 и фронтальные срезы толщиной 3 мм, матрица 256х256;
- T2-SE (TR=4500мс, ТЕ=99мс, FA=180 град.), аксиальные срезы толщиной 3-5 мм, матрица 256Х256
- Flair (TR=9000, TE=114 мс, FA=150 град.), аксиальные срезы толщиной 5 мм, матрица 256Х256.
Качественная оценка результатов МРТ включала выявление очаговых и диффузных изменений интенсивности сигнала от головного мозга. Полуколичественная оценка выявленных изменений проводилась с помощью ряда методик по бальной системе: определение выраженности изменений белого вещества в перивентрикулярных (Liu C.K., Miller B.I., 1992) и субкортикальных областях (Fazekas F, Chawluk J.B, Alavi A. et. al., 1987; Яхно Н.Н., 2001), выраженности РПВ (MacLullich A, Wardlaw J M, Ferguson K J, et al., 2004).
Нейропсихологическое исследование включало тестирование с использованием ряда шкал и тестов. Так как в настоящее время не существует общепринятого набора нейропсихологических тестов для диагностики мягкой когнитивной дисфункции, то были выбраны формализованные скрининговые методики с количественной оценкой полученных результатов, позволяющие оценить основные когнитивные функции (память, внимание, речь, зрительно-пространственные функции и регуляцию произвольной деятельности): Шкала общего ухудшения когнитивных функций (GDS, Reisberg B. et al, 1982), Краткая шкала оценки психического статуса (MMSE, Folstein MF., Folstein SE., McHugh PR., 1975), Батарея лобной дисфункции (Dubois B., Slachevsky A., Litvan I., et al, 2000), тест рисования часов (Lezak MD., 2004), тест «Литеральные ассоциации» (Lezak MD., 2004). Для углубленного изучения когнитивных функций у обследуемых пациентов применялись также более развернутые тесты, которые кроме количественной оценки позволяли провести и качественный анализ выявляемых отклонений (тесты заучивания 10 слов (Лурия А.Р., 2003), тест 12 слов Гробера и Бушке (Grober E., Bushke H., Crystal H. et al., 1988), проба Шульте (Васильева В.А., 1960; Рубинштейн С.Я., 1999). Перед проведением нейропсихологического тестирования всем пациентам предлагались опросники для оценки наличия и выраженности депрессивных симптомов (шкала депрессии Бека, Beck AT., et al, 1961) и оценки уровня ситуационной (реактивной) тревожности (тест Спилбергера-Ханина, 1976)
Статистический анализ
Статистическая обработка полученных результатов проводилась с использованием программы SSPS 13.0. Описательная статистика при нормальном распределении признака (в соответствии с результатами теста Колмогорова-Смирнова) была представлена в виде среднего значения и стандартного отклонения (M±SD). При распределении признака, отличного от нормального, описательная статистика была представлена значениями медианы (Ме) и значениями 25 и 75 процентилей (интерквартильный размах). Для некоторых показателей дополнительно были приведены минимальные и максимальные значения (Maximum, Minimum). Описательная статистика качественных признаков была представлена также в виде абсолютных и относительных частот (процентов). Для сравнения двух независимых групп по одному признаку применялись U-критерий Уитни-Манна, критерий 2, точный критерий Фишера (в случаях малых выборок). Для сравнения двух зависимых групп по одному признаку использовались критерий Вилкоксона и МакНемара (при наличии дихотомических переменных). Сравнение трех независимых групп по одному признаку проводилось методом однофакторного дисперсионного анализа вариаций по Краскелу-Уоллису. Статистически значимыми различия считались при р<0,05. Для выявления взаимосвязи двух признаков применялся непараметрический корреляционный анализ по Спирмену. Для исключения искажающих переменных проводился расчет частной корреляции.
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ
- Результаты клининико-неврологического и биохимического обследования пациентов
Пациенты с СД 2 типа имели более отягощенный сосудистый анамнез (АГ, ИБС) по сравнению с пациентами без диабета. 90,2% больных СД 2 типа имели диагностированную артериальную гипертензию (АГ), 46,1% – ИБС, 5,9% пациентов перенесли инфаркт миокарда. Также пациенты обеих групп значимо различались по значениям ИМТ, уровням HbA1с и триглицеридов. Клинико-лабораторные характеристики пациентов обеих групп представлены в таблице 1.
Таблица 1.
Клинико-лабораторные характеристики пациентов основной группы и группы сравнения
| Клинико-лабораторная характеристика групп | Основная группа (n=102) | Группа сравнения (n=21) |
| Наличие АГ | 92 пациента (90,2%) | 0** |
| Среднее САД, M±SD, мм рт ст | 136±11 | 116±12** |
| Среднее ДАД, M±SD, мм рт ст | 76±8 | 65±4** |
| Длительность АГ, Ме, лет | 11 (7;22) | 0** |
| ИМТ, Ме, кг/м2 | 30 (28;33) | 25 (22;26)** |
| HbA1с, M±SD, % | 8,1±1,5 | 5,7±0,2** |
| Холестерин, M±SD, ммоль/л | 5,9±1 | 5,7±0,8 |
| Триглицериды, M±SD, ммоль/л | 2,0±1,3 | 0,7±0,1* |
| ЛПНП, M±SD, ммоль/л | 4,2±4,3 | 3,5±0,54 |
| ЛПВП, M±SD, ммоль/л | 1,4±0,5 | 2,0±0,6 |
Здесь и далее: ** - различия при уровне значимости р<0,001,
* - различия при уровне значимости р<0,05
Для анализа неврологических и нейропсихологических особенностей поражения головного мозга при различной длительности СД 2 типа все пациенты основной группы были разделены на две подгруппы – с длительностью СД 2 типа менее 5 лет (подгруппа 1) и с длительностью заболевания 5 лет и более (подгруппа 2). Пациенты обеих подгрупп были сопоставимы по полу и возрасту и количеству больных АГ. Для пациентов с более длительным течением СД 2 типа были характерны более высокие уровни ДАД, чаще имели в анамнезе ИБС (таблица 2).
Таблица 2.
Основные клинико-лабораторные характеристики пациентов с различной длительностью СД 2 типа
| Клинико-лабораторная характеристика | Подгруппа 1(n=40) | Подгруппа 2 (n=62) |
| Средний возраст, лет | 60±6 | 63±7 |
| Возраст, максимум-минимум, лет | 46-77 | 48-75 |
| Мужчины/Женщины | 14 (35%)/26 (65%) | 12 (9,4%)/50 (80,6%) |
| Длительность АГ, M±SD, лет | 11,5±10,3 | 17,2±11* |
| Среднее САД, M±SD, мм рт ст. | 138±12 | 134±11 |
| Среднее ДАД, мм рт ст. | 79±8 | 74±8* |
| Инфаркт миокарда в анамнезе | 3 (7,5%) | 3 (4,9%) |
| ИБС | 9 (22,5%) | 38 (62,3%)** |
| ИМТ; Ме, кг/м2 | 30 (28; 36) | 30 (27; 32) |
| Гликированный гемоглобин HbA1с, M±SD, % | 7,9%±1,7 | 8,3%±1,3* |
| Холестерин, M±SD, ммоль/л | 5,8±1,0 | 6,0±0,99 |
| Триглицериды, M±SD, ммоль/л | 1,9±1,5 | 2,1±1,6 |
| ЛПОНП, M±SD, ммоль/л | 3,8±0,9 | 4,4±5,4 |
| ЛПВП, M±SD, ммоль/л | 1,3±0,35 | 1,5±0,5 |
Жалобы и особенности неврологического статуса у пациентов в основной группе и группе сравнения.
Пациенты обеих групп предъявляли жалобы на ухудшение памяти. При более тщательном расспросе было выявлено, что под ухудшением памяти больные понимали собственно забывчивость, рассеянность, трудности подбора слов при разговоре, утомляемость, снижение работоспособности. Также пациенты предъявляли жалобы на головную боль, головокружение, несистемного характера, шум в голове.
При исследовании неврологического статуса у пациентов обеих групп выявлялась минимальная очаговая неврологическая симптоматика в виде симптомов орального автоматизма и вестибулярно-атактических расстройств (неустойчивость в позе Ромберга, неточность при выполнении координаторных проб).
При увеличении длительности СД 2 типа пациенты чаще предъявляли жалобы на рассеянность (точный критерий Фишера, р=0,045), трудности подбора слов в разговоре (точный критерий Фишера, р=0,023). Также у пациентов с большей длительностью СД 2 типа выявлялась более выраженная минимальная очаговая неврологическая симптоматики в виде вестибулярно-атактических расстройств, чем у пациентов с меньшей длительностью заболевания (точный критерий Фишера, р=0,021).
Основные жалобы и очаговые неврологические симптомы у пациентов различных групп представлены в таблице 3.
Таблица 3.
Жалобы и очаговые неврологические симптомы у обследованных пациентов
| Клиническая характеристика групп | Подгруппа 1 (n=40) | Подгруппа 2 (n=62) | Группа сравнения (n=21) |
| Нарушения памяти | 18 (45,5%) | 42 (67,3%) | 7 (33,3%)* |
| Рассеянность | 17 (41,4%) | 38 (62,6 %) * | 8 (39,6)% |
| Трудности подбора слов при разговоре | 14 (34,4%) | 39 (65%)* | 3 (15%)* |
| Повышенная утомляемость и снижение работоспособности | 11 (27,3%) | 13 (22,4%) | 11 (52,4%)* |
| Головная боль | 6 (15,6%) | 19 (31,3%) | 14 (66,7%)** |
| Головокружение, несистемного характера | 9 (21,9%) | 22 (37,5%) | 4 (19)% |
| Шум в голове | 4 (9,4)% | 5 (8,3%) | 0 |
| Симптомы орального автоматизма | 10 (25%) | 26 (42,9%) | 6 (29%) |
| Вестибулярно-атактические расстройства | 15 (37,5%) | 41 (68,4%) * | 8 (38,1)% |
- Результаты нейропсихологического тестирования пациентов
Перед проведением нейропсихологического тестирования пациенты обеих групп выполняли тесты на наличие и выраженность депрессивных симптомов (шкала депрессии Бека) и оценку уровня ситуационной (реактивной) тревожности (тест Спилбербера-Ханина) для исключения «дистимического» типа когнитивных расстройств. Выраженных депрессивных расстройств выявлено не было. У большинства пациентов выявлялся умеренный уровень ситуационной тревожности (таблица 4).
Таблица 4.
Уровень депрессии и тревоги у обследованных пациентов
| Название теста | Интерпретация теста | Подгруппа 1(n=40) | Подгруппа 2 (n=62) | Группа сравнения (n=21) |
| Шкала депрессии Бека | 0 – 9 баллов (отсутствие депрессии) | 35 (87,5%) | 51 (82,3%) | 19 (90,5%) |
| 10 – 15 баллов (субдепрессия) | 5 (12,5%) | 11 (17,7%) | 2 (9,5%) | |
| Шкала Спилберга-Ханина | Низкий уровень РА | 1 (2,5%) | 0 | 0 |
| Умеренный уровень РА | 26 (65%) | 47 (75,8%) | 15 (71,4%) | |
| Высокий уровень РА | 13 (32,5%) | 15 (24,2%) | 6 (28,6%) |
По результатам тестирования по шкале Общего ухудшения когнитивных функций (GDS) у пациентов не выявлялось значимого когнитивного дефицита, однако больные с длительно текущим СД 2 типа в большем числе случаев соответствовали 3 стадии по GDS, чем больные с меньшей длительностью заболевания. Также не было выявлено значимых отклонений когнитивных функций у пациентов различных групп по результатам тестов MMSE и Батареи лобной дисфункции.
Статистически значимые отличия в группах были получены при проведении теста на литеральные ассоциации, теста рисования часов, пробы Шульте. Было выявлено, что пациенты с СД 2 типа в целом за минуту называют меньшее количество слов на букву «С», чем пациенты группы сравнения, при увеличении длительности заболевания больные с диабетом хуже выполняли тест рисования часов и медленнее – пробу Шульте.
Также у пациентов с СД 2 типа выявлялись нарушения памяти. В тесте заучивания 10 слов у больных диабетом чаще выявлялись легкие и умеренные нарушения памяти, а также ослабление внимания, чем у пациентов группы сравнения. С увеличением длительности СД 2 типа отмечалось нарастание выраженности расстройств памяти, ослабление внимание значимо не нарастало.
Тест Гробера и Бушке (заучивание 12 слов с использованием семантической подсказки; воспроизведение непосредственное и отсроченное, с подсказкой и без подсказки) позволил разделить нарушения памяти у пациентов обеих групп на амнестические и неамнестические. По результатам данного теста было выявлено, что нарушения памяти чаще отмечались у пациентов с диабетом, при этом в большем проценте случаев они носили неамнестический характер. Результаты нейропсихологических тестов у пациентов различных групп приведены в таблице 5.
Таблица 5.
Результаты нейропсихологического тестирования обследованных пациентов
| Название теста | Интерпретация теста | Подгруппа 1(n=40) | Подгруппа 2 (n=62) | Группа сравнения (n=21) |
| GDS | Баллы, соответствующие тяжести когнитивного дефицита, M±SD | 1,7±0,6 | 2±0,4** | 1,8±0,6 |
| MMSE | Средний балл, M±SD | 28±2 | 27±2 | 28±1 |
| БЛД | Средний балл, M±SD | 16±2 | 16±2 | 16±1 |
| Литеральные ассоциации | Количество пациентов, назвавших менее 10 слов за минуту | 11 (27,5%) | 21 (33,9%) | 2 (9,5%)* |
| Количество пациентов, назвавших более 10 слов за минуту | 29 (72,5%) | 41 (66,1%) | 19 (90,5%)* | |
| Тест рисования часов | Средний балл, M±SD | 8±1 балла | 7±2 балла * | 8±2 балла * |
| Проба Шульте | Среднее время выполнения теста, M±SD | 47,1±11,5 секунд | 52,9±13,5 секунд * | 42,8±8,3 секунды * |
| Тест заучивания 10 слов, память | Нарушений памяти не выявлено (9/10 слов к третьему воспроизведению) | 10 (26,3%) | 8 (13,8%) * | 14 (66,7%) ** |
| Легкие нарушения памяти (8/7 слов к третьему воспроизведению) | 20 (52,6%) | 26 (44,8%) * | 7 (33,3%) ** | |
| Умеренные нарушения памяти (5/6 слов к третьему воспроизведению) | 8 (21,1%) | 22 (37,9%) * | - ** | |
| Выраженные нарушения памяти (3/4 слов к третьему воспроизведению) | - | 2 (3,4%) * | - ** | |
| Тест заучивания 10 слов, внимание | Ослабление внимания | 27 (67,5%) | 45 (72,6%) | 7 (33,3%)* |
| Нарушений внимания не выявлено | 13 (32,5%) | 17 (27,4%) | 14 (66,7%)* | |
| Тест Гробера и Бушке | Нет нарушений памяти | 14 (66,7%) ** | 9 (22,5%) | 15 (24,2%) |
| Неамнестические нарушения | 7 (33,3%) ** | 29 (72,5%) | 42 (67,7%) | |
| Амнестические нарушения | - ** | 2 (5%) | 5 (8,1%) |
Нейропсихологическое исследование пациентов с СД 2 типа и пациентов без диабета, сопоставимых по полу и возрасту, показало, что у пациентов с СД 2 типа достоверно хуже выполняют пробу Шульте, тест «Литеральные ассоциации», т. е. преимущественно имеются нарушения внимания, психического темпа, беглости речи. Также у пациентов с СД 2 типа чаще выявляются расстройства зрительно-пространственных функций (по результатам теста рисования часов), по сравнению с пациентами, не страдающими СД 2 типа, и нарушения памяти. Последние в большинстве случаев носят вторичный характер, в результате ослабления внимания. Выявленные изменения соответствуют легким когнитивным нарушениям нейродинамического характера.
С увеличением длительности заболевания нейродинамические нарушения нарастают, в основном за счет замедления скорости мыслительных процессов; при этом ослабление внимания и снижение темпа речевой активности изменяются незначительно. Кроме этого, при длительности СД 2 типа 5 и более лет усиливаются зрительно-пространственные нарушения и мнестические расстройства.
- Нейровизуализационные феномены хронических расстройств мозгового кровообращения у пациентов с СД 2 типа.
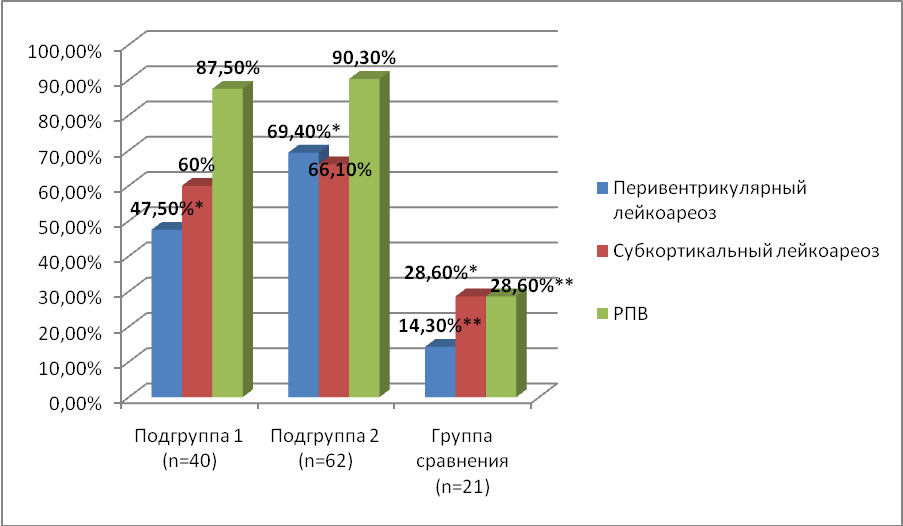
Рисунок 1. Выявленные изменения вещества головного мозга по данным МРТ у обследованных пациентов.
У пациентов обеих групп выявлялось поражение белого вещества головного мозга в виде лейкоареоза (субкортикального и перивентрикулярного) и расширения перивентрикулярных пространств. «Немые» инфаркты были выявлены только у двух пациентов основной группы, локализовались они в области мозжечка.
Диффузные изменения белого вещества головного мозга выявлялись чаще у пациентов с СД 2 типа, по сравнению с пациентами без диабета. Различия в частоте выявления лейкоареоза и частоте выявления расширения периваскулярных пространств между двумя группами были статистически значимы. У больных с длительным течением заболевания чаще выявлялись изменения белого вещества в перивентрикулярных областях (рисунок 1).
Группы пациентов сравнивались по медианам шкал оценки перивентрикулярного, субкортикального лейкоареоза и РПВ. Выраженность изменений белого вещества головного мозга отличалась в основной и группе сравнения. Степень выраженности перивентрикулярного лейкоареоза у большинства пациентов основной группы достигала 1 балла, что соответствовало ограниченным передними или задними областями изменениям перивентрикулярного белого вещества. Такого рода изменения рядом исследователей рассматриваются как вариант возрастной нормы (Fazekas F., et al, 1993; Schmidt R. et al, 1995). В то же время в группе сравнения изменения в перивентрикулярном белом веществе не достигали такой выраженности, как в группе пациентов с СД 2 типа. Выраженность перивентрикулярного лейкоареоза в основной группе была статистически значимо больше, чем в группе сравнения, сопоставимой по возрасту и полу.
Изменения белого вещества головного мозга в виде субкортикального лейкоареоза также не были сильно выражены. У большинства пациентов основной и группы сравнения выявлялись менее 5 мелких, диаметром до 5 мм, локальных очагов или менее 2 крупных, диаметром 5-10 мм, локальных очагов. Различия между обеими группами в количестве и размерах выявляемых очагов в субкортикальном белом веществе не были статистически значимыми.
Наиболее значимыми оказались различия в обеих группах по степени выраженности расширения периваскулярных пространств. Так, в группе пациентов с СД 2 типа наиболее часто выявлялось от 10 до 20 гиперинтенсивных на Т2 очагов, диаметром 1-2 мм, расположенных в соответствии с ходом перфорирующих артерий, перпендикулярно поверхности мозга. В группе сравнения такие очаги выявлялись наиболее часто в количестве менее 10.
У пациентов с длительным течением СД 2 типа перивентрикулярный лейкоареоз был более выражен. Статистически значимых отличий в выраженности субкортикального лейкоареоза и расширения перивентрикулярных пространств у пациентов с различной длительностью СД 2 типа получено не было (рисунок 2).
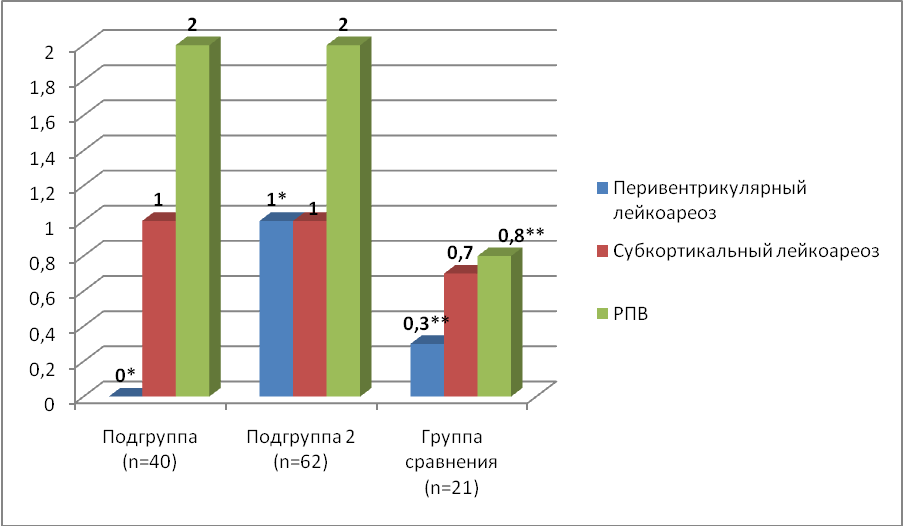
Рисунок 2. Выраженность в баллах изменений головного мозга по данным МРТ у обследованных пациентов.
При проведении корреляционного анализа по методу Спирмена была выявлена умеренная прямая корреляционная связь между выраженностью перивентрикулярного лейкоареоза и нарушением памяти по результатам теста заучивания 10 слов (метод Спирмена, r=0,246, р=0,007, N 117) и временем выполнения пробы Шульте (метод Спирмена, r=0,285, р=0,002, N 121), а также прямая статистически значимая связь между выраженностью субкортикального лейкоареоза и нарушениями памяти (метод Спирмена, r=0,263, р=0,004, N 117).
На основании проведенного корреляционного анализа по Спирмену было установлено, что прогрессирование изменений белого вещества головного мозга клинически выражается в нарастании когнитивной дисфункции в виде ухудшения памяти, внимания, психического темпа. Проведенное исследование позволило уточнить факторы патогенеза поражения вещества головного мозга при СД 2 типа. Прогрессирование перивентрикулярного лейкоареоза зависит, в основном, от наличия и компенсации артериальной гипертензии. Умеренная прямая корреляционная связь была выявлена между выраженностью перивентрикулярного лейкоареоза и длительностью АГ (метод Спирмена,r=0,385, р<0,001, N 119) и средним САД (метод Спирмена, r=0,385, р<0,001, N 119), средним ДАД (метод Спирмена, r=0,196, р=0,033, N 119). На прогрессирование субкортикального лейкоареоза, главным образом, оказывает влияние возраст (метод Спирмена, r= 0,285, р=0,001, N 123), а не АГ или метаболические нарушения СД 2 типа (хроническая гипергликемия). В патогенезе прогрессирования расширения периваскулярных пространств при СД 2 типа, играют роль и сосудистые факторы (артериальная гипертензия) (метод Спирмена, r= 0,353, р<0,001, N 119), и дисметаболические нарушения (хроническая гипергликемия) (метод Спирмена, r= 0,33, р<0,001, N 115).
- Маркеры эндотелиальной дисфункции у пациентов с СД 2 типа
Анализировались показатель острой фазы воспаления в основной и группе сравнения – С-реактивный белок. Статистически значимые отличия в уровне С-реактивного белка были выявлены только при сопоставлении группы сравнения и группы с длительностью СД 5 и более лет.
Средний уровень С-реактивного белка в группе с СД 2 типа с длительностью заболевания 5 и более лет составил 4,34±3,42 ммоль/л, в группе сравнения – 1,84±1,8 ммоль/л (U-критерий Уитни-Манна, р=0,009).
У больных с СД 2 типа проводилось исследование крови на содержание молекул клеточной и сосудистой адгезии и Е-селектина. С увеличением длительности течения заболевания отмечалось повышение концентрации VCAM-1 (таблица 6).
Таблица 6.
Концентрации молекул адгезии у пациентов с различной длительностью СД 2 типа
| Маркеры эндотелиальной дисфункции | Подгруппа 1(n=40) | Подгруппа 2 (n=62) |
| Молекулы клеточной адгезии (ICAM-1), M±SD | 420,6±134,2 нг/мл | 473,1±204,2 нг/мл |
| Молекулы сосудистой адгезии (VCAM-1), M±SD | 399,48±135,96 нг/мл | 528,36±125,8 нг/мл * |
| E-селектин, M±SD | 65,6±50,6 нг/мл | 52,3±29,1 нг/мл |
Выявленные более высокие показатели концентраций молекул сосудистой адгезии у пациентов с длительностью СД 2 типа более 5 лет могут свидетельствовать о нарастании эндотелиальной дисфункции при длительно текущем диабете, что может иметь значение в патогенезе поражения вещества головного мозга при этом заболевании.
- Исследование биохимических маркеров повреждения мозговой ткани у пациентов с СД 2 типа
Проводилось определение аутоантител к мозгоспецифическим антигенам белку S-100, глиофибриллярному кислому протеину (GFAP).
Среднее значение уровня антител к S-100 в основной группе составило 135,17±63,5 нг/мл, в группе сравнения – 143,3±98,8 нг/мл. Различия между обеими группами не были статистически значимыми (U-критерий Уитни-Манна, р=0,3).
Среднее значение уровня антител к кислому глияфибриллярному кислому протеину в основной группе составило 0,39±0,98 нг/мл, в группе сравнения – 0,28±0.14 нг/мл. Различия между обеими группами не были статистически значимыми (U-критерий Уитни-Манна, р=0,288).
Учитывая отсутствие статистически значимой разницы в выявленных титрах аутоантител в группах пациентов с СД 2 типа и без этого заболевания, проводилось сравнение их концентраций у пациентов с различной длительностью СД 2 типа с аналогичными показателями у пациентов группы контроля. Различия по группам анализировались методом однофакторного дисперсионного анализа Краскела-Уоллиса. Статистически значимых отличий между группами по титрам аутоантител к мозгоспецифическим антигенам выявлено не было.
Таким образом, аутоантитела к мозгоспецифическим нейроглиальным антигенам выявлялись и у пациентов с СД 2 типа, и у пациентов без диабета, однако статистически значимых различий в их уровнях в основной и контрольной группах выявлено не было. Также не отмечалось статистически значимого нарастания титра мозгоспецифических аутоантител при увеличении длительности СД 2 типа.
В то же время выявление антиглиальных аутоантител к белку S-100 и глиофибриллярному кислому белку может отражать наличие хронической сосудистой патологии головного мозга у обследованных пациентов.
На основании корреляционного анализа по Спирмену установлено, что повышение концентраций аутоантител к белку S-100 ассоциировано с выраженностью поражения белого вещества головного мозга (лейкоареозом и расширением периваскулярных пространств). Выявлены прямые статистически значимые корреляционные связи концентрации аутоантител к глияспецифическому белку S-100 с выраженностью перивентрикулярного лейкоареоза (метод Спирмена, r=0,324, р=0,001, N 103), выраженностью субкортикального лейкоареоза (метод Спирмена, r=0,198, р=0,045, N 103), степенью расширения периваскулярных пространств (метод Спирмена, r=0,208, р=0,035, N 103).
ВЫВОДЫ
- Ранними проявлениями хронических расстройств мозгового кровообращения у пациентов с СД 2 типа в отсутствии выраженной очаговой неврологической симптоматики могут являться легкие когнитивные нарушения, выявление которых необходимо, в связи с повышенным риском их прогрессирования до стадии тяжелого когнитивного дефицита.
- Когнитивные расстройства у пациентов с СД 2 типа без инсульта в анамнезе заключаются в ослаблении внимания, снижении темпа психической и речевой активности, нарушении зрительно-пространственных функций и вторичных нарушений памяти. Данные нарушения укладываются в рамки легких когнитивных расстройств нейродинамического характера. При увеличении длительности течения СД 2 типа отмечается нарастание замедления скорости психомоторных реакций, зрительно-пространственных нарушений и снижения памяти, при этом ухудшение когнитивных функций происходит независимо от возраста и длительности АГ и показателей дислипидемических нарушений.
- Наличие СД 2 типа ассоциировано с большей частотой выявления диффузного поражения белого вещества головного мозга. Наиболее выраженные изменения головного мозга у больных с СД 2 типа выявляются в перивентрикулярном веществе и в области периваскулярных пространств. С увеличением длительности СД 2 типа отмечается прогрессирование изменений в перивентрикулярном белом веществе головного мозга. В прогрессировании перивентрикулярного лейкоареоза при длительно текущем СД 2 типа наибольшую роль играет АГ. Выраженность субкортикального лейкоареоза и расширения периваскулярных пространств с увеличением длительности СД 2 типа нарастает незначительно. Прогрессирование субкортикального лейкоареоза связано, главным образом, со старением; а в патогенезе прогрессирования расширения периваскулярных пространств при СД 2 типа, играют роль и сосудистые факторы (АГ), и дисметаболические нарушения (хроническая гипергликемия). Прогрессирование диффузных изменений белого вещества головного мозга ассоциировано с нарастанием нарушений памяти, внимания, психического темпа.
- С увеличением длительности СД 2 типа отмечается повышение концентрации молекул сосудистой адгезии, что может отражать нарастание эндотелиальной дисфункции, играющей роль в патогенезе поражения головного мозга.
- Для пациентов с СД 2 типа и без диабета, имеющих признаки хронической сосудистой патологии головного мозга характерно выявление антиглиальных аутоантител к белку S-100 и глиофибриллярному кислому белку. Повышение уровня аутоантител к белку S-100 ассоциировано с выраженностью лейкоареоза и степенью расширения периваскулярных пространств головного мозга.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- При наличии активных жалоб пациентов с СД 2 типа на нарушения памяти или других когнитивных функций необходимо проведение нейропсихологического тестирования для раннего выявления когнитивной дисфункции.
- Использованные в работе шкалы и тесты являются простыми в применении и эффективными в отношении выявления негрубых когнитивных расстройств, позволяют оценить когнитивные функции в полном объеме и могут быть рекомендованы для использования при проведении нейропсихологического исследования у больных СД 2 типа.
- Применение методов нейровизуализации (МРТ) необходимо у пациентов с СД 2 типа при выявлении когнитивных нарушений для установления возможных причин развития когнитивной дисфункции.
- Определение концентрации молекул сосудистой адгезии может быть рекомендовано в качестве биохимического маркера сосудистого поражения головного мозга у больных СД 2 типа.
- Выявление патогенетической роли артериальной гипертензии, липидных нарушений, эндотелиальной дисфункции в развитии когнитивных расстройств при СД 2 типа позволяет рекомендовать применение сосудистых препаратов в схемах лечения пациентов с диабетом.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Чугунова Л.А., Тарасов Е.В., Баcсэ Д.А., Михайлова Н.А., Семенова И.В., Князева А.П., Дроздова Е.Н., Камчатнов П.Р., Владимирова В.П., Воронцов А.В., Чугунов А.В., Шестакова М.В. Факторы сосудистого риска, когнитивные расстройства и изменения картины МРТ головного мозга у больных сахарным диабетом 2 типа// Сахарный диабет. – 2006. - № 4. – с. 24-28.
- Камчатнов П.Р., Чугунов А.В., Чугунова Л.Ю., Семенова И.В., Бассэ Д.А., Михайлова Н.А., Умарова Х.Я.Когнитивные функции у больных сахарным диабетом 2 типа// Журнал неврологии и психиатрии им. С.С. Корсакова. Инсульт. Мат 11 Всерос. Конгресса. – 2007. - с. 371.
- Чугунова Л.А., Чугунов А.В., Бассэ Д.А., Михайлова Н.А., Семенова И.В., Камчатнов П.Р., Шестакова М.В. Влияние нарушения метаболизма глюкозы на течение и исход острого ишемического инсульта// Сахарный диабет. – 2007. - № 4. – с. 18-21.
- Камчатнов П.Р., А.В. Чугунов, Д.А. Бассэ, Н.А. Михайлова,Х.Я. Умарова, И.В. Семенова, Л.А. Чугунова. Нарушение углеводного обмена у больных с острым ишемическим инсультом// Клиницист. – 2007. - № 6. – с. 21-26.
- Камчатнов П.Р., Л.А.Чугунова, И.В.Семенова, Д.А. Бассэ, Х.Я. Умарова, А.В. Чугунов. Хронические расстройства мозгового кровообращения у больных сахарным диабетом 2-го типа// Клиницист. – 2007. - № 2. – с. 9-15.
- Камчатнов П.Р., Каралкин А.В., Чугунов А.В., Кабанов А.А., Бассэ Д.А., Михайлова Н.А., Умарова Х.Я., Бойко А.Н. Возможности патогенетической терапии больных сахарным диабетом 2-го типа и дисциркуляторной энцефалопатией// Журнал неврологии и психиатрии им. С.С. Корсакова. - 2008. - № 3. – с. 18-24.
Список сокращений:
АГ
- Артериальная гипертензия
АД
- Артериальное давление
БЛД
- Батарея лобной дисфункции
ДАД
- Диастолическое артериальное давлении
ИБС
- Ишемическая болезнь сердца
ИМТ
- Индекс массы тела
ЛПВП
- Липопротеиды высокой плотности
ЛПНП
- Липопротеиды низкой плотности
Ме
- Медиана
МРТ
- Магнитно-резонансная томография
РПВ
- Расширение периваскулярных пространств
САД
- Систолическое артериальное давление
СД 2 типа
- Сахарный диабет 2 типа
УКР
- Умеренные когнитивные расстройства
ЦНС
hs-CРБ
- Центральная нервная система
- С-реактивный белок
ICAM-
- Молекулы клеточной адгезии
GDS
- Шкала общего ухудшения когнитивных функций
GFAP
- Глиофибриллярный кислый протеин
HbA1с
- Гликированный гемоглобин
MMSE
- Краткая шкала оценки психического статуса
VCAM-1
- Молекулы сосудистой адгезии

