Поздние сердечно-сосудистые осложнения химиолучевой терапии лимфогранулематоза
На правах рукописи
Авдеев Юрий Владимирович
ПОЗДНИЕ СЕРДЕЧНО-СОСУДИСТЫЕ
ОСЛОЖНЕНИЯ ХИМИОЛУЧЕВОЙ ТЕРАПИИ ЛИМФОГРАНУЛЕМАТОЗА
14.01.05 – кардиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва - 2010
Работа выполнена в ГОУ ВПО Московская медицинская академия
им. И.М. Сеченова Росздрава
Научный руководитель:
Доктор медицинских наук, профессор Сыркин Абрам Львович
Официальные оппоненты:
Доктор медицинских наук, профессор Сизова Жанна Михайловна
Доктор медицинских наук, профессор Барт Борис Яковлевич
Ведущая организация:
Российский кардиологический научно-производственный комплекс Росмедтехнологий
Защита диссертации состоится «__»_____________ 2010 в «__» часов на заседании диссертационного совета Д.208.040.05 при ГОУ ВПО Московская медицинская академия им. И.М. Сеченова Росздрава (119991), г. Москва, ул. Трубецкая, д.8, стр. 2
С диссертацией можно ознакомиться в библиотеке Московской медицинской академии им. И.М. Сеченова (117998, Москва, Нахимовский проспект, д.49).
Автореферат разослан «__»____________2010 г.
Ученый секретарь
диссертационного совета,
доктор медицинских наук,
профессор Волчкова Елена Васильевна
АКТУАЛЬНОСТЬ РАБОТЫ
Заболеваемость лимфогранулематозом (болезнью Ходжкина) в России составляет 2-4 на 100 000 человек. Благодаря внедрению высокоэффективных схем химио- и лучевой терапии за последние 40 лет достигнуты значительные успехи в лечении этой опухоли, и 5-летняя выживаемость возросла с 40% (1960-1963гг.) до 86% и более (1996-2004гг.). Ожидаемая продолжительность жизни после излечения – высокая, поскольку лимфогранулематозом зачастую заболевают в молодом возрасте. Так, в 10-15% случаев заболевание наблюдается у лиц моложе 16 лет, еще один пик заболеваемости приходится на 25 - 30 лет [V. Diehl, 1996]. Таким образом, осложнения лечения могут наблюдаться в весьма отдаленные сроки после его окончания.
О влиянии химиолучевой терапии (ХЛТ) на сердечно-сосудистую систему известно с 70-х годов [Lefrak E.A., 1973]. Наиболее хорошо изучена дозозависимая кардиотоксичность метаболитов антрациклиновых антибиотиков [Kremer L., 2001], проявляющаяся как правило уже в ходе лечения или в первые месяцы и годы после его окончания.
При лимфогранулематозе с поражением внутригрудных лимфоузлов дополнительным фактором, потенциально патогенным для сердца, является облучение средостения. Наиболее распространенным из ранних клинически значимых кардиальных осложнений лучевой терапии является выпотной перикардит. Поражения коронарных артерий, клапанов, констрикция перикарда и хроническая сердечная недостаточность (ХСН), обусловленные прогрессирующими склеротическими изменениями всех структур сердца, дебютируют значительно позже [Berthe M., 2003]. Таким образом, с поздними осложнениями сталкиваются в основном терапевты и кардиологи, незнакомые с этой патологией. Своевременной диагностике и раннему выявлению таких осложнений препятствуют отсутствие диспансерного наблюдения за пациентами, снятыми с онкологического учета. Рекомендации по кардиологическому обследованию данного контингента пациентов не разработаны.
В отечественной литературе нет данных о распространенности поздних сердечно-сосудистых осложнений у пациентов, леченных с применением современных режимов ХЛТ, более щадящих по сравнению с применявшимися в 70х - 80х годах 20века. Зарубежные работы посвящены в основном влиянию ХЛТ на риск инфаркта миокарда и реже – ХСН [P. Aleman, 2007]. Имеются единичные исследования клапанных поражений [M. J. Adams, 2004], однако большинство работ выполнено на малых группах пациентов, леченных с применением «старых» методик, и обследованных без применения современных методов диагностики сердечно-сосудистых заболеваний.
Наименее изученными остаются бессимптомные пациенты и пациенты со стертой неспецифической симптоматикой. Многие больные, излеченные от онкологических заболеваний, предъявляют неспецифические жалобы (на слабость, утомляемость, одышку, снижение переносимости нагрузок), которые некоторые авторы связывают с патологией легких, щитовидной железы, воспалительным синдромом [P. Heidenreich, 2007]. Роль сердечно-сосудистой патологии в развитии этих симптомов, как и распространенность доклинических изменений сердца, не изучена.
В связи с этим целью исследования явилось:
изучить поздние сердечно-сосудистые осложнения химиолучевой терапии лимфогранулематоза с поражением внутригрудных лимфатических узлов.
Задачи исследования:
- Изучить распространенность сердечно-сосудистых осложнений через 5 и более лет после химиолучевой терапии лимфогранулематоза с поражением внутригрудных лимфоузлов.
- Выявить особенности поражения сердца в отдаленные сроки после химиолучевой терапии.
- Определить предикторы развития поздних сердечно-сосудистых осложнений химиолучевой терапии.
- Изучить связь снижения толерантности к нагрузке и тахикардии с поражением сердца у малосимптомных пациентов без значимой ХСН.
Научная новизна:
Впервые было проведено исследование распространенности и типов поздних сердечно-сосудистых осложнений ХЛТ лимфогранулематоза у пациентов, получавших лечение по используемым в настоящее время протоколам, с применением современных методов визуализации сердца и функциональной диагностики, включая эргоспирометрию и тканевую миокардиальную допплерэхокардиографию (ТД).
Впервые выявлены особенности изменений сердца в отдаленные сроки после ХЛТ с облучением средостения: тенденция к уменьшению объема левого желудочка (ЛЖ), отсутствие признаков ремоделирования левых отделов сердца у пациентов с клапанными пороками, систолической дисфункцией ЛЖ и ХСН.
У малосимптомных пациентов впервые описана связь неспецифических жалоб, снижения толерантности к нагрузке и тахикардии с рестриктивными изменениями миокарда.
Впервые установлено, что у лиц до 45 лет проведение ХЛТ в более старшем возрасте увеличивает риск развития сердечно-сосудистых осложнений в отдаленные сроки.
Практическая значимость исследования:
В работе выявлена высокая распространенность патологии сердечно-сосудистой системы в отдаленные сроки после химиолучевой терапии лимфогранулематоза с облучением средостения. Это определяет необходимость разработки системы динамического наблюдения за данным контингентом пациентов не только онкологами, но и кардиологами.
Продемонстрировано повышение риска клинически значимой сердечной патологии, в первую очередь – клапанных поражений, по мере увеличения срока, прошедшего после ХЛТ. Это указывает на необходимость пожизненного контроля состояния пациентов и имеет существенное значение для профилактики инфекционного эндокардита.
Выявлены предикторы поздних сердечно-сосудистых осложнений химиолучевой терапии. Показано, что с учетом факторов риска кардиологическому обследованию в первую очередь подлежат пациенты, получавшие лечение в возрасте старше 19 лет, в суммарной дозе на средостение от 40 Гр и более, не менее 8 лет назад, а также имеющие любые, в том числе неспецифические симптомы.
У данного контингента пациентов установлена связь тахикардии с рестриктивными изменениями сердца. В связи с этим назначение ритм-урежающей терапии может сопровождаться клинически значимым снижением сердечного выброса, поэтому оно должно быть обоснованным и требует особой осторожности.
Положения, выносимые на защиту:
1. У большинства пациентов (84,5%) в отдаленные сроки после химиолучевой терапии с облучением средостения по поводу лимфогранулематоза выявляются патологические изменения сердца, включающие поражения всех его структур.
2. Патология сердца после ХЛТ имеет особенности, обусловленные развитием рестриктивных изменений: у больных с систолической дисфункцией, клапанными поражениями и ХСН отсутствуют признаки компенсаторного ремоделирования ЛЖ и увеличения левого предсердия (ЛП).
3. Риск поздних сердечно-сосудистых осложнений у лиц до 45 лет возрастает при увеличении суммарной облучающей дозы (СОД) на средостение, возраста окончания ХЛТ и времени, прошедшего после ее окончания.
4. Неспецифические симптомы (одышка, утомляемость, тахикардия) и снижение толерантности к нагрузке при отсутствии клинически значимой ХСН ассоциированы с признаками рестриктивного поражения сердца (уменьшение объема ЛЖ, диастолическая дисфункция).
Апробация работы. Проведена 18 марта 2009 года на заседании кафедры профилактической и неотложной кардиологии ФППОВ Московской медицинской академии им. И.М. Сеченова
Публикации. По теме диссертации опубликовано 6 печатных работ.
Объем и структура диссертации. Диссертация изложена на 116 страницах машинописного текста и состоит из введения, четырех глав, заключения, выводов, практических рекомендаций, библиографического указателя литературы, включающего 105 источников (12 отечественных и 93 зарубежных). Диссертация иллюстрирована 29 таблицами, 9 рисунками.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследование, проведенное на базе Клиники кардиологии ММА им. И.М. Сеченова, включен 71 пациент.
Критерии включения в исследование:
1 Мужской или женский пол.
2 Возраст от 18 лет до 50 лет.
3 ХЛТ по поводу лимфогранулематоза с облучением лимфоузлов средостения, завершенная не менее 5 лет назад.
4 Стойкая ремиссия лимфогранулематоза (не менее 5 лет без рецидивов).
5 Согласие пациента на участие в обследовании
Критерии исключения из исследования:
1 Указания на наличие любой сердечно-сосудистой патологии до начала ХЛТ.
2 Рецидив лимфогранулематоза или новое онкологическое заболевание
3 Туберкулез, ВИЧ-инфекция и другие заболевания бактериальной и вирусной этиологии.
4 Психические нарушения, препятствующие проведению исследования
5 Злоупотребление алкоголем в течение последнего года
Отбор и пациентов. От врачей-онкологов были получены сведения о 187 пациентах, последовательно проходивших лечение с 1992 по 2002 год в Российском научном центре рентгенорадиологии, Гематологическом научном центре РАМН, Российском онкологическом научном центре им. Н.Н.Блохина РАМН, и удовлетворявших критериям включения в исследование. Удалось проследить за исходами лечения 143 пациентов. Было установлено, что 23 из них к моменту исследования умерли от онкологических заболеваний (рецидив лимфогранулематоза либо другая опухоль). 109 человек опрошены по телефону, из них 49 не предъявляли жалоб и отказались от обследования. 60 пациентов согласились участвовать, и были обследованы амбулаторно. Еще 11 пациентов, получавших ХЛТ с 1978 по 2002г., госпитализированы в Клинику кардиологии целенаправленно в связи с клиническими проявлениями ХСН. У всех лиц, включенных в исследование, при контрольных обследованиях онкологами констатировалась ремиссия основного заболевания.
Характеристика пациентов. В исследование включен 71 пациент, 44 мужчины и 27 женщин, в возрасте от 18 до 49 лет (в среднем 30,4±7,5 лет), получавших ХЛТ по поводу лимфогранулематоза 2-4 стадий с поражением внутригрудных лимфоузлов в период с 1978 по 2002г. и имевших стойкую ремиссию заболевания не менее 5 лет. Возраст пациентов на момент начала ХЛТ составлял от 8 до 40лет (в среднем 20,7±6,7лет), от окончания лечения прошло от 5 до 26 лет (в среднем 8,8±4,6лет).
Химиотерапия проводилась по следующим схемам: ABVD – у 18,3%, COPP+ABVD – у 45,1%, COPP/MOPP – у 16,9%, BEACOPP - у 8,6%, OPPA+COPP+DEXABEAM – у 5,7%, STANFORD V – у 4,2% больных, в 1 случае схема неизвестна. Доксорубицин или другие антрациклиновые производные получали 58 (81,7%) пациентов. Суммарные дозы доксорубицина составляли 223±50,7 мг/м2.
Суммарные облучающие дозы (СОД) на средостение составляли от 20 до 56Гр в среднем – 38,2±7,0, СОД выше диафрагмы - от 26 до 103 Гр (в среднем 103±24,9 Гр), СОД на все тело от 26 до 268 Гр (в среднем 109,6±34,4).
Методы исследования включали у всех пациентов: стандартное клиническо-лабораторное обследование, исследование гормонов щитовидной железы и тиреотропного гормона, исследование функции внешнего дыхания (аппарат Sensor Medics), суточное мониторирование ЭКГ (система Shiller MT 200), ЭхоКГ, включая ТД. 60 больных выполнили нагрузочный тест на тредмиле с ЭКГ контролем (Woodway EXO 43), 18 - максимальный нагрузочный тест на тредмиле с газовым анализом. У части пациентов обследование включало также однофотонную эмиссионную томосцинтиграфию миокарда (ОФЭКТ, Межклиническое радионуклидное диагностическое отделение, зав. отделением к.м.н. Паша С.П.), и мультиспиральную компьютерную томографию органов грудной полости (межклинический кабинет МСКТ, заведующая к.м.н. Фоминых Е.В.). У всех пациентов исключены рецидив лимфогранулематоза и другие опухоли, а также специфические и неспецифические инфекционные заболевания, которые могли бы быть причиной клинических проявлений.
ЭхоКГ выполнялась на аппарате Vivid 7 (GE, США). Степень клапанной регургитации определяли в соответствии с Рекомендациям американского общества эхокардиографии (ASE, 2003). При трактовке данных к патологическим изменениям не относили трикуспидальную регургитацию I степени. Систолическую дисфункцию левого желудочка (СДЛЖ) диагностировали при фракции выброса (ФВ) ЛЖ45%. Для выявления диастолической дисфункции (ДД) ЛЖ использовали показатели трансмитрального кровотока, измеренные в режиме импульсной допплерэхоКГ: максимальную скорость в период раннего (E) и предсердного (A) наполнения, их соотношение (E/A), время замедления раннего диастолического кровотока (Dt) и изоволюмического расслабления ЛЖ (ВИВР), - а также пиковые скорости диастолического смещения фиброзного кольца митрального клапана по данным тканевого допплера: Еm (критерий ДД - Em<8см/с), Аm и их соотношение (Еm/Аm). Степень ДД диагностировали в соответствии с рекомендациями Европейского общества кардиологов (ESC, 2007). Для идентификации псевдонормализации использовали критерии Shon N. и соавт. (1997): Еm<8 см/с, Еm/Аm <1 в сочетании с показателями трансмитрального кровотока. При ТД определяли также скорость систолического укорочения ЛЖ (S).
ЭхоКГ критериями повышения давления заполнения (ДЗ) ЛЖ считали E/Em>15 или 8<E/Em<15+дополнительный признак: E/A <1, Dt>220мс, или ARdur –Adur>30мс, или индекс объема левого предсердия (ИОЛП)>40мл/м2. Индекс массы миокарда ЛЖ не учитывали, так как ее значимого увеличения не выявлено ни у одного пациента.
К несомненным признакам констрикции перикарда относили типичные изменения раннедиастолического наполнения ЛЖ в зависимости от фаз дыхания, а также изменения перикарда при МСКТ: кальциноз, утолщение3мм, отсутствие пространства между париетальным и висцеральным листками.
Тредмил-тест с газовым анализом (эргоспирометрию) проводили с использованием тредмила Woodway EXO 43 и диагностической станции CS-200 фирмы Shiller (Швейцария). Определяли пиковые ЧСС и АД, резерв ЧСС (разница между ЧСС максимальным и достигнутым), пиковую минутную легочную вентиляцию (VE), пиковое потребления кислорода (VO2peak), потребление кислорода при достижении анаэробного порога (AП), кислородный пульс (O2pulse=VO2/ЧСС) и дыхательный резерв (ДР) по соотношению пиковой минутной и максимальной произвольной вентиляции (MVV), определенной до теста.
Критериями несомненной ХСН считали: сочетание жалоб и симптомов, характерных для ХСН, со следующими объективными признаками: клапанными поражениями, за исключением митральной регургитации I степени, ФВЛЖ45%, повышением ДЗЛЖ, констрикцией перикарда или экссудативным перикардитом. Критериями вероятной ХСН при наличии жалоб и/или симптомов считали также любую, в том числе легкую, степень ДД ЛЖ, уплотнение перикарда, а также «сердечно-сосудистый» тип функциональных ограничений при эргоспирометрии.
Методы статистической обработки результатов исследования
Статистический анализ осуществлялся с помощью пакета программ SPSS for Windows, версия 11.5. Для описания показателей, представленных в виде альтернативных переменных, приведены число наблюдений и доля пациентов в процентах. Для описания показателей, представленных в виде количественных переменных, использовали данные описательной статистики, cредние значения представлены в формате: среднее арифметическое ± стандартное отклонение (М±).
Для проверки характера распределения переменных использовали графический метод (построение гистограмм) и непараметрический тест Колмогорова-Смирнова. В зависимости от типа и распределения переменных, а также от количества наблюдений применялись методы параметрической или непараметрической статистики. Так, для оценки значимости различий между двумя независимыми выборками использовали Т-тест Стъюдента или критерий Манна-Уитни. При оценке достоверности различий частоты качественных показателей применяли двухсторонний точный критерий Фишера.
Связь признаков анализировали с помощью таблиц сопряженности с применением статистического критерия 2, корреляционного и регрессионного анализа (метод биноминальной логистической регрессии). При корреляционном анализе использовали в зависимости от характера распределения и количества наблюдений коэффициент корреляции Пирсона или коэффициент ранговой корреляции Спирмена.
Определяли также относительный риск (ОР) развития сердечно-сосудистых осложнений в зависимости от того или иного фактора.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Клиническая характеристика. Жалобы и симптомы, характерные для заболеваний сердечно-сосудистой системы (одышка, отеки, слабость, учащенное сердцебиение, гипотония) имелись у 66,2% пациентов. Наиболее часто встречались жалобы на одышку при нагрузках, сердцебиение, утомляемость (табл. 1).
Таблица 1. Клинические проявления у обследованных больных.
| Клинические проявления | n | % |
| Без симптомов | 24 | 33,8 |
| С симптомами | 47 | 66,2 |
| в том числе: одышка | 42 | 59,2 |
| сердцебиения | 41 | 57,7 |
| cлабость, утомляемость | 35 | 49,3 |
| отеки | 12 | 16,9 |
| гипотония | 10 | 14,1 |
| плевральный выпот | 6 | 8,5 |
| асцит | 5 | 7,0 |
Среднее систолическое АД составляло 115,2±10,4, диастолическое - 71,0±6,0 мм рт.ст. Средняя ЧСС в покое составляла 82,1±11,2-1. У всех пациентов был синусовый ритм, у 1 больного – имплантированный электрокардимостимулятор в связи с АВ блокадой III степени. Ни у одного пациента не было артериальной гипертонии.
Различные патологические изменения сердца при обследовании были выявлены у 60 (84,5%) пациентов, а без учета изолированной митральной регургитации 1 ст.- у 50 (70,4%) пациентов. Типы поражений представлены в таблице 2.
Помимо этого, признаки поражения миокарда по данным ОФЭКТ выявлены у всех 13 пациентов, которым выполнено это исследование. У всех этих пациентов, кроме одного, имелись и другие патологические изменения, перечисленные в табл. 2. В 9 случаях изменения перфузии миокарда были диффузными (характерными для некоронарогенной патологии), а у 4 пациентов, причем у 2-х – без документированного инфаркта миокарда в анамнезе, выявлены также крупноочаговые поражения.
18 пациентов (25,4%) соответствовали критериям несомненной хронической сердечной недостаточности, еще у 17 пациентов она была вероятна. У 11 пациентов с клинически значимой ХСН выявлены признаки сочетанного поражения миокарда (в 9-ти случаях), значимых изменений клапанов (у 7-ми больных, причем у 5-ти – патология 2 или 3 клапанов) и перикарда (у 6-и больных).
Таблица 2. Сердечно-сосудистые поражения у обследованных пациентов
| Патология | Число пациентов | (%) |
| Поражения клапанов / исключая МР 1 Митрального /без МР 1ст регургитация/регургитация > I ст стеноз Аортального регургитация стеноз Трикуспидального регургитация> I ст стеноз | 33 /13 31/7 31/7 4 7 6 3 5 5 2 | 46,5/18,3 43,7/9,9 43,7/9,9 5,7 9,9 8,5 4,3 7,1 7,1 2,9 |
| Поражения перикарда Констрикция, уплотнение Выпот | 11 9 2 | 15,5 12,7 2,9 |
| Инфаркт миокарда | 2 | 2,9 |
| Другие поражения миокарда Систолическая дисфункция Диастолическая дисфункция В т. числе изолированная | 3 26 13 | 4,3 36,6 18,3 |
| АВ блокады 2 и 3 степени | 5 | 7,1 |
| Желудочковая экстрасистолия > 10 в час | 5 | 7,1 |
| ХСН В том числе несомненная ХСН IФК II ФК III ФК IV ФК | 35 18 7 5 2 4 | 49,3 25,4 9,9 7,1 2,9 5,7 |
| Всего пациентов с патологией | 60 | 84,5 |
АВ блокада III степени имелась у 1 пациента в сочетании с тяжелым поражением всех структур сердца: 3-х клапанов, миокарда и констрикцией перикарда. АВ блокады 2 степени у 2-х пациентов сочетались с ДД и другими признаками поражения миокарда, у 1-го – только с МР 1степени, и в 1 случае была изолированной.
Особенности поражений сердечно-сосудистой системы. В среднем объем ЛЖ был в пределах нормы, однако имелась тенденция к его уменьшению. При анализе распределения индексов конечнодиастолического (КДИ) и конечносистолического (КСИ) объемов у большинства обследованных пациентов их значения смещены ближе к нижней границе нормы, а у части пациентов – ниже нижней границы (рис 1). Ни у одного пациента не был увеличен КДИ, и лишь у 1 (после инфаркта) – незначительно увеличен КСИ. Это сопровождалось тенденцией к уменьшению ударного объема, а сердечный индекс был ниже нормы у подавляющего большинства обследованных лиц (рис. 2).
При исследовании диастолической функции ЛЖ были выявлены следующие особенности: несмотря на значительную долю пациентов с выявленной диастолической дисфункцией ЛЖ, у большей части пациентов ВИВР и Dt оставались в пределах нормы или укорочены. Удлинение Dt отмечено лишь у 4 и ВИВР – у 1 обследованного. (рис 3)
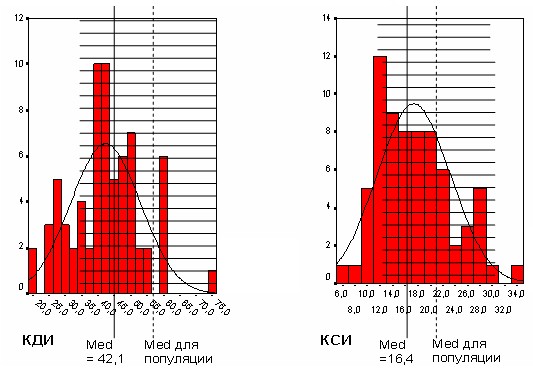
Рисунок 1 Распределение индексов конечнодиастолического и конечносистолического объемов ЛЖ. (заштрихованы границы нормы)
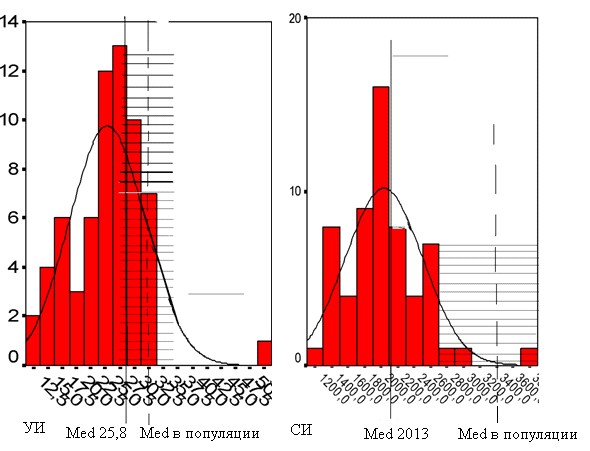
Рисунок 2. Распределение индекса ударного объема и сердечного индекса (заштрихованы границы нормы)
Рисунок 3 Распределение пациентов по диастолическим показателям
При ЭхоКГ обращало на себя внимание сохранение, даже у пациентов с тяжелой ХСН, нормальных размеров камер сердца и отсутствие гипертрофии миокарда. Пациенты были разделены на 3 группы в зависимости от характера преимущественного поражения сердца. В первую вошли пациенты без существенных эхокардиографических изменений (условно – «норма»). В вторую группу включены пациенты с систолической дисфункцией и/или митральной/аортальной регургитацией 2 степени, у которых можно было ожидать увеличение левых отделов сердца, в 3-ю – пациенты с констрикцией перикарда или изолированной ДД миокарда, у которых можно было ожидать дилатацию ЛП при нормальных размерах ЛЖ (условно – «с ДД») Некоторые ЭхоКГ параметры этих пациентов представлены в таблице 4.
Таблица 4. ЭхоКГ показатели в зависимости от преобладающего характера поражения сердца
| Показатель | 1 «Норма» n=37 | 2 СД, клапанные пороки (n=14) | р1 | 3 ДД (n=20) | р2 |
| КДИ, мл/м2 | 45,5±10,0 | 40,1±12,2 | н/д | 37,2±8,6 | 0,002 |
| КСИ, мл/м2 | 18,5±5,1 | 19,1±8,3 | н/д | 14,1±4,1 | 0,002 |
| УИ, мл/м2 | 27,3±6,4 | 21,0±7,5 | 0,010 | 23,1±5,4 | 0,014 |
| ФВ, % | 59,7±5,1 | 53,2±12,8 | н/д | 63,3±4,2 | 0,012 |
| СИ, мл/м2/мин | 2141,2±487,3 | 1755,8±706,4 | н/д | 1879,4±346,7 | 0,032 |
| ИММЛЖ, г/м2 | 78,6±21,1 | 87,6±23,3 | н/д | 79,0±19,5 | н/д |
| ИОЛП, мл/м2 | 24,8±6,0 | 27,8±7,3 | н/д | 22,7±7,1 | н/д |
| E, см/с | 103,7±19,3 | 126,8±44,6 | н/д | 95,7±23,3 | н/д |
| Dt, мс | 182,9±21,6 | 142,0±33,1 | 0,001 | 181,0±38,7 | н/д |
| ВИВР, мс | 79,5±6,8 | 68,8±11,4 | 0,010 | 76,8±10,9 | н/д |
| S, см/с | 9,39±1,25 | 7,00±1,41 | 0,001 | 8,32±1,60 | 0,019 |
| Em, см/с | 12,69±1,68 | 8,87±3,09 | 0,002 | 10,38±2,27 | 0,000 |
| E/Em | 7,78±1,63 | 12,48±6,13 | 0,080 | 8,67±3,03 | н/д |
Р1 – достоверность различий между 1 и 2 группами
Р2 – достоверность различий между 1 и 3 группами, критерий Манна -Уитни
У пациентов второй группы, вопреки ожиданиям, не было выявлено признаков ремоделирования ЛЖ, отсутствовали гипертрофия ЛЖ, увеличение объема ЛП, что в сочетании с достоверным снижением систолической и диастолической скоростей движения фиброзного кольца митрального клапана свидетельствовало о развитии, помимо СД и клапанных поражений, рестриктивных изменений миокарда.
У больных с изолированной ДД показатели диастолической функции были изменены в меньшей степени. Средние показатели диастолического трансмитрального кровотока не отличались от нормы, но имелось наиболее значимое уменьшение объема ЛЖ. Следует отметить более высокую ФВ и меньший КСИ у пациентов этой группы по сравнению с 1-й. Повышение сократимости могло иметь компенсаторный характер.
Средняя ЧСС в покое составляла 82,1±11,2-1, среднесуточная ЧСС при холтеровском мониторировании - 87,7±10,5-1. ЧСС в покое была 80мин-1 у 44 (62,0%) пациентов, среднесуточная ЧСС 90-1 - у 33 (46,5%) пациентов. Тахикардия выявлялась не только у пациентов со значимой ХСН. После исключения пациентов со значимой ХСН и значимыми клапанными регургитациями у больных с тахикардией объемы были существенно меньше: средний КДИ составлял 40,6±9,4 по сравнению с 50,3±7,2 мл/м2 (p<0,006), КСИ - 16,0±4,9 по сравнению с 22,1±4,4 мл/м2 (p<0,004). ЧСС в покое связывали достоверные отрицательные корреляции с УО (r=0,506), УИ (r=0,488) и КДИ (r=0,452, во всех случаях p<0,001, r – коэффициент корреляции Пирсона). Среднесуточная ЧСС также была связана с объемами ЛЖ, хотя и несколько слабее: с УИ (r=0,309, p=0,019), КДИ (r=0,406, p=0,002) и КСИ (r=0,435, p=0,001).
Вариабельность сердечного ритма. Результаты суточного мониторирования ЭКГ представлены в таблице 5. У 73 % обследованных один или несколько показателей вариабельности сердечного ритма были ниже нормы. Вариабельность ритма закономерно связывали достоверные отрицательные корреляции с ЧСС.
Таблица 5. Вариабельность ритма по данным суточного мониторирования ЭКГ
| Показатель | Min-Max | (М±) | Число пациентов со снижением |
| SDNN мсек | 32-187 | 108,0±34,1 | 35 |
| SDANN мсек | 24-165 | 91,0±33,2 | 30 |
| SDNNi мсек | 18,5-95,7 | 47,4±17,2 | 12 |
| RMSSD мсек | 10,5-74,5 | 33,5±14,5 | 18 |
| NN50 | 155-31124 | 6911±6534 | - |
| PNN50% | 0,14-28,00 | 6,8±6,9 | 52 |
Связь неспецифических симптомов с поражением сердца.
«Малосимптомные» пациенты с жалобами на одышку и/или утомляемость при нагрузках (исключая больных с клинически значимой ХСН) отличались от тех, кто не предъявлял никаких жалоб, более высокой сократимостью ЛЖ (судя по более высокой ФВЛЖ и меньшему КСО) и меньшим Dt. Наиболее существенно их отличали тканевые диастолические показатели: более низкая скорость раннедиастолического удлинения миокарда и соответственно «худшие» Em/Am и E/Em (таблица 6).
Таблица 6. Различие показателей ЭхоКГ у пациентов с неспецифическими жалобами и без жалоб
| Показатель | Пациенты без жалоб (М±) N=24 | Пациенты с жалобами (М±) N=36 | P |
| Еm*, см/сек | 15,57±3,40 | 13,49±3,02 | 0,015 |
| Аm* см/сек | 8,19±2,07 | 9,31±1,72 | 0,005 |
| Еm*/Am* | 1,98±0,59 | 1,50±0,44 | 0,000 |
| E/Em* | 6,65±1,34 | 7,85±2,44 | 0,028 |
| Dt мсек | 193,8±29,0 | 175,4±24,1 | 0,007 |
| КСО,мл | 36,2±11,9 | 29,8±8,7 | 0,049 |
| ФВЛЖ, % | 59,0±4,9 | 62,1±8,8 | 0,013 |
*Приведены параметры, измеренные в области свободной стенки ЛЖ.
**Р – достоверность различий показателей у пациентов с жалобами и без жалоб, критерий Манна-Уитни.
Поражение легких также имело значение: у пациентов с одышкой или слабостью ФЖЕЛ и ОФВ1 были достоверно ниже, чем у бессимптомных (таблица 7). Вместе с тем, соотношение ОФВ1/ФЖЕЛ не различалось даже на уровне тенденции, что позволило нам сделать вывод о том, что наибольший вклад в развитие симптомов вносили рестриктивные, а не обструктивные изменения.
Показатели ФВД коррелировали с показателями ЭХО КГ (Таблица 8)
Таблица 7. Сравнение показателей ФВД у пациентов с жалобами на одышку и без жалоб.
| Одышки нет 29 (М±) | Одышка есть 31 (М±) | p | |
| ФЖЕЛ мл | 4542±1139 | 3897±1058 | 0,034 |
| ФЖЕЛ мл, % от ожидаемого | 93,4±15,8 | 83,3±13,8 | 0,005 |
| ОФВ1 мл | 3727±835 | 3182±910 | 0,018 |
| ОФВ1 мл, % от ожидаемого | 93,1±14,2 | 83,7±13,4 | 0,008 |
| ОФВ1/ФЖЕЛ | 82,7±5,8 | 81,6±7,8 | 0,83 |
Таблица 8 Корреляции ФЖЕЛ и показателей ЭХО КГ
| Показатель ЭхоКГ | ФЖЕЛ | |
| R Спирмена | P | |
| КДО | 0,453 | 0,000 |
| УО мл | 0,445 | 0,000 |
| Em | 0,435 | 0,000 |
| ВИВР | 0,427 | 0,000 |
Р- достоверность корреляций
У больных с клинически значимой ХСН снижение легочных объемов было обусловлено очевидными причинами (грубые фиброзные изменения легочной паренхимы, плевральный выпот – у 5 пациентов, в том числе у одного – хилоторакс, а также сама сердечная недостаточность). Вместе с тем, и после исключения из анализа 11 пациентов со значимой ХСН, сохранялись достоверные корреляции между ФЖЕЛ и ОВФ1 с одной стороны и КДО, УО и тканевыми доплеровскими параметрами - с другой. Это свидетельствовало о развитии однонаправленных (рестриктивных) изменений сердца и легких.
Результаты кардиореспираторного нагрузочного теста.
Максимальная проба с нагрузкой на тредмиле с газовым анализом проведена у 18 пациентов, не имевших клинически значимой сердечной недостаточности и избыточной массы тела. У большинства (12) из них отсутствовали какие бы то ни было изменения сердца в покое, за исключением митральной регургитации I степени в 2-х случаях. У 3-х пациентов имелась ДД 1ст. и у 1 – ДД 2 ст. В таблице 9 приведены основные результаты пробы.
Таблица 9 Результаты кардиореспираторного
нагрузочного теста
| Показатель | (М±) | Норма |
| ЧССпик | 176,5±12,6 | |
| CАДпик | 172,3±25,1 | |
| МЕТ | 11,3±3,2 | |
| Резерв ЧСС | 11,8±13,8 | 15 уд/мин |
| Дыхательный резерв, % MVV | 50,2±21,1 | 72 ± 15% |
| VO2пик, % | 73,7±17,2 | 84% |
| VO2 АП, %VO2пик | 73,7±17,2 | мин >40% от VO2max должного |
| O2 пульс, % | 78,8±17,1 | 80% |
Пиковое потребление кислорода было умеренно снижено, что свидетельствовало о снижении толерантности к физической нагрузке. Остальные показатели в среднем были в пределах нормы, однако, кислородный пульс (эквивалент ударного объема) - на нижней границе нормы. Характерен был также быстрый рост ЧСС, опережавший рост кислородного пульса. Такие изменения характерны для сердечной недостаточности (при отсутствии коронарной патологии). У 7 больных значимое снижение этих показателей в отсутствие изменений сердца по данным ЭхоКГ позволило предполагать наличие постлучевой рестриктивной кардиомиопатии.
Снижение пикового потребления кислорода тесно коррелировало с уменьшением индексов конечнодиастолического (r=0,809, p<0,001) и ударного объема ЛЖ (r=0,737, p=0,001).
У всех пациентов определялся высокий дыхательный резерв, таким образом легочная патология не являлась причиной снижения толерантности к нагрузке.
Предикторы сердечно-сосудистых осложнений химиолучевой терапии.
Мы проанализировали прогностическую значимость пола, возраста, срока, прошедшего после лечения, особенностей химио- и лучевой терапии (препараты, дозы) в отношении следующих исходов: 1) любых объективных изменений сердца; 2) вероятной ХСН; 3) значимой ХСН тяжестью не менее II ФК; 4) клапанных поражений (исключая МР I степени). Предикторы поражения клапанов анализировали отдельно в связи с тем, что их развитие может иметь значение для профилактики инфекционного эндокардита.
Предикторы любых поражений. Развитие сердечных поражений не зависело от пола пациентов, а было ассоциировано с проведением ХЛТ в более старшем возрасте и с большим возрастом в настоящее время. Пациенты с патологией получили более высокую дозу антрациклинов, дозы прочих химиопрепаратов различались недостоверно. Доза облучения на средостение при патологии была недостоверно выше.
Значимыми предикторами каких бы то ни было изменений сердца были возраст пациента, в котором проводилась ХЛТ (по данным регрессионного анализа коэффициент = 0,301, константа =3,855), а также возраст в момент настоящего обследования ( = 0,257, константа = 5,376). Риск развития сердечных поражений существенно возрастал при проведении ХЛТ в возрасте старше 19лет (таблица 10).
Пациенты, которые получали ХЛТ в возрасте старше 19 лет, получили в среднем большую дозу антрациклинов, чем остальные (212,7±71,9 по сравнению с 167,4±105,6мг/м2, р=0,036), и большую СОД на средостение (40,76±6,739 по сравнению с 35,95±6,55Гр, р=0,003, в обоих случаях – критерий Т). Вместе с тем, связь сердечных поражений и возраста не была обусловлена этими различиями, так как и после поправки на дозу антрациклина или СОД сохранялись значимые корреляции возраста начала лечения с развитием любых поражений:
Признаки вероятной сердечной недостаточности были ассоциированы, помимо более старшего возраста при проведении ХЛТ и большего возраста в момент настоящего обследования, с более высокой облучающей дозой на средостение, а также более длительным сроком, прошедшим после окончания ХЛТ.
Наиболее значимым предиктором вероятной ХСН был возраст пациента в момент настоящего обследования ( = 0,207, константа = 6,132), несколько менее значимым – возраст проведения ХЛТ ( = 0,184, константа =3,668). Риск вероятной ХСН существенно возрастал при проведении ХЛТ в возрасте старше 19лет (таблица 10). СОД на средостение также была значимым предиктором вероятной ХСН ( = 0,085, константа = 3,226), (таблица 10), но при регрессионном анализе с пошаговым добавлением ковариат не уточняла прогноз, сделанный на основании возраста при проведении ХЛТ.
Значимые корреляции вероятной ХСН с возрастом в начале лечения сохранялись после коррекции на дозу антрациклинов и СОД на средостение.
Клапанные поражения были ассоциированы с большим возрастом пациентов в момент обследования и большей СОД на средостение, а также с более длительным сроком, прошедшим после ХЛТ. Все эти факторы являлись независимыми предикторами значимых клапанных поражений, и наиболее значимым предиктором была СОД на средостение (остальные ковариаты не уточняли прогноз):
для СОД = 0,161, константа =7,934;
для срока, прошедшего после лечения: =0,113, константа = 2,560.
Минимальный срок после окончания ХЛТ, при котором выявлены значимые поражения клапанов, составлял 6 лет. Риск клапанных поражений существенно возрастал после 8 лет, прошедших после лечения лимфогранулематоза (таблица 10).
Развитие несомненной ХСН тяжестью не менее 2 ФК было ассоциировано с проведением ХЛТ в более старшем возрасте, с большим возрастом в настоящее время, более высокой дозой облучения на средостение, а также с общей полученной дозой облучения. Наиболее значимым предиктором была СОД на средостение ( = 1,177, константа = 52,794) (табл. 10). Значимость прогноза на основании этого показателя составляла 93%..
Независимыми предикторами ХСН также являлись более старший возраст начала ХЛТ ( = 0,138, константа = 4,808) и более старший возраст при данном обследовании ( = 0,189, константа = 8,002).
Регрессионный анализ с пошаговым включением двух ковариат – дозы облучения на средостение ( = 2,792) и возраста начала ХЛТ ( = 0,687, константа = 139,243) позволял предсказывать развитие ХСН IIФК с вероятностью =97,2%.
Таблица 10. Предикторы поздних сердечно-сосудистых осложнений
| Осложнение | Предиктор | ОР | 95%ДИ | р |
| ХСН 2ФК | СОД 40 Гр | 1,9 | 1,4 - 2,4 | 0,002 |
| ХСН 2ФК | СОД 44 Гр | 7,5 | 3,9 - 14,2 | <0,001 |
| Вероятная ХСН, все ФК | СОД 44 Гр | 2,7 | 1,1 - 6,8 | 0,019 |
| Поражение клапанов (без МР I) | СОД 44 Гр | 3,5 | 1,7 - 7,1 | <0,001 |
| ХСН 2ФК | возраст в начале химиолучевой терапии >19лет | 2,7 | 1,9 - 3,8 | <0,001 |
| Вероятная ХСН, все ФК | возраст в начале химиолучевой терапии >19лет | 3,0 | 1,6 - 5,8 | <0,001 |
| Любое поражение сердца | возраст в начале химиолучевой терапии >19лет | 6,5 | 1,0 - 43,1 | <0,001 |
| Поражение клапанов | срок после окончания лечения >8 лет | 2,2 | 1,3 - 3,7 | 0,012 |
СОД – суммарная облучающая доза на средостение
ВЫВОДЫ.
1. Патологические изменения сердечно-сосудистой системы выявлены у 84,5% пациентов моложе 50 лет, перенесших не менее 5 лет назад химиолучевую терапию по поводу лимфогранулематоза с поражением внутригрудных лимфоузлов. Поражения клапанов диагностированы у 49,3%, диастолическая дисфункция левого желудочка (ЛЖ) – у 38%, систолическая дисфункция – у 12,7%, поражения перикарда – у 15,5%, нарушения ритма и проводимости – у 23,9%, инфаркт миокарда - у 2,8%, хроническая сердечная недостаточность (ХСН) - у 25,4% пациентов.
2. Для пациентов, перенесших химиолучевую терапию с облучением средостения, характерны рестриктивные изменения ЛЖ: уменьшение объема, сокращение времени изоволюмического расслабления и времени замедления раннего трансмитрального наполнения (Dt), снижение ударного объема и сердечного выброса (средний сердечный индекс=2,03±0,49л/мин/м2). В отличие от диастолической дисфункции другого генеза это не сопровождается дилатацией левого предсердия, а у больных с систолической дисфункцией, клапанными поражениями и ХСН отсутствуют также признаки компенсаторного ремоделирования ЛЖ.
3. Предикторами поражений сердца являются: более высокая суммарная облучающая доза на средостение [при дозе 44Гр ОР ХСН = 7,5 (95% ДИ: 3,9; 14,3)], более старший возраст на момент лечения [для возраста >19лет ОР ХСН = 2,7 (95% ДИ: 2,0; 3,8)] и при данном обследовании. Риск поражения клапанов возрастает также по мере увеличения срока, прошедшего после окончания химиолучевой терапии [для срока > 8 лет ОР = 2,2 (95% ДИ: 1,3; 3,7)].
4. Распространенность жалоб на одышку, утомляемость, сердцебиения при отсутствии клинически значимой ХСН достигает 50,7%. Эти симптомы ассоциированы с укорочением Dt, ухудшением тканевых диастолических показателей ЛЖ, и с повышением сократимости ЛЖ и ЧСС. Компенсаторный характер тахикардии подтверждают умеренные корреляции между ростом ЧСС и уменьшением конечнодиастолического (r=0,452, p<0,001) и ударного объема ЛЖ (r=0,506, p<0,001).
5. У малосимптомных и бессимптомных пациентов пиковое потребление кислорода умеренно снижено (74%). Снижение этого и других показателей физической работоспособности тесно коррелирует с уменьшением индексов конечнодиастолического (r=0,809, p<0,001) и ударного объема ЛЖ (r=0,737, p=0,001).
Практические рекомендации:
- С учетом высокой распространенности поздних сердечно-сосудистых осложнений пациенты, получавшие химиолучевую терапию с облучением средостения по поводу лимфогранулематоза, должны находиться под наблюдением кардиолога. Срок наблюдения не ограничен, поскольку риск развития поздних сердечно-сосудистых осложнений возрастает по мере увеличения срока после окончания лечения
- В первую очередь в наблюдении кардиолога нуждаются пациенты со следующими факторами риска:
- доза облучения на средостение не менее 40 Гр
- проведение ХЛТ в возрасте старше 19 лет
- срок с момента окончания ХЛТ – 8 и более лет
- У больных, перенесших ХЛТ с облучением средостения, назначение препаратов, снижающих ЧСС, может привести к клинически значимому снижению сердечного выброса, поэтому требует повышенной осторожности и дополнительного контроля состояния пациента.
Список опубликованных научных работ по теме диссертации
- Авдеев Ю.В., Полтавская М.Г., Куприна И.В., Куклина М.Д., Мкртумян Э.А., Шорников С.Б., Сыркин А.Л. Хроническая сердечная недостаточность в отдаленные сроки после химиолучевой терапии лимфогранулематоза с поражением внутригрудных лимфоузлов// Доклады II конгресса общества специалистов по сердечной недостаточности «Сердечная недостаточность 2007». Москва, декабрь 2007: с.10.
- Мкртумян Э.А., Полтавская М.Г., Авдеев Ю.В., Сыркин А.Л. Эргоспирометрия в дифференциальной диагностике хронической сердечной недостаточности // Доклады II конгресса общества специалистов по сердечной недостаточности «Сердечная недостаточность 2007». Москва, декабрь 2007: с 28.
- Сыркин А.Л., Куприна И.В., Авдеев Ю.В., Полтавская М.Г., Стручкова Т.Я., Пивник А.В. Влияние лучевой и химиотерапии злокачественных новообразований на развитие атеросклероза, ишемической болезни сердца и липидный спектр. «Клиническая медицина», 2008;Том 86, № 11, с 28-31.
- M.G. Poltavskaya, E.A. Mkrtumian, A.L. Syrkin, A.A. Doletskij, M.D. Kuklina, Y.V.Avdeev. Evaluation of the origin of exercise limitations by cardiopulmonary exercise testing in patients with suspected diastolic heart failure. European Journal of Heart Failure Supplements 2008; Vol. 7(1), page 42.
- Ю. Авдеев, М. Полтавская, С. Шорников, А. Сыркин
Патология сердца в отдаленные сроки после химиолучевой терапии лимфогранулематоза с поражением внутригрудных лимфатических узлов. «Врач»- №9. 2009г с. 72-76. - M. Poltavskaya, Y. Avdeev, S. Shornikov, E. Mkrtumian, А. Doletskij, A. Syrkin Cardiac disease after mediastinal irradiation for Hodgkin's lymphoma. European Journal of Heart Failure Supplements 2009; Vol. 8(2).
Список сокращений
| A | максимальная скорость позднедиастолического наполнения левого желудочка |
| Adur | максимальная скорость диастолического потока в легочных венах |
| Am | максимальная скорость движения фиброзного кольца митрального клапана в систолу предсердий |
| ARdur | максимальная продолжительность диастолического реверсивного потока в легочных венах |
| AT | анаэробный порог |
| Dt | время замедления раннедиастолического трансмитрального кровотока |
| E | максимальная скорость раннедиастолического трансмитрального кровотока |
| Em | максимальная скорость фиброзного кольца митрального клапана в фазу раннедиастолического наполнения |
| MVV | максимальная произвольная вентиляция легких |
| O2-pulse | кислородный пульс |
| S | максимальная скорость фиброзного кольца митрального клапана в диастолу |
| VO2peak | пиковое потребление кислорода |
| VЕ | минутная легочная вентиляция |
| АД | артериальное давление |
| ВИВР | время изоволюмического расслабления левого желудочка |
| Гр | Грей, единица измерения облучающей дозы |
| ДД | диастолическая дисфункция |
| ДЗЛЖ | давление заполнения ЛЖ |
| ИММЛЖ | индекс массы миокарда левого желудочка |
| ИОЛП | индекс объема левого предсердия |
| КДИ | индекс конечно-диастолического объема левого желудочка |
| КДО | конечно-диастолический объем левого желудочка |
| КСО | индекс конечно-систолического объема левого желудочка |
| ЛЖ | левый желудочек |
| ЛП | левое предсердие |
| МР | митральная регургитация |
| ОР | относительный риск |
| ОФВ1 | объем форсированного выдоха за 1 секунду |
| ОФЭКТ | однофотонная эмиссионная томосцинтиграфия |
| СД | систолическая дисфункция |
| СОД | суммарная облучающая доза |
| ТД | тканевая миокардиальная допплерэхокардиография |
| УИ | индекс ударного объема |
| УО | ударный объем |
| ФВ | фракция выброса |
| ФВД | функция внешнего дыхания |
| ФЖЕЛ | форсированная жизненная емкость легких |
| ФК | функциональный класс |
| ХЛТ | химиолучевая терапия |
| ХСН | хроническая сердечная недостаточность |
| ЧСС | частота сердечных сокращений |

