Хроническая сердечная недостаточность ишемического и ревматического генеза: инструментальные и биохимические маркёры в сопоставлении с клиническими признаками
На правах рукописи
Казаковцева Татьяна Алексеевна
ХРОНИЧЕСКАЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ ИШЕМИЧЕСКОГО И РЕВМАТИЧЕСКОГО ГЕНЕЗА: ИНСТРУМЕНТАЛЬНЫЕ И БИОХИМИЧЕСКИЕ МАРКЁРЫ В СОПОСТАВЛЕНИИ С КЛИНИЧЕСКИМИ ПРИЗНАКАМИ
14.00.05 – внутренние болезни
Автореферат
диссертации на соискание учёной степени
кандидата медицинских наук
Москва - 2009
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель:
доктор медицинских наук, профессор Шостак Надежда Александровна
Официальные оппоненты:
Доктор медицинских наук, профессор
ГОУ ВПО РГМУ Росздрава Потешкина Наталья Георгиевна
Доктор медицинских наук, профессор
ГОУ ВПО ММА Росздрава Цурко Владимир Викторович
Ведущая организация:
ГОУ ВПО “Московский государственный медико-стоматологический университет Росздрава”.
Защита состоится «14 » декабря 2009 г. в 14.00 часов на заседании диссертационного совета Д 208.072.01 при ГОУ ВПО РГМУ Росздрава (117997, Москва, ул. Островитянова, д. 1)
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО РГМУ Росздрава
Автореферат разослан «02» сентября 2009 г.
Учёный секретарь диссертационного совета
доктор медицинских наук, профессор Джанашия Платон Харитонович
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Хроническая сердечная недостаточность (ХСН) является одной из важнейших проблем кардиологии и требует детального анализа. Эта патология входит в число ведущих причин заболеваемости и смертности в мире. На лечение ХСН в России тратится от 55 до 295 млрд рублей в год, а расходы на госпитализацию по поводу обострений ХСН достигают 184,7 млрд рублей [Д. А. Напалков и совт., 2008]. По данным эпидемиологического исследования Общества сердечно-сосудистой недостаточности распространённость ХСН в России достигает 4-5%, что соответствует 6-7 миллионам человек [Беленков, Мареев, 2002]. Средняя 5-летняя смертность во всей популяции больных ХСН (с учетом начальных и умеренных стадий) остается высокой и составляет 65% для мужчин и 47% для женщин [Ho K.K., Pinsky J.L и соавт., 1993].
ХСН является прогрессирующим синдромом, и пациенты, имеющие бессимптомную ХСН, в течение 1–5 лет могут перейти в группу самых тяжелых больных, плохо поддающихся лечению. Поэтому ранняя диагностика ХСН и дисфункции левого желудочка (ЛЖ), а, следовательно, и раннее начало лечения таких больных — залог успеха в профилактике смертности от сердечной недостаточности. К сожалению, в России крайне редко диагностируют ХСН на начальной стадии, что свидетельствует об отсутствии четких критериев диагностики ХСН в самый ранний период ее развития.
Ведущим компонентом формирования и прогрессирования ХСН является ремоделирование сердца [Сергеева Л.И., 2007]. В глобальном смысле ремоделирование характеризуется прогрессирующим увеличением левого желудочка и повышением его сферичности. На клеточном уровне процесс ремоделирования характеризуется гипертрофией и "сморщиванием" миоцитов, аккумуляцией коллагена в интерстициальном пространстве. Структурное ремоделирование сердца является интегральным механизмом перехода скрытой сердечной недостаточности в явную [Goldstein S, 1995]. Нарушение геометрии ЛЖ присуще всем пациентам с дисфункцией ЛЖ и часто предшествует уменьшению фракции выброса, нарушениям системной гемодинамики и клиническим проявлениям [В.Г.Флоря, 1997].
В настоящее время внедряется большое количество новых эхокардиографических показателей, позволяющих оценивать ремоделирование сердца, таких как систолический и диастолический индексы сферичности, миокардиальный стресс, индекс напряжения миокарда, показатели диастолической функции (в том числе, время изоволюмического расслабления, время замедления раннего наполнения). Васюк и соавт. (МГМСУ, Москва, 2003) предложили использование интегральных систолического и диастолического индексов ремоделирования (ИСИР и ИДИР соответственно), которые отражают взаимосвязь систолической и диастолической функций левого желудочка с особенностями его геометрии. По данным ряда исследований некоторые из этих показателей в большей степени, чем фракция выброса левого желудочка, коррелируют с выраженностью симптомов заболевания [Кузнецов Г.Э., 2004, Tischler MD, 1993, Perlowski AA, 2007]. Kleber F.X. с соавт. (1992 г) расценивают индекс сферичности как единственный значимый прогностический фактор, позволяющий предсказать дальнейшее увеличение размеров ЛЖ. Роль этих параметров в практической медицине ещё предстоит оценить.
Изучение гормональной активности сердца началось в 1980 г, несколькими годами позже была идентифицирована химическая структура предсердного (ПНП), а затем - мозгового (МНП) и С-типа натрийуретических пептидов. Были продемонстрированы высокие чувствительность и специфичность этих веществ в ранней диагностике ХСН, корреляция их уровня в плазме крови с фракцией выброса левого желудочка. Следовательно, повышенный уровень МНП может являться одним из критериев диагностики сердечной недостаточности и использоваться при дифференциальной диагностике сердечной недостаточности и других патологий, сопровождающихся одышкой [Sirithunyanont C, 2003]. Однако существуют данные и о том, что до 21% пациентов с систолической дисфункцией миокарда при хронической сердечной недостаточности имеют нормальный уровень МНП [Tang WWH, 2003]. Синтез этих пептидов при ХСН на фоне ревматических пороков сердца изучен недостаточно.
Таким образом, роль МНП в патофизиологии сердечной недостаточности, взаимосвязь этого параметра с эхокардиографическими показателями нуждаются в дальнейшем изучении.
Цель исследования: провести комплексный анализ клинических, биохимических и инструментальных показателей у больных ХСН в зависимости от ее тяжести и генеза.
Задачи исследования:
- Оценить клинические проявления ХСН ишемического и ревматического генеза с учетом темпов её прогрессирования на догоспитальном этапе.
- Проследить зависимость клинических проявлений ХСН от типов ремоделирования левого желудочка и выраженности его диастолической дисфункции.
- Выявить ранние эхокардиографические маркёры ХСН.
- Исследовать уровень мозгового и предсердного натрийуретических пептидов при ХСН ишемического и ревматического генеза.
- Изучить корреляцию между клиническими, лабораторными (с учетом натрийуретических пептидов), и различными эхокардиографическими показателями (фракция выброса, индекс сферичности, масса миокарда левого желудочка и др.) у больных ХСН ишемического и ревматического генеза.
6. Установить эхокардиографические и биохимические параметры наиболее значимые в прогностическом отношении, а также выявить эхокардиографические показатели в большей степени подверженные изменениям при прогрессировании ХСН ишемического и ревматического генеза.
Научная новизна:
1. Произведена комплексная оценка эхокардиографических параметров систолический и диастолической функций левого и правого желудочков, определяющих ремоделирование сердца при ХСН ишемического и ревматического генеза.
2. Выявлены ЭхоКГ-показатели, обладающие наибольшей диагностической значимостью у пациентов с ХСН ревматического генеза. К ним, в частности, относятся: систолическое давление в лёгочной артерии (СДЛА), соотношение КСР/КДР лп (LAEF), площадь левого предсердия, степень митральной регургитации (МР), фракция выброса правого желудочка (EFпж). Ряд этих показателей охарактеризован при РБС впервые.
3. Впервые выявлены ранние эхокардиографические маркёры ХСН у пациентов с ИБС с сохранной систолической функцией ЛЖ и I ФК по NYHA. К ним, в том числе, относятся систолический индекс сферичности, интегральный систолический индекс ремоделирования, соотношение УО/КСОлж.
4. Изучена корреляция ЭхоКГ-параметров с клиническими показателями; выявлены параметры, наиболее информативные в прогностическом отношении. Установлено, что при ХСН на фоне ИБС ряд ЭхоКГ-показателей в большей степени, чем фракция выброса ЛЖ коррелирует с тяжестью состояния пациента. К таким показателям, в частности, относятся: маркёры диастолической дисфункции, интегральный систолический индекс ремоделирования, индексы сферичности ЛЖ, степень митральной регургитации и лёгочной гипертензии.
5. Впервые разработаны шкалы оценки ремоделирования сердца по данным эхокардиографического исследования, а также выявлены комбинации клинических, эхокардиографических и биохимических признаков, позволяющих оценить прогноз пациента.
6. Оценена целесообразность биохимических методов диагностики (МНП, ПНП) при ХСН различного генеза (РБС, ИБС). Продемонстрирована недостаточно высокая информативность уровня МНП при ранних этапах развития ХСН, особенно при её ревматической этиологии.
Практическое значение: Определение ранних эхокардиографических маркёров ХСН поможет выявлять пациентов на начальной стадии заболевания, что может повлиять на тактику их лечения и прогноз. Установлено, что биохимический маркёр ХСН - мозговой натрийуретический пептид не всегда адекватно отражает тяжесть ХСН, особенно при её развитии на фоне ревматических пороков сердца. Предложенные шкалы оценки ремоделирования сердца, а также выявленные комбинации наиболее значимых в прогностическом отношении признаков, после доработки и изучения на большой группе пациентов помогут врачу-клиницисту в выявлении больных, нуждающихся в более пристальном наблюдении врача.
Положения, выносимые на защиту
1. ХСН ишемического генеза характеризуется более тяжёлым течением, чем ХСН на фоне ревматических митральных пороков сердца, что проявляется в более высокой частоте встречаемости таких симптомов как влажные хрипы в лёгких, отёки нижних конечностей, эпизоды сердечной астмы, а также в более высокой потребности в госпитализациях по поводу декомпенсации сердечной недостаточности.
2. Для ХСН на фоне ревматических митральных пороков характерно длительное сохранение нормальной геометрии ЛЖ либо формирование концентрических адаптивных форм ремоделирования, в отличие от ХСН ишемического генеза, при которой, начиная с ранних стадий, отмечается преобладание дезадаптивных эксцентрических форм ремоделирования ЛЖ.
3. К наиболее ранним эхокардиографическим маркёрам ХСН при ИБС относятся: систолический и диастолический индексы сферичности ЛЖ, систолический миокардиальный стресс ЛЖ, интегральный систолический индекс ремоделирования, соотношение КСР/КДРлп (LAEF) и соотношение УО/КСОлж.
4. Уровень МНП на ранних этапах развития ХСН часто не превышает нормальных значений, в то время как при развёрнутой ХСН он достоверно коррелирует практически со всеми маркёрами систолической и диастолической функций ЛЖ. Таким образом, уровень МНП не может использоваться в качестве единственного маркёра при диагностике начальных форм ХСН, особенно ревматического генеза.
5. При оценке взаимосвязи между клиническими симптомами ХСН и рядом ЭхоКГ-параметров, установлено, что при ишемической ХСН степень диастолической дисфункции ЛЖ, площадь ЛП и систолический индекс сферичности в наибольшей степени соответствовали выраженности клинических симптомов. Корреляция фракции выброса ЛЖ с клиническими проявлениями ХСН была менее существенной. При ХСН на фоне РБС наибольшей степенью корреляции с клиническим статусом характеризовались: СДЛА, LAEF, площадь ЛП.
6. При оценке пациентов в динамике было отмечено, что в группе ИБС ухудшение клинического состояния в немалой степени было связано с нарастанием диастолической дисфункции ЛЖ и лёгочной гипертензии. В группе РБС ухудшение клинического состояния коррелировало с увеличением площади левого предсердия, ухудшением диастолической функции ПЖ, нарастанием миокардиального стресса ЛЖ, а также с увеличением степени лёгочной гипертензии и митральной регургитации.
Апробация работы
Материалы диссертации доложены на 7-th John Humphrey advanced summer school in immunology (Moscow, 2005), на научно-практической конференции "Современная кардиология: наука и практика" (Санкт-Петербург, 2007), III Конгрессе (IX конференции) «Сердечная недостаточность» (Москва, 2008).
По материалам диссертации опубликовано 7 печатных работ.
Объем и структура диссертации.
Диссертация изложена на 146 страницах машинописного текста и состоит из введения, обзора литературы, описания материалов и методов исследования, 2 глав собственных исследований, обсуждения, выводов и указателя литературы, содержащего 51 отечественных и 106 зарубежных источников. Диссертация иллюстрирована 19 диаграммами, 39 таблицами, 3 рисунками, 4 клиническими примерами.
Внедрение в практику
Результаты исследования внедрены в практику терапевтического отделения 1 ГКБ имени Н. И. Пирогова, в работу Московского Городского Ревматологического Центра при ГКБ№ 1, а также в преподавательскую работу кафедры факультетской терапии лечебного факультета имени академика А. И. Нестерова ГОУ ВПО РГМУ Росздрава.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Для решения задач, поставленных в работе, обследовано 200 больных ХСН (средний возраст 62,7±10,0 лет (35-85 лет), женщин - 115, мужчин – 85), из них 100 больных с ИБС и 100 больных РБС (сочетанный митральный или комбинированный митрально-аортальный порок). Также было обследовано 30 больных в качестве группы сравнения (средний возраст 57,8±1,24 года; женщин – 18, мужчин - 12).
Критериями включения в группе ИБС являлся перенесённый Q-инфаркт миокарда (более 6 месяцев назад), в группе РБС – сочетанный митральный порок. Допускалось также наличие незначительного аортального порока (аортальная регургитация не более I степени, пиковый градиент на аортальном клапане не более 15 mm Hg). Критериями исключения были: острые формы ИБС (инфаркт миокарда, нестабильная стенокардия), ХОБЛ, ХПЛГ, врождённые пороки сердца, дегенеративный стеноз устья аорты, декомпенсированные заболевания щитовидной железы, ожирение III ст, умеренная и тяжёлая степень артериальной гипертензии, декомпенсированная ХПН, анемия с уровнем Hb 95 г/л, сочетанная патология (ИБС + РБС). У больных с РБС ишемическая болезнь сердца исключалась на основании данных анамнеза, жалоб (отсутствие стенокардии), отсутствия рубцовых и ишемических изменений на ЭКГ.
Тяжесть ХСН оценивалась по Нью-Йоркской классификации (1964, 1979) и шкале оценки клинического состояния больного - ШОКС в модификации В.Ю. Мареева (2000). Дополнительно с целью оценки функционального статуса пациента проводился тест ходьбы в течение 6 минут c определением пройденного пути в метрах.
Характеристика обследованных пациентов представлена в таблицах 1 и 2.
Таблица 1. Общая характеристика обследованных больных ХСН
на фоне ИБС
| Возраст, годы (М±s) | 68,6±10,0 |
| Мужчины, чел (%) | 62 (62%) |
| Женщины, чел (%) | 38 (38%) |
| Один ИМ в анамнезе, чел (%) | 69 (69%) |
| Более одного ИМ в анамнезе, чел (%) | 31 (31%) |
| Перенесённый передний ИМ, чел (%) | 60 (60%) |
| Перенесённый нижний ИМ, чел (%) | 11 (11%) |
| Перенесенный циркулярный ИМ, чел (%) | 29 (29%) |
| Артериальная гипертензия, чел (%) | 65 (65%) |
| Длительность одышки, лет (М±s) | 3,4±3,0 |
| Длительность отёчного синдрома, лет (М±s) | 0,8±1,2 |
| Сердечная астма в анамнезе, чел (%) | 31 (31 %) |
| Отёк лёгких в анамнезе, чел (%) | 11 (11 %) |
| Постоянная форма ФП, чел (%) | 18 (18%) |
| Сопутствующие заболевания | |
| Острое нарушение мозгового кровообращения в анамнезе в анамнезе, чел.(%) | 10 (5%) |
| Сахарный диабет 2 типа (лёгкое и средне-тяжёлое течение, стадия компенсации), чел. (%) | 15 (7,4%) |
Таблица 2. Общая характеристика обследованных больных ХСН
на фоне РБС
| Возраст, годы (М±s) | 56,7±9,9 |
| Мужчины, чел (%) | 23 (23%) |
| Женщины, чел (%) | 77 (77%) |
| Сочетанный митральный порок, чел (%) | 54 (54%) |
| Комб митрально-аортальный порок, чел (%) | 46 (46%) |
| Преобладание митр. стеноза, чел (%) | 59 (59%) |
| Преобладанием митр. недостат., чел (%) | 41 (41%) |
| Бициллинопрофилактика, чел (%) | 44 (44%) |
| Операции (митр ком-томия) в анамнезе, чел (%) | 17 (17%) |
| Артериальная гипертензия, чел. (%) | 18 (18%) |
| Длительность одышки, лет (М±s) | 9,1±9,0 |
| Длительность отёчного синдрома, лет (М±s) | 1,3±2,2 |
| Сердечная астма в анамнезе, чел. (%) | 7 (7%) |
| Отёк лёгких в анамнезе, чел. (%) | 2 (2%) |
| Постоянная форма ФП, чел (%) | 54 (54%) |
| Пароксизмальная форма ФП, чел (%) | 15 (15%) |
| Экстрасистолия, чел (%) | 21 (21%) |
| Сопутствующие заболевания | - |
Изначально все пациенты были разделены на две большие группы: 1) ХСН на фоне ИБС: постинфарктного кардиосклероза и 2) ХСН на фоне РБС: митральных пороков сердца.
Пациенты с ХСН на фоне ИБС: постинфарктного кардиосклероза в соответствии с количеством баллов, набранных по ШОКС, были разделены на четыре подгруппы: I - менее 3 баллов (21 пациент), II - 3-6 баллов (25 пациентов), III - 7-9 баллов (27 пациентов), IV - более 9 баллов (25 пациентов). Пациенты с ХСН на фоне РБС также были разделены на четыре подгруппы: I – ХСН I-II ФК на фоне сочетанного митрального (или комбинированного митрально-аортального) порока с преобладанием митрального стеноза (МС) (27 пациентов); II - ХСН III-IV ФК на фоне сочетанного митрального (или комбинированного митрально-аортального) порока с преобладанием МС (30 пациентов); III - ХСН I-II ФК на фоне сочетанного митрального (или комбинированного митрально-аортального) порока с преобладанием митральной недостаточности (МН) (30 пациентов); IV - ХСН III-IV ФК на фоне сочетанного митрального (или комбинированного митрально-аортального) порока с преобладанием МН (13 пациентов).
Проанализировано лечение, которое больные получали на догоспитальном этапе. Практически не получали лекарственных препаратов 30% пациентов в группе ИБС и 38% - в группе РБС; -блокаторы использовали 38% пациентов в группе ИБС и 29% - в группе РБС; ингибиторы АПФ – 57% в группе ИБС и 25% в группе РБС; сердечные гликозиды – 16% в группе ИБС, 33% - в группе РБС; антикоагулянты – 17% в обеих группах, дезагреганты – 68% в группе ИБС, 35% - в группе РБС.
Катамнестическое наблюдение в динамике проведено у 108 больных ХСН через 18 месяцев после первичного обследования: у 53 пациентов с ИБС и 55 – с РБС. 16 пациентов умерли (13 – ИБС, 3 – РБС), у 60 пациентов был оценен весь комплекс инструментально-клинических показателей и у 32 пациентов состояние оценивалось по телефону в связи с невозможностью их приезда в клинику. Среди 92 выживших пациентов было выделено 2 группы: пациенты, состояние которых не ухудшилось (15 - ИБС, 34 – РБС) и пациенты, состояние которых ухудшилось (25 - ИБС, 18 – РБС). Ухудшение состояния оценивалось по клиническим показателям, в число которых входили: усиление одышки, слабости, появление/увеличение отёков нижних конечностей, сердцебиения, сердечной астмы, влажных хрипов в лёгких. Также у этих 107 пациентов оценены факторы прогноза при помощи многофакторных статистических моделей. Пациенты, наблюдавшиеся в динамике, получали стандартную терапию, состоявшую из средних терапевтических доз ингибиторов АПФ, -блокаторов, дигоксина, мочегонных препаратов. За время наблюдения их лечение существенным образом не менялось.
Всем больным проводилось комплексное обследование, включающее клиническое исследование крови, мочи, биохимических показателей, ЭКГ, рентгенографию грудной клетки.
2Д ЭхоКГ была проведена на аппарате Dornier AI 4800 (датчик 3,5 MHz). Исследование проводилось в М-режиме, В-режиме и режимах с использованием импульсно-волнового, постоянно-волнового и цветного допплеровского картирования. В М-режиме определялись: размер аорты, передне-задний размер левого предсердия (ЛП) в систолу и диастолу, митрально-септальная сепарация – EPSS - E-point septal separation - расстояние между передней створкой митрального клапана в точке движения Е и межжелудочковой перегородкой (у больных ИБС), толщина межжелудочковой перегородки (МЖП), толщина задней стенки ЛЖ в систолу и в диастолу, конечно-диастолический размер (КДР) ЛЖ, конечно-систолический размер (КСР) ЛЖ. В В-режиме определялись: площадь ЛП, поперечный размер правого предсердия (ПП), площадь митрального отверстия (планиметрический метод) (Sмо), поперечный размер ЛЖ в систолу и в диастолу, продольный размер ЛЖ в систолу и в диастолу, конечно-диастолический объем (КДО) ЛЖ, конечно-систолический объем (КСО) ЛЖ, фракция выброса (EF) ЛЖ (по методу Simpson), размер и фракция выброса правого желудочка (ПЖ) (по методу площадь-длина), оценивались нарушения локальной сократимости ЛЖ, структура и характер движения клапанов. В режиме цветного допплеровского картирования оценивались наличие и степень митральной, аортальной и трикуспидальной регургитаций. В режиме с использованием импульсно-волнового допплера определялись время изгнания из левого желудочка (ЕТ) и диастолические показатели: соотношение Е/А митрального и трикуспидального потоков, время изоволюмического сокращения и расслабления (IVCT и IRCT, соответственно), время замедления раннего наполнения (ВЗРН) ЛЖ. В режиме с использованием постоянно-волнового допплера определялись градиенты давления на митральном и аортальном клапанах, расчитывалось систолическое давление в лёгочной артерии (СДЛА) (с учётом скорости потока трикуспидальной регургитации). Исходя из значений вышеперечисленных показателей, расчитывались следующие параметры: 1) соотношение систолического и диастолического размеров левого предсердия – LAEF (left atrium eruption fraction);
2) систолический и диастолический индексы сферичности левого желудочка (ИСс, ИСд) – соотношение поперечного и продольного размеров ЛЖ в систолу и в диастолу соответственно;
3) систолический и диастолический миокардиальный стресс ЛЖ (МСс и МСд соответственно);
4) индексы КСРлж, КДРлж, КСОлж, КДОлж, Sмо (индексация проводилась к площади поверхности тела – Sпт);
5) относительная толщина стенок (ОТС) – отношение суммы толщины МЖП и задней стенки к КДРлж;
6) масса миокарда ЛЖ определялась по формуле Devereux с последующим индексированием к Sпт (ИММ);
7) интегральный систолический индекс ремоделирования (ИСИР) – соотношение фракции выброса ЛЖ и диастолического индекса сферичности ЛЖ;
8) интегральный диастолический индекс ремоделирования (ИДИР) – соотношение времени замедления раннего наполнения (ВЗРН) и диастолического индекса сферичности ЛЖ;
9) индекс напряжения миокарда (MPI – myocardial performance index) – отношение суммы IVCT и IVRT ко времени изгнания из левого желудочка (ЕТ);
10) индекс асинергии левого желудочка (ИА).
С учётом ИММ, индекса КДР и ОТС определялся вариант ремоделирования левого желудочка. Стадии диастолической дисфункции определялись согласно Национальным рекомендациям ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр) с учётом показателей: Е/А, ВЗРН, IVRT.
Количественное определение уровней мозгового и предсердного натрийуретических пептидов (МНП и ПНП соответственно) проводилось в лаборатории клинической иммунологии КНЦ РАМН методом конкурентного иммуноферментного анализа без экстракции с использованием стандартных наборов фирмы "Peninsula Laboratories" (США).
Данные обработаны при помощи пакета программ Statistica 6. Применялись: расчёт средних величин со стандартным отклонением, сравнение средних величин с расчётом t-критерия Стьюдента и оценкой его значимости р. За уровень достоверности статистических показателей принято р<0,05, в ряде случаев – р<0,001 (для решения проблемы множественных сравнений с использованием поправки Бонферрони). Также проводился расчет коэффициентов корреляции. При сравнении количественных признаков с нормальным распределением использовалась параметрическая статистика (метод Пирсона). При сравнении количественных признаков с распределением отличным от нормального, а также качественных порядковых признаков использовался метод ранговой корреляции по Спирмену. Для сравнения частот бинарных признаков использовался анализ четырёхпольных таблиц с применением критерия -квадрат. Нормальность распределения признаков оценивалась путём построения гистограмм распределения признаков. Кроме того, с целью выявления факторов прогноза в группе пациентов, обследованных в динамике, проводился многофакторный статистический анализ с помощью комплекса программ медико-биологической статистики "АСТА", разработанный в лаборатории медицинской кибернетики РОНЦ им. Н.Н.Блохина РАМН. Для каждого признака (клинического, эхокардиографического, лабораторного) определялись коэффициенты информативности Вапника-Червоненкиса. Использовалось построение решающих правил по методу Байеса, использующих различные наборы признаков. Формировались " обучающая" и "экзаменационная" выборки. Частота правильного определения группы (с учётом 95%-го доверительного интервала) служила оценкой качества решающего правила. Доверительные интервалы вычислялись с помощью биноминального распределения. Доверительный интервал для "лучшего правила из N правил" определялся по методу Бонферрони ("Учёт многократных сравнений").
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ОБСУЖДЕНИЕ
1. Клинико-инструментально-лабораторная характеристика пациентов
с ХСН на фоне ИБС
У всех пациентов с ХСН на фоне ИБС имелся постинфарктный кардиосклероз, подтверждённый данными ЭКГ и ЭхоКГ. Мягкая артериальная гипертензия в качестве сопутствующей патологии имелась у 65 пациентов (65%). Давность перенесённого инфаркта миокарда в среднем составила 7,1 (±5,0) лет. Аневризма левого желудочка, по данным ЭхоКГ, была выявлена у 41 (41%) пациента, из них у 23 пациентов (56%) был передне-перегородочный и у 18 (44%) – циркулярный инфаркт миокарда. Нарушения ритма выявлены у 56 (56%) и у 18 (18%) пациентов были представлены постоянной формой фибрилляции предсердий (ФП), у 5 (5%) пациентов - пароксизмальной формой ФП, у 15 (15%) пациентов - наджелудочковой и у 8 (8%) пациентов – желудочковой экстрасистолией. У 72 пациентов (72%) присутствовала ишемическая митральная регургитация, при этом у 20 пациентов (20%) площадь струи регургитации составляла 40% и более от площади ЛП.
Таблица 3. Клиническая характеристика обследованных больных
в соответствии с ФК ХСН
| ФК I | ФК II | ФК III | ФК IV | ||
| Давность симптомов НК, годы М±s | 2,8±1,7 | 2,7±1,7 | 3,6±2,5 | 4,6±2,6 | |
| Сердечная астма, чел (%) | 0 | 0 | 9 (36)* | 22 (82)* | |
| Отёк лёгких в анамнезе, чел (%) | 0 | 0 | 3 (12)* | 10 (37)* | |
| Количество госпитализаций за год, чел (%) | 0-1 | 21 (100) | 25 (93) | 18 (72) | 6 (22)* |
| 2-4 | - | 2 (7) | 7 (28) | 21 (78)* | |
| Одышка, чел (%) | 18 (85) | 27 (100) | 25 (100) | 27 (100) | |
| Пастозность/Отёки, чел (%) | 1 (7) | 9 (33)* | 21 (84)* | 24 (89)* | |
| Хрипы в лёгких, чел (%) | 0 | 7 (26)* | 17 (68)* | 24 (89)* | |
| Застой в МКК по данным R-графии, чел (%) | 4 (19) | 20 (74)* | 24 (96)* | 27 (100)* | |
| Кол-во ИМ в анамнезе, чел (%) | 1 | 19 (91) | 18 (67) | 15 (60) | 17 (63) |
| > 1 | 2 (9) | 9 (33) | 10 (40) | 10 (37) | |
| Дистанция, пройденная при тесте 6-мин ходьбы, метры М±s | 413±27 | 332±51 | 235±65 | 161±39 | |
| Наличие аневризмы ЛЖ, чел (%) | 3 (14) | 10 (37) | 8 (32) | 20 (74)* | |
| Число больных | 21 | 27 | 25 | 27 | |
*- р<0,05 при сравнении подгрупп ФК II-IV с ФК I.
При ЭхоКГ-исследовании признаки ремоделирования левого желудочка нами были выявлены у 87 (87%) пациентов. Уже на ранних стадиях развития ХСН отмечено преобладание эксцентрического (дезадаптивного) типа ремоделирования. Так, только у четверти больных (24%) с ФК I сохраняется нормальная геометрия левого желудочка, а эксцентрическое ремоделирование (с и без дилатации полости ЛЖ) составило 43% (Диаграмма 1). При более высоких ФК ХСН отмечался дальнейший рост числа случаев эксцентрического ремоделирования ЛЖ.

НГ - нормальная геометрия; КР – концентрическое ремоделирование; КГ – концентрическая гипертрофия; ЭГ без дЛЖ – эксцентрическая гипертрофия без дилатации левого желудочка;
ЭГ с дЛЖ – эксцентрическая гипертрофия с дилатацией левого желудочка
Диаграмма 1. Распределение типов ремоделирования левого желудочка
при ФК I ХСН
При оценке пациентов с эксцентрическим типом ремоделирования ЛЖ было отмечено преобладание среди них больных перенесших инфаркт миокарда (ИМ) передней стенки ЛЖ – 56%, по сравнению с 9% перенесших ИМ нижней стенки и 35% - циркулярный ИМ. Давность перенесённого ИМ при эксцентрическом ремоделировании была достоверно больше, чем у пациентов с концентрическими типами ремоделирования (8,1±6,8 и 4,9±3,3 соответственно, р=0,03). У 35% пациентов с ЭГ в анамнезе было более одного ИМ (по сравнению с 21% в группе с концентрическими формами ремоделирования). Также у пациентов с эксцентрическим типом ремоделирования достоверно чаще, чем при концентрическом типе встречались сердечная астма и отёк лёгких в анамнезе: 49% и 20% против 21% и 4%, соответственно, (р<0,05).
У 24 пациентов из обследованных 100 отмечалась изолированная диастолическая дисфункция (ДД), у остальных 76 – выявлена как диастолическая, так и систолическая дисфункция левого желудочка.

ЗР – замедленная релаксация, ПН – псевдонормализация, Р - рестрикция
Диаграмма 2. Характеристика диастолической дисфункции
при начальных стадиях развития ХСН (ФК I-II)
У больных с начальными проявлениями ХСН выявлено преобладание ДД по типу замедленной релаксации (Диаграмма 2). Поздние стадии ХСН, напротив, характеризовались большим числом случаев рестриктивного типа ДД. Так при ФК III ДД по типу замедленной релаксации ЛЖ составила 17%, рестриктивный тип – 44%, а при ФК IV замедленная релаксация – всего 13%, в то время как рестриктивный тип ДД – 52%.
У пациентов с более высоким ФК ХСН отмечены достоверно большие (р<0,05) значения таких показателей как: размер и площадь ЛП, LAEF, размеры и объёмы ЛЖ, EPSS, индексы сферичности, миокардиальный стресс, индекс асинергии, масса миокарда ЛЖ, индекс напряжения миокарда ЛЖ, соотношение Е/А митрального потока, СДЛА. Достоверно (р<0,05) меньшими были значения следующих параметров: фракция выброса левого и правого желудочков, соотношение УО/КСО, интегральные систолический и диастолический индексы ремоделирования левого желудочка и др. (Таблица 4).
Таблица 4. Средние значения эхокардиографических
показателей при различных ФК ХСН и в группе сравнения, М±s
| Гр сравн | I ФК | II ФК | III ФК | IV ФК | |
| Sлп, см2 | 20,3±3,5 | 22,4±0,9* | 25,2±5,4 * | 29,2±4,1* | 34,6±7,4 * |
| LAEF | 0,69±0,07 | 0,8±0,08 ** | 0,80±0,04 | 0,86±0,05** | 0,90±0,04* |
| иКДО, мл/м2 | 56±9 | 74±20** | 93±32 * | 111±42 | 122±37* |
| иКСО, мл/м2 | 18±3 | 39±16 ** | 55±27* | 69±32 | 85±30* |
| УО/КСО | 2,2±0,5 | 0,92±0,3** | 0,85±0,4 | 0,83±0,6 | 0,54±0,3* |
| ИСд | 0,59±0,05 | 0,69±0,04** | 0,71±0,07 | 0,77±0,06* | 0,78±0,05 |
| ИСс | 0,50±0,05 | 0,60±0,05** | 0,62±0,07 | 0,68±0,07* | 0,73±0,04* |
| EF ЛЖ % | 68±5 | 48±10** | 44±11 | 40±10 | 32±11* |
| EF ПЖ % | 68±8 | 58±11** | 53±14 | 44±14* | 40±14 |
| МСс, г/см2 | 115±9 | 163±38 ** | 182±38 | 186±39 | 209±35* |
| ИСИР | 113±11 | 70±17** | 62±20 | 52±17 | 42±15* |
| ИА | 1±0 | 1,34±0,24** | 1,50±0,36 | 1,66±0,37 | 2,1±0,4** |
| ИММ, г/м2 | 86±13 | 120±27** | 146±36* | 160±47 | 165±41 |
| MPI | 0,45±0,07 | 0,55±0,08** | 0,56±0,13 | 0,66±0,11* | 0,67±0,11 |
| Е/Амк | 1,23±0,2 | 0,89±0,3** | 0,99±0,5 | 1,77±0,9** | 2,1±0,7 |
| ИДИР | 0,36±0,04 | 0,32±0,08* | 0,28±0,08 | 0,24±0,06* | 0,21±0,08 |
*- р<0,05; **- р<0,001 при сравнении последующей и предыдущей групп
Таким образом, уже при I ФК увеличивается размер ЛП со снижением его сократительной функции, увеличиваются систолические и диастолические размеры и объёмы ЛЖ, снижается EF ЛЖ, растёт индекс напряжения миокарда (MPI), ухудшается диастолическая функция ЛЖ. Обращает на себя внимание, что такие показатели как систолический индекс сферичности, соотношение УО/КСО, интегральный систолический индекс ремоделирования, систолический миокардиальный стресс также изменяются уже на ранних этапах развития ХСН (р<0,001 при сравнении группы ФК I и группы пациентов без ХСН).
Далее мы оценили взаимосвязь ЭхоКГ-параметров в частности с такой клинической характеристикой как количество баллов по ШОКС (Таблица 5).
Таблица 5. Коэффициенты корреляции со статусом больного,
оцененным по ШОКС
| ЛП | 0,56 (р<0,0001) | МСс | 0,39 (р<0,0001) |
| Sлп | 0,60 (р<0,0001) | МСд | 0,28 (р=0,005) |
| LAEF | 0,61 (р<0,0001) | EPSS | 0,52 (р<0,0001) |
| ИСс | 0,61 (р<0,0001) | ИММ | 0,33 (р=0,001) |
| ИСд | 0,51 (р<0,0001) | Тип ДД лж | 0,65 (р<0,0001) |
| EFлж | -0,48 (р<0,0001) | ВЗРН | -0,52 (р<0,0001) |
| иКДО | 0,46 (р<0,0001) | ИДИР | -0,54 (р<0,0001) |
| иКСО | 0,54 (р<0,0001) | MPI | 0,47 (р<0,0001) |
| ИСИР | -0,53 (р<0,0001) | IVRT | -0,42 (р<0,0001) |
| ИА | 0,58 (р<0,0001) | СДЛА | 0,52 (р<0,0001) |
| EFпж | -0,48 (р<0,0001) | МР | 0,57 (р<0,0001) |
Таким образом, наибольшая степень корреляции тяжести ХСН была отмечена с маркерами ДД (r=0,65), в том числе - соотношением КСР/КДРлп (LAEF) (r=0,61). Это соответствует данным литературы: по мнению Беленкова Ю.Н. и соавт. (2002) диастолические маркёры точнее систолических отражают функциональное состояние миокарда и его резерв. Так же по данным Агеева Ф.Т. с соавт. (1995) толерантность к физическим нагрузкам в большей степени коррелирует с рестриктивным нарушением диастолической функции, чем с систолической дисфункцией. Это ещё раз подтверждает необходимость более тщательной оценки показателей ДД у пациентов с патологией сердца и, в частности, с ИБС. Также отмечена корреляция с конечными систолическими размером и объёмом (r=0,54), ИА ЛЖ (r=0,58), наличием и степенью выраженности МР (r=0,57), EPSS, ИСИР. В то время как корреляция тяжести состояния с фракцией выброса ЛЖ была менее выраженной (r=-0,48). По нашему мнению необходимо обратить внимание на высокую значимость митральной регургитации в определении тяжести проявлений ХСН. Учитывая, что это потенциально обратимый фактор, пациентам следует активно рекомендовать хирургическую коррекцию митральной недостаточности III-IV степени.
Во многих источниках предлагается использование индекса напряжения миокарда (MPI, Tei-индекс) для оценки тяжести ХСН [Рыбакова, 2002, Барт, 2006, Lind, 2005]. По мнению авторов MPI позволяет связать систолическую и диастолическую функции левого желудочка. По нашим данным корреляция выраженности ХСН с этим показателем была достаточно умеренной: r=0,47, p<0,0001 в группе ИБС. Тем не менее, его использование целесообразно для комплексной оценки ремоделирования ЛЖ, особенно на ранних этапах развития ХСН. Так, в группе пациентов с ИБС с количеством баллов по ШОКС<3 и EFлж50% MPI составил 0,52±0,07 (в группе сравнения – 0,45±0,07). Это согласуется с данными литературы. Так, по мнению Bruch с соавт. (2000) значение MPI выше 0.47 может быть использовано для диагностики застойной сердечной недостаточности, также авторы указывают, что MPI является чувствительным индикатором мягкой (умеренной) сердечной недостаточности.
При оценке уровня МНП в подгруппе с начальными проявлениями ХСН (менее 3 баллов по ШОКС) он существенно не отличался от группы сравнения. По мере прогрессирования ХСН уровень МНП увеличивался, резко возрастая в подгруппе 7-9 баллов по ШОКС. На фоне тяжёлой ХСН с количеством баллов по ШОКС более 9 отмечалась тенденция к снижению уровня МНП (статистически недостоверная) (Диаграмма 3), что, по-видимому, объясняется выраженным уменьшением количества жизнеспособного миокарда, являющегося источником продукции МНП [Phillips R, 1991].

1. Группа сравнения; 2. Менее 3 баллов; 3. От 3 до 6 баллов; 4. От 7 до 9 баллов. 5. Более 9 баллов.
| Гр.ср.-менее 3 б | менее 3 б - 3-6 б | 3-6 б – 7-9 б | 7-9 б –более 9 б | |
| МНП | р<0,05 | р<0,05 | р<0,001 | р>0,05 |
Диаграмма 3. Уровень МНП в зависимости от баллов,
набранных по ШОКС
Уровень МНП достоверно коррелировал с клиническими показателями тяжести состояния пациента (ШОКС, тест 6-минутной ходьбы, наличие сердечной астмы, R-признаки застоя в малом круге кровообращения), а также с большинством маркёров систолической и диастолической дисфункции ЛЖ. Кроме того, отмечена существенная корреляция с размерами правых отделов, диастолической дисфункцией ПЖ, степенью МР и СДЛА. Следует отметить, что корреляция МНП с клинической выраженностью ХСН (ШОКС) была сопоставимой с эхокардиографическими показателями: тип ДД – 0,65, ИСс – 0,61, ИСИР - -0,53, EFлж - -0,48 (р<0,0001), по сравнению с МНП – 0,66 (р<0,0001).
Однако, как и по данным ряда авторов [Bibbins, 2004; Tang, 2003], значения МНП у наших пациентов характеризовались широким разбросом. Так, у двоих пациентов с III ФК ХСН уровень МНП был менее 100 пг/мл. У половины пациентов (11 из 21) с ШОКС<3 баллов МНП также был в пределах нормы (менее 100 пг/мл), а в группе из 8 пациентов с ШОКС<3 баллов и EF50% уровень МНП превышал 100 пг/мл только в одном случае. Это указывает на необходимость комплексного подхода к диагностике ХСН (особенно, ранних этапов), включающего не только лабораторные, но и клинико-инструментальные методики.
При оценке уровня ПНП существенных корреляций с клиническими и ЭхоКГ-характеристиками, а также существенных отличий его уровня у пациентов с ХСН в сопоставлении с группой сравнения не отмечено.
Для выявления наиболее ранних эхокардиографических и биохимических маркёров ХСН мы отдельно охарактеризовали группу пациентов (8 человек) с начальным этапом развития ХСН (количество баллов по ШОКС<3) и отсутствием систолической дисфункции (EFлж50%).
Таблица 6. Оценка ЭхоКГ и биохимических маркёров у пациентов с начальными проявлениями ХСН и сохранённой систолической функцией ЛЖ, М±s.
| Гр сравн | ШОКС<3 EF50% | Гр сравн | ШОКС<3 EF50% | ||
| Sлп, см2 | 20,3±3,5 | 19,8±2,9 | EF ЛЖ % | 68±5 | 59±8* |
| LAEF | 0,69±0,07 | 0,83±0,07** | МСс г/см2 | 115±9 | 139±25** |
| иКСР | 1,6±0,2 | 1,8±0,2* | ИСИР | 113±11 | 88±13** |
| иКДО | 56±9 | 57±12 | EF/MCc | 0,62±0,06 | 0,44±0,15** |
| иКСО | 18±3 | 22±6* | ИММ | 86±13 | 118±25** |
| УО/КСО | 2,2±0,5 | 1,3±0,2** | Е/Амк | 1,23±0,2 | 1,16±0,4 |
| ИСд | 0,59±0,05 | 0,67±0,10* | MPI | 0,45±0,07 | 0,52±0,08* |
| ИСс | 0,50±0,05 | 0,56±0,03* | МНП, нг/мл | 0,023±0,02 | 0,062±0,10* |
| Число б-х | 30 | 8 | 30 | 8 |
*- р<0,05; ** - р<0,001
Представляется важным повышение ИСс до увеличения объёмов ЛЖ и снижения фракции выброса. Так, в указанной группе пациентов ИСс составил 0,56±0,03 (при норме до 0,50), а иКСО, иКДО и ИСд были в пределах нормы. При обзоре литературы использование ИСс для оценки ремоделирования левого желудочка встречается очень редко, с этой целью принято использовать ИСд, который, по мнению многих авторов, является более информативным показателем, чем фракция выброса, размеры и объёмы ЛЖ [Бойцов С.А, 2005, Mannaerts HF, 2004, Kleber FX, 1992]. В той же группе пациентов МСс составил 139±25, что на 17,3% превышает показатели группы сравнения. ИСИР у этих пациентов составил 87±13 (на 23% меньше, чем в группе сравнения), LAEF – 0,83 (на 17% больше, чем в группе сравнения). Таким образом, ИСс, МСс, ИСИР и LAEF, по-видимому, являются одними из наиболее ранних эхокардиографических маркёров сердечной недостаточности у пациентов с ИБС.
Также мы оценили взаимосвязь ряда эхокардиографических параметров и уровня МНП с такими клиническими проявлениями ХСН как одышка, аускультативные признаки застоя в малом круге кровообращения (хрипы в лёгких), отёки н/конечностей (Таблица 7).
Таблица 7. Взаимосвязь ЭхоКГ-параметров и уровня МНП
с клиническими проявлениями ХСН
| МНП | Sлп | иКСО | иКДО | EF | ИСс | ИСд | ИСИР | СДЛА | МР | Тип ДД | |
| Одышка | 0,32 | 0,41 | 0,27 | 0,23 | -0,25 | 0,40 | 0,38 | -0,32 | 0,38 | 0,45 | 0,40 |
| Хрипы | 0,63 | 0,53 | 0,39 | 0,34 | -0,36 | 0,46 | 0,47 | -0,42 | 0,20 | 0,35 | 0,49 |
| Отеки | 0,50 | 0,53 | 0,22 | - | -0,24 | 0,33 | 0,32 | -0,29 | 0,40 | 0,26 | 0,43 |
р<0,01
Таким образом, можно отметить, что уровень МНП, степень диастолической дисфункции, площадь ЛП и ИСс в наибольшей степени соответствовали выраженности клинических симптомов. Корреляция фракции выброса ЛЖ с клиническими проявлениями ХСН была менее выраженной.
В динамике (через 18 месяцев) прослежено состояние 53 пациентов: 9 пациентов с ФК I, 12 пациентов с ФК II, 13 пациентов с ФК III и 19 пациентов с ФК IV. Были выделены три группы пациентов:
1. Состояние не ухудшилось - 15 больных;
2. Состояние ухудшилось - 25 больных;
3. Скончалось - 13 пациентов.
Из выживших больных у 30 пациентов оценивался весь спектр клинических и эхокардиографических данных (Таблица 8), состояние 10 пациентов оценивалось по телефону в связи с тяжестью их состояния и невозможностью приехать в клинику для контрольного обследования.
Таблица 8. Изменение клинических и эхокардиографических параметров
в динамике, М±s
| Исходно | В динамике | % | Исходно | В динамике | % | ||
| ШОКС, б | 5,8±3,7* | 7,9±4,0 | +26,6 | МСс | 192±45* | 220±60 | +12,7 |
| 6-мин ходьба, метры | 287±92** | 225±88 | -21,6 | МСд | 277±49* | 320±81 | +13,4 |
| Одышка в баллах (1-3) | 1,18±0,4* | 1,44±0,5 | +18,1 | ИСИР | 51±17 | 45±17 | -11,8 |
| Отёки в баллах (1-3) | 0,93±0,5 | 1,05±0,6 | +11,4 | EF/MCc | 0,21±0,09* | 0,16±0,09 | -23,8 |
| Хрипы в баллах (1-3) | 0,53±0,4* | 0,84±0,4 | +36,9 | EFпж % | 50±15 | 44±14 | -12,0 |
| Sлп, см2 | 28±6,3* | 32±9,0 | +12,5 | Е/Амк | 1,27±0,8** | 1,88±0,9 | +32,4 |
| иКСР, см/м2 | 2,9±0,6 | 3,2±0,8 | +9,4 | ИДИР | 0,25±0,06** | 0,18±0,04 | -28,0 |
| ИСс | 0,63±0,08** | 0,69±0,06 | +8,7 | МР, б | 1,3±1,0 | 1,7±0,9 | +23,5 |
| EFлж % | 37±8,8 | 33±9,0 | -10,8 | СДЛА, mm Hg | 26±11* | 33±14 | +21,2 |
*-р<0,05; **-р<0,01
Таким образом, в динамике через 18 месяцев увеличилась выраженность одышки и застойных явлений в лёгких по данным аускультации, снизилась толерантность к физической нагрузке, оцениваемая по тесту 6-минутной ходьбы, увеличилось количество баллов, набранных по ШОКС. Из эхокардиографических показателей наиболее существенно увеличились площадь ЛП (+12,5%), систолический и диастолический миокардиальный стресс ЛЖ (+12,7 и 13,4% соответственно), соотношение Е/А на митральном клапане (+32,4%), выраженность МР (+23,5%), СДЛА (+21,2%). Уменьшились EF левого (-10,8%) и правого (-12%) желудочков, соотношение EFлж/МСс (-23,8%), интегральные систолический и диастолический индексы ремоделирования (-11,8 и 28% соответственно). Особенно высокая достоверность отмечена в изменении таких показателей как: дистанция, пройденная при тесте 6-минутной ходьбы, ИСс ЛЖ и в ряде диастолических показателей (соотношение Е/А, ИДИР). Исходя из этих данных, можно судить о том, что ухудшение состояния пациентов в немалой степени было связано с нарастанием диастолической дисфункции ЛЖ и лёгочной гипертензии. Этот факт необходимо учитывать при выборе стратегии лечения пациентов с ХСН на фоне ИБС.
При оценке уровня МНП в выше указанных трёх группах пациентов (состояние которых не изменилось, либо ухудшилось, либо, они скончались в течение последующих 18 мес) были получены следующие данные (Диаграмма 4). Таким образом, последующая динамика состояния пациента в значительной степени зависела от уровня МНП, определённого при первичном обследовании пациента.

1 – состояние не изменилось; 2 – состояние ухудшилось; 3 - скончались
р<0,05 при сравнении групп между собой
Диаграмма 4. Уровень МНП в зависимости от последующей динамики
состояния пациента
С помощью многофакторного анализа мы попытались определить прогностические факторы, совокупность которых может влиять на динамику состояния пациента. С этой целью для каждого признака были определены коэффициенты информативности Вапника-Червоненкиса. Затем по методу Байеса была выбрана совокупность 15 параметров, позволяющих предсказывать динамику состояния пациента, в том числе вероятность летального исхода в течение последующих 18 месяцев. К этим параметрам по нашим данным относятся: 1) количество баллов по ШОКС более 9; 2) дистанция по тесту 6-минутной ходьбы менее 150 м; 3) наличие сердечной астмы; 4) наличие гидроторакса; 5) давность перенесённого инфаркта более 10 лет; 6) количество госпитализаций в год – 3 и более; 7) давность отёчного синдрома более двух лет; 8) иКСО > 80 мл/м2; 9) ИСд > 0,8; 10) ИСИР < 60; 11) EPSS > 20 мм; 12) рестриктивный тип ДД; 13) ИДИР < 0,23; 14) митральная регургитация 40% от Sлп; 15) уровень МНП > 0,5 нг/мл.
2. Клинико-инструментально-лабораторная характеристика пациентов
с ХСН на фоне митральных пороков сердца ревматической этиологии
У всех больных РБС имелся сочетанный митральный порок. Сопутствующий гемодинамически малозначимый аортальный порок (АР I, max Pgav 15 mm Hg) был у 50 больных из 100 (50%). Нарушения ритма были в основном представлены постоянной (54 пациента – 54%) или пароксизмальной (15 пациентов – 15%) формой фибрилляции предсердий. У 17 пациентов (17%) в анамнезе была митральная комиссуротомия (других оперативных вмешательств на сердце не было).
Таблица 9. Клиническая характеристика обследованных больных
в соответствии с ФК ХСН
| Сочетанный МП с преобладанием стеноза | Сочетанный МП с преобладанием недостаточности | ||||
| I-II ФК | III-IV ФК | I-II ФК | III-IV ФК | ||
| Давность выявления порока (годы) М±s | 33±15 | 37±15 | 23±15 | 30±19 | |
| Давность симптомов НК (годы) М±s | 7,7±6,4 | 11,7±9,7 | 7,5±6,8 | 8,5±8,1 | |
| Количество госпитализаций за год | 0, чел (%) | 15 (56) | 7 (23)* | 26 (87) | 2 (15)* |
| 1, чел (%) | 12 (44) | 23 (67)* | 4 (13) | 11 (85)* | |
| Сердечная астма, чел (%) | 0 | 5 (16)* | 0 | 2 (15)* | |
| Бициллинопрофилактика, чел (%) | 12 (44) | 11 (33) | 15 (50) | 5 (38) | |
| Одышка, чел (%) | 26 (95) | 30 (100) | 30 (100) | 13 (100) | |
| Пастозность/Отёки, чел (%) | 8 (29) | 23 (67) | 5 (16) | 10 (77)* | |
| Хрипы в лёгких. чел (%) | 3 (10) | 14 (42)* | 1 (3) | 6 (46)* | |
| Застой в МКК по данным R-графии, чел (%) | 19 (70) | 30 (100) | 6 (20) | 13 (100)* | |
| Митр. комиссуротомия, чел (%) | 3 (11) | 6 (20) | 7 (23) | 1 (8) | |
| Число больных | 27 | 30 | 30 | 13 | |
* - р<0,05 при сравнении подгрупп ФК III-IV с подгруппами ФК I-II
При обследовании пациентов с ХСН на фоне ревматических пороков сердца признаки ремоделирования ЛЖ были выявлены у 61 (61%) пациента. Как при МС, так и при МН отмечено преобладание концентрических (адаптивных) форм ремоделирования ЛЖ, в том числе у пациентов с высокими ФК ХСН (Диаграммы 5 и 6).

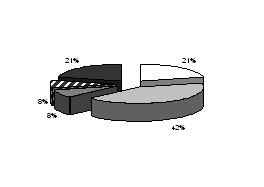
ФК I-II ФК III-IV
Диаграмма 5. Распределение типов ремоделирования при
сочетанном МП с преобладанием стеноза I-II и III-IV ФК ХСН


ФК I-II ФК III-IV
Диаграмма 6. Распределение типов ремоделирования при
сочетанном МП с преобладанием недостаточности I-II и III-IV ФК ХСН
Такой адаптивный характер ремоделирования ЛЖ наряду с другими факторами, возможно, играет роль в более плавном развитии ХСН у пациентов с ревматическими пороками сердца по сравнению с ХСН другой этиологии.
При оценке средних эхокардиографических показателей в группе ревматических пороков сердца с преобладанием МС I-II ФК ХСН наиболее существенно по сравнению с пациентами без ХСН отличались следующие показатели (не считая иSмо, PGmv, МР, СДЛА): Sлп (+34%), соотношение EFлж/МСс (-28%), ПП (+26%), ИСИР (-21%) и МСс (+21%). В группе с преобладанием МН I-II ФК ХСН наиболее существенно отличались те же показатели, что и при преобладании стеноза, но в меньшей степени: Sлп (+29%), соотношение EFлж/МСс (-23%), ПП (+23%), ИСИР (-18%) и МСс (+17%), кроме того, была больше масса миокарда ЛЖ (ИММ +17% в отличие от группы с преобладанием стеноза - +6%).
Пациенты с более тяжёлыми проявлениями ХСН (ФК III-IV) характеризовались большими размерами предсердий и массы миокарда ЛЖ, снижением сократительности ЛП и ПЖ, уменьшением IVRT ЛЖ (что, возможно, свидетельствует об ухудшении диастолической функции ЛЖ), большей степенью МР и лёгочной гипертензии. Такие показатели как размеры и объёмы ЛЖ, EF ЛЖ менялись менее существенно (Таблица 10).
Таким образом, при преобладании МС отмечается более выраженное ремоделирование сердца, чем при преобладании МН. Возможно, это обусловлено более тяжёлым пороком в группе с преобладанием стеноза.
Таблица 10. Средние значения ЭхоКГ-показателей
у пациентов с РБС, М±s
| Группа сравнения | Сочетанный митральный порок с преобладанием стеноза | Сочетанный митральный порок с преобладанием недостат. | |||
| I-II ФК | III-IV ФК | I-II ФК | III-IV ФК | ||
| ЛП, см | 3,6±0,4 | 5,1±0,6** | 6,1±2,0 | 4,8±1,0** | 5,6±0,8* |
| Sлп, см2 | 20,3±3,5 | 30,8±6,0** | 38,5±12,0* | 28,5±7,0** | 37±7,5** |
| LAEF | 0,69±0,07 | 0,81±0,04** | 0,88±0,02** | 0,79±0,04** | 0,88±0,05** |
| иSмо, см/м2 | 2,9±0,05 | 1,16±0,2** | 1,01±0,2* | 1,83±0,3** | 1,77±0,2 |
| ПП, см | 3,1±0,3 | 4,2±0,7** | 4,6±0,9 | 4,0±0,6** | 4,8±0,9** |
| иКДР, см/м2 | 2.6±0,2 | 2,7±0,2 | 2,9±0,4 | 2,8±0,3 | 2,7±0,3 |
| иКСР, см/м2 | 1,6±0,2 | 1,8±0,2* | 2,0±0,4 | 1,9±0,3** | 1,9±0,2 |
| иКДО, мл/м2 | 56±9 | 58±10 | 66±25 | 65±13* | 65±15 |
| иКСО, мл/м2 | 18±3 | 24±8 | 31±17 | 26±9** | 26±7 |
| ИСд | 0,60±0,04 | 0,67±0,05** | 0,71±0,08 | 0,66±0,07** | 0,68±0,08 |
| ИСс | 0,49±0,05 | 0,59±0,06** | 0,62±0,09 | 0,56±0,06** | 0,59±0,05 |
| EF ЛЖ% | 68±5 | 59±10* | 56±11 | 61±7 | 59±8 |
| МСс, г/см2 | 113±10 | 143±27** | 132±26 | 136±24** | 134±9 |
| EF/MCc | 0,6±0,06 | 0,43±0,13** | 0,45±0,15 | 0,46±0,12** | 0,44±0,06 |
| ИСИР | 112±11 | 89±18** | 80±17 | 92±18** | 88±12 |
| ИММ, г/м2 | 86±13 | 92±14 | 114±36* | 104±20** | 112±26 |
| IVRT, ms | 88±11 | 85±18 | 66±19** | 88±21 | 74±13* |
| ПЖ, см | 2,8±0,3 | 3,3±0,5** | 3,4±0,6 | 3,2±0,5** | 3,5±0,6 |
| EF ПЖ% | 69±9 | 58±13* | 46±13** | 59±18* | 50±13 |
| MPI | 0,45±0,07 | 0,56±0,1** | 0,59±0,1 | 0,56±0,1** | 0,62±0,08 |
| MP,баллы | 0 | 1,7±0,8** | 2,5±1,0** | 2,0±0,7** | 2,9±1,1* |
| MaxPGmv, mm Hg | 3,1±0,05 | 14,1±6** | 16,8±8 | 9,8±3,7** | 12,2±3,6* |
| СДЛА, mm Hg | 20±5 | 38±13** | 49±18* | 28±10** | 45±20** |
*- р<0,01, **- р<0,001 при сравнении пациентов с ФК I-II с группой сравнения и пациентов с ФК III-IV с пациентами с ФК I-II.
Как известно, традиционная оценка диастолической функции ЛЖ по трансмитральному потоку при митральном стенозе невозможна в связи с исходно повышенным давлением в ЛП, однако, косвенно судить о ДД ЛЖ можно по времени изоволюмического расслабления ЛЖ [Hess O.M, 1991]. Таким образом, снижение IVRT в обеих группах (преобладание МС и преобладание МН) может свидетельствовать об ухудшении ДД ЛЖ по мере прогрессирования порока. Обращает на себя внимание снижение систолической функции правого желудочка, что связано с его ремоделированием.
При оценке взаимосвязи клинического состояния пациентов с ревматическими пороками сердца (количество баллов по ШОКС) с различными эхокардиографическими параметрами наибольшая корреляция отмечена с СДЛА (r=0,62), LAEF (r=0,67), размерами ЛП и ПП (r=0,53), ИСс ЛЖ, иSмо (r=-0,38), PGmv (r=0,38) и выраженностью МР (r=0,41), IVRT ЛЖ (r=-0,42); EF и размером ПЖ (r=-0,42) (Таблица 11). Показатель LAEF (фракция опорожнения левого предсердия) был предложен Kurtoglu N с соавт. в 2000 г для оценки диастолической функции ЛЖ у пациентов с ИБС и артериальной гипертензией. В других работах использования этого показателя нам не встретилось. У пациентов с ревматическими пороками сердца при наличии митрального стеноза LAEF, по-видимому, зависит от эффективной площади митрального отверстия и косвенно отражает степень сопротивления потоку. Учитывая достаточно высокую корреляцию с клиническим состоянием пациента этот показатель может использоваться как дополнение к традиционным показателям (PGmv, Smv, PHT). Недостатком LAEF является возможность его использования только при синусовом ритме.
Таблица 11. Коэффициенты корреляции со статусом больного,
оцененным по ШОКС
| Sлп | 0,47 (р=0,0001) | КСРлж | 0,20 (р=0,04) |
| maxPGmv | 0,38 (р=0,0001) | EFпж | -0,42(р=0,0001) |
| иSмо | -0,38 (р=0,0001) | ПЖ | 0,38 (р=0,0001) |
| ПП | 0,53 (р=0,0001) | MPI | 0,34 (р=0,0001) |
| LAEF | 0,67 (р=0,0001) | IVRT | -0,42 (р=0,0001) |
| ИСс | 0,27 (р=0,007) | СДЛА | 0,62 (р=0,0001) |
| EFлж | -0,25 (р=0,01) | МР | 0,41 (р=0,0001) |
Значимая корреляция тяжести состояния пациента с систолическим давлением в лёгочной артерии и размером ПП определяет ведущую роль лёгочной гипертензии в прогрессировании ХСН у пациентов с митральными пороками сердца. Корреляция с площадью ЛП была более существенной, чем с традиционно используемым поперечным размером ЛП (0,47 и 0,44, соответственно), что указывает на целесообразность использования Sлп в протоколах эхокардиографического исследования. Обращает на себя внимание также наличие корреляции тяжести ХСН при РБС с диастолическим показателем IVRT.
Прослежены уровни МНП и ПНП в зависимости от выраженности сердечной недостаточности (ФК ХСН), подтверждённой количеством баллов, набранных по шкале Мареева и тестом 6-минутной ходьбы, а также в зависимости от характера порока (Диаграмма 7).

1- Группа сравнения. 2-Преобладание МС ФК I-II. 3- Преобладание МН ФК I-II. 4- Преобладание МС ФК III-IV. 5-Преобладание МН ФК III-IV.
Достоверность различий с группой сравнения: подгруппа 2 – р<0,05; подгруппа 4 – р<0,001; подгруппа 3 – р>0,05; подгруппа 5 – р<0,05.
Диаграмма 7. Уровень МНП у пациентов с ревматическими пороками сердца.
В подгруппе с преобладанием МС и ФК I-II уровень МНП составил 76±80 пг/мл (превышение 100 пг/мл в 3 случаях из 8). В подгруппе с преобладанием МН при ФК I-II не было отмечено ни одного случая повышения МНП больше нормы (20±19 пг/мл). Таким образом, можно отметить, что существенное повышение МНП (333±250) отмечалось лишь у пациентов с ХСН III-IV ФК на фоне выраженного сочетанного митрального порока с преобладанием стеноза, что, по-видимому, объясняется более выраженным пороком у пациентов этой подгруппы. В целом, в группе РБС уровень МНП превышал 100 пг/мл в 14 случаях из 41 (12 – преобладание стеноза, 2- преобладание недостаточности). При этом существенное повышение показателя (более 500 пг/мл), рекомендуемое в литературе в качестве достоверного критерия сердечной недостаточности (Weber M, 2006) отмечалось только у пяти пациентов с терминальной ХСН, двое из которых скончались в течение 6 месяцев наблюдения от прогрессирования сердечной недостаточности. Это указывает на сомнительную диагностическую ценность МНП у пациентов с ревматическими митральными пороками сердца. Как и в случае группы ИБС у пациентов с РБС не было зафиксировано достоверных изменений уровня ПНП на фоне ХСН при сопоставлении с группой сравнения, за исключением снижения уровня этого пептида у пациентов с преобладанием митральной недостаточности и III-IV ФК ХСН.
При оценке корреляции уровня натрийуретических пептидов с ЭхоКГ-показателями у пациентов с ревматическими пороками сердца существенная корреляция уровня МНП отмечена лишь с количеством баллов по ШОКС и дистанцией по тесту 6-минутной ходьбы, Sлп, степенью лёгочной гипертензии и EF ПЖ (Таблица 12).
Таблица 12. Коэффициенты корреляции МНП
| Параметр | Коэфф. корреляции | Параметр | Коэфф. корреляции |
| ШОКС | 0,49 (р=0,001) | иSмо | -0,35 (р=0,02) |
| Тест 6 мин-ходьбы | -0,40 (р=0,01) | MaxPGmv | 0,37 (р=0,02) |
| Sлп | 0,45 (р=0,003) | СДЛА | 0,53 (р=0,0004) |
| EF ПЖ | -0,42 (р=0,007) | МР | 0,36 (р=0,02) |
Также как и в группе ИБС мы оценили взаимосвязь ряда эхокардиографических параметров и уровня МНП с такими клиническими проявлениями ХСН как одышка, аускультативные признаки застоя в малом круге кровообращения (хрипы в лёгких), отёки н/конечностей (Таблица 13).
Таблица 13. Корреляция уровня МНП и ряда ЭхоКГ-параметров
с клиническими проявлениями ХСН
| МНП | Sлп | иSмо | MaxPgmv | ПП | ИСс | ИСИР | СДЛА | МР | |
| Одышка | 0,47 | 0,36 | -0,28 | 0,38 | 0,38 | - | - | 0,36 | 0,30 |
| Хрипы | - | 0,26 | - | - | 0,27 | 0,20 | - | - | 0,24 |
| Отеки | 0,33 | 0,40 | - | - | 0,48 | 0,24 | -0,21 | 0,48 | 0,28 |
р<0,05
Таким образом, одышка у пациентов с ХСН на фоне ревматических митральных пороков сердца коррелировала с уровнем МНП, размерами предсердий, пиковым градиентом на митральном клапане, СДЛА. Отёки нижних конечностей также коррелировали с размерами предсердий и степенью лёгочной гипертензии, в то время как корреляция аускультативных признаков застоя в малом круге кровообращения с ЭхоКГ-показателями была достаточно слабой, а с уровнем МНП её не прослеживалось вообще.
В группе РБС в динамике (через 18 месяцев) прослежено состояние 55 пациентов: 14 пациентов с ФК I-II и преобладанием МС, 19 пациентов с ФК III-IV и преобладанием МС, 15 пациентов с ФК I-II и преобладанием МН, 7 пациентов с ФК III-IV и преобладанием МН.
Были выделены четыре группы пациентов (объектов):
1. Состояние не ухудшилось - 30 больных;
2. Состояние ухудшилось - 18 больных;
3. Скончалось - 3 пациента;
4. Прооперировано (протезирование митрального клапана) – 4 пациента.
Из выживших больных у 30 оценивался весь спектр клинических и эхокардиографических данных (Таблица 14), состояние 22 пациентов оценивалось по телефону в связи с невозможностью их приезда в клинику для контрольного обследования.
Таблица 14. Изменение клинических и эхокардиографических параметров
в динамике, М±s
| Исходно | В динамике | % | Исходно | В динамике | % | ||
| ШОКС, б | 5,0±2,9 | 5,6±3,2 | +10,7 | иКСР, см/м2 | 1,91±0,3 | 1,92±0,3 | +0,5 |
| 6-мин ходьба, метры | 324±83 | 294±99 | -9,3 | EFлж % | 59±10 | 58±10 | -1,7 |
| Одышка в баллах (1-3) | 1,00±0,0 | 1,15±0,3 | +13,0 | МСс | 127±23 | 140±26* | +9,3 |
| Отёки в баллах (1-3) | 0,68±0,4 | 0,68±0,5 | 0 | EF/MCc | 0,50±0,1 | 0,43±0,1* | -14 |
| Хрипы в баллах (1-3) | 0,21±0,1 | 0,42±0,2** | +50,0 | Е/Атк | 1,2±0,3 | 0,87±0,2** | -27,5 |
| Sлп, см2 | 31±7,1 | 35±8,0* | +11,4 | МР | 1,6±0,9 | 2,0±0,9 | +20 |
| иSмо, см/м2 | 1,39±0,2 | 1,32±0,3 | -5,0 | PGmv | 12,6±5,7 | 13,8±5,3 | +8,7 |
| LAEF | 0,81±0,05 | 0,86±0,05** | +5,8 | СДЛА | 35±19 | 40±18 | +12,5 |
*-р<0,05; ** - р<0,001
Таким образом, в динамике через 18 месяцев увеличилась выраженность одышки и застойных явлений в лёгких по данным аускультации, снизилась толерантность к физической нагрузке, оцениваемая по тесту 6-минутной ходьбы, увеличилось количество баллов, набранных по ШОКС. Из эхокардиографических показателей наиболее существенно увеличились площадь ЛП (+11,4%), систолический миокардиальный стресс ЛЖ (+9,3%), выраженность МР (+20%), СДЛА (+12,5%); уменьшилось соотношение EFлж/МСс (-14%), соотношение Е/А трикуспидального потока (-27,5%), что указывает на ухудшение диастолической функции правого желудочка.
Так же как в группе ИБС с помощью многофакторного анализа мы попытались определить прогностические факторы, совокупность которых может влиять на динамику состояния пациента. По методу Байеса была выбрана совокупность 8 параметров, позволяющих предсказывать вероятность ухудшения состояния пациента. По нашим данным к этим параметрам относятся: 1) давность постоянной формы ФП более 10 лет; 2) количество баллов по ШОКС более 9; 3) дистанция по тесту 6-минутной ходьбы менее 150 м; 4) Sлп более 31 см2; 5) LAEF более 0,85; 6) СДЛА более 70 mm Hg; 7) EFпж менее 45%; 8) уровень МНП более 0,5 нг/мл.
Уровень МНП отдельно был оценен у пациентов, состояние которых за последующие 18 месяцев не ухудшилось и у пациентов, состояние которых ухудшилось, либо они скончались от прогрессирования сердечной недостаточности (Диаграмма 8).
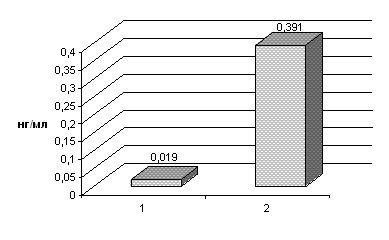
р<0,05
Диаграмма 8. Уровень МНП у пациентов, состояние которых за последующие 18 месяцев не ухудшилось (1) и состояние которых ухудшилось, либо они скончались (2)
Таким образом, у пациентов, состояние которых ухудшилось, либо которые скончались в течение 18 месяцев, уровень МНП при первичном обследовании был существенно выше, чем у пациентов, состояние которых не изменилось за указанный промежуток времени.
В целом можно отметить, что ХСН на фоне ревматических митральных пороков сердца характеризуется более медленным развитием симптоматики, чем при ИБС. Из эхокардиографических параметров наибольшей диагностической значимостью, по нашим данным, обладают такие показатели как систолическое давление в лёгочной артерии, площадь ЛП и соотношение КСР/КДРлп, размеры правых отделов и фракция выброса ПЖ, площадь митрального отверстия, градиент давления на митральном клапане и степень митральной регургитации. Уровень МНП как биохимического маркёра ХСН не всегда адекватно соответствовал тяжести клинических проявлений сердечной недостаточности и нередко находился в пределах нормальных значений даже при выраженной ХСН. Однако отмечена достаточно высокая информативность уровня МНП как фактора прогноза.
На основании эхокардиографических показателей продемонстрировавших наибольшую клиническую значимость в группах ИБС и РБС возможна разработка шкал ремоделирования сердца, аналогично ШОКС В.Ю. Мареева, что требует дальнейших исследований в этой области.
ВЫВОДЫ
1. Для ХСН на фоне ревматических митральных пороков сердца характерно медленное развитие клинической симптоматики, меньшая выраженность симптомов ХСН, таких как: одышка, эпизоды сердечной астмы, отёки нижних конечностей, а также меньшая потребность в госпитализациях по поводу декомпенсации сердечной недостаточности, в отличие от ИБС.
2. Для ХСН на фоне ревматических митральных пороков характерно длительное сохранение нормальной геометрии левого желудочка либо формирование концентрических адаптивных форм ремоделирования левого желудочка, что, возможно, играет роль в более медленном прогрессировании ХСН при этих заболеваниях. В то время как при ХСН на фоне ИБС, начиная с ранних стадий (ФК I-II), характерно развитие эксцентрических дезадаптивных форм ремоделирования ЛЖ, что обусловливает быстрое прогрессирование сердечной недостаточности. Диастолическая дисфункция ЛЖ является одним из ведущих механизмов прогрессирования ХСН.
3. К наиболее ранним эхокардиографическим маркёрам ХСН при ИБС относятся: систолический и диастолический индексы сферичности ЛЖ, систолический миокардиальный стресс ЛЖ, интегральный систолический индекс ремоделирования ЛЖ, соотношение КСРлп/КДРлп (LAEF) и соотношение УО/КСО.
4. МНП не может использоваться в качестве единственного критерия для диагностики начальных форм ХСН на фоне ИБС, так как на ранних этапах развития ХСН его уровень часто не превышает нормальных значений (0,1 нг/мл). Уровень МНП при тяжелой ХСН на фоне ИБС достоверно превышает таковой при начальных стадиях её развития. При РБС нормальные значения МНП не свидетельствуют об отсутствии ХСН и не несут отрицательного прогностического значения. Высокий уровень МНП при РБС отмечается лишь в случаях терминальной ХСН.
5. При оценке взаимосвязи между клиническими симптомами ХСН и рядом ЭхоКГ-параметров, установлено, что при ишемической ХСН степень диастолической дисфункции ЛЖ, площадь ЛП и ИСс в наибольшей степени соответствовали выраженности клинических симптомов. Корреляция фракции выброса ЛЖ с клиническими проявлениями ХСН была менее существенной. Уровень МНП также достоверно коррелировал с тяжестью ХСН при ИБС за исключением её ранних этапов (ФК I). При ХСН на фоне РБС наибольшей степенью корреляции с клиническим статусом характеризовались: СДЛА, LAEF, площадь левого предсердия.
6. Наиболее значимыми факторами прогноза по нашим данным являются: в группе ИБС – интегральные диастолический и систолический индексы ремоделирования, систолический индекс сферичности, тип ДД ЛЖ; в группе РБС – выраженность лёгочной гипертензии, LAEF, площадь ЛП. При оценке пациентов в динамике было отмечено, что в группе ИБС ухудшение клинического состояния в немалой степени было связано с нарастанием диастолической дисфункции ЛЖ и лёгочной гипертензии. В группе РБС ухудшение клинического состояния коррелировало с увеличением площади левого предсердия, ухудшением диастолической функции ПЖ, нарастанием миокардиального стресса ЛЖ, а также с увеличением степени лёгочной гипертензии и митральной регургитации.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
Для оценки выраженности ремоделирования сердца при ХСН ишемического генеза при эхокардиографическом исследовании целесообразно использование таких показателей как систолический и диастолический индексы сферичности ЛЖ, систолический миокардиальный стресс ЛЖ, интегральный систолический индекс ремоделирования ЛЖ, также необходимо обращать более пристальное внимание на показатели диастолической функции ЛЖ, включая время изоволюмического расслабления и время замедления раннего наполнения. У пациентов с митральными пороками сердца ревматической этиологии помимо традиционных показателей (градиенты давления, площадь митрального отверстия, степень митральной регургитации и лёгочной гипертензии) следует указывать площадь левого предсердия и его сократительную функцию (при синусовом ритме), фракцию выброса правого желудочка.
При использовании для диагностики ХСН уровня мозгового натрийуретического пептида необходимо дополнять его определение другими методами диагностики ХСН (ЭхоКГ), так как уровень МНП не всегда достоверно отражает тяжесть ХСН.
Учитывая полученные нами данные о существенной роли нарастания выраженности диастолической дисфункции ЛЖ и степени лёгочной гипертензии при прогрессировании ХСН у больных с ИБС необходимо уделять более пристальное внимание коррекции этих состояний при назначении лечения таким пациентам.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Poscrebisheva А.S., Smurova U.V., Kazakovtseva T.A. Evaluation of neuroimmunoendocrine indicators independence on heart failure severity // Abstracts of 7-th John Humphrey advanced summer school in immunology – Moscow, 2005. – Vol. 45.
2. Поскребышева А.С., Шостак Н.А., Трофимов Е.С., Смурова Ю.В., Казаковцева Т.А. Оценка трехлетней выживаемости больных хронической сердечной недостаточностью с учетом нейроиммунноэндокринных показателей // Тез. II конгресса общества специалистов по сердечной недостаточности «Сердечная недостаточность’ 2007»: Сборник трудов – Москва, 2007. – С.48.
3. Казаковцева Т.А. Шостак Н.А. Зависимость тяжести проявлений ХСН от параметров ремоделирования сердца при ИБС и РБС // Тез. II конгресса общества специалистов по сердечной недостаточности «Сердечная недостаточность’ 2007»: Сборник трудов – Москва, 2007. – С.48.
4. Поскребышева А.С., Смурова Ю.В., Казаковцева Т.А. Изменение уровня провоспалительных и противовоспалительных маркеров у больных хронической сердечной недостаточности различного генеза // Вестник Санкт-Петербургской государственной медицинской академии им И.И. Мечникова – Спб, 2007 - №2(2) – С.164-165.
5. Казаковцева Т.А., Шостак Н.А. Эхокардиографические и лабораторные маркёры хронической сердечной недостаточности: возможно ли их использование при ревматических пороках сердца? // Рациональная фармакотерапия в кардиологии. 2008;5:33-36.
6. Казаковцева Т.А. Шостак Н.А. Диагностическая ценность мозгового и предсердного натрийуретических пептидов при определении выраженности ХСН ишемического и неишемического генеза (стендовый доклад) // Тез. III конгресса общества специалистов по сердечной недостаточности «Сердечная недостаточность’ 2008»: Сборник трудов – Москва, 2008. – С.112.
7. Шостак Н.А., Новиков П.В., Казаковцева Т.А. Уровень концентрации оксида азота в выдыхаемом воздухе у пациентов с системной склеродермией, интерстициальным поражением лёгочной ткани и лёгочной гипертензией // Тез. III конгресса общества специалистов по сердечной недостаточности «Сердечная недостаточность’ 2008»: Сборник трудов – Москва, 2008. – С.85.

