Метастатические опухоли легких (возможности диагностики и место хирургического метода в лечении)
На правах рукописи
Пикин Олег Валентинович
МЕТАСТАТИЧЕСКИЕ ОПУХОЛИ ЛЕГКИХ
(возможности диагностики и место хирургического метода в лечении)
14.00.14 – онкология
14.00.27 – хирургия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Москва – 2006
Работа выполнена в ФГУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена Росздрава»
(директор – академик РАМН, профессор В.И. Чиссов)
Научный консультант:
доктор медицинских наук В.Д. Паршин
Официальные оппоненты:
доктор медицинских наук, профессор А.А.Вишневский
доктор медицинских наук, профессор В.С. Мазурин
доктор медицинских наук, профессор А.С. Мамонтов
Ведущее учреждение:
ФГУ «Российский Научный Центр Рентгенрадиологии Росздрава»
Защита диссертации состоится «18» апреля 2006 года в 14 часов на заседании диссертационного совета Д 208.047.01 при ФГУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена Росздрава»
Адрес: 125284, Москва, 2-ой Боткинский пр., 3.
С диссертацией можно ознакомиться в библиотеке ФГУ «МНИОИ им. П.А. Герцена Росздрава» (125284, Москва, 2-ой Боткинский пр., 3)
Автореферат разослан « » марта 2006 г.
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор С.А. Седых
Общая характеристика работы
Актуальность исследования. При обследовании метастазы в лёгких обнаруживают у 6 – 30% больных со злокачественными опухолями любой локализации [Атанасян Л.А. с соавт., 1977, Айтаков З.Н. с соавт., 1986, Трахтенберг А.Х., Чиссов В.И., 2000, Dresler M., et al., 1996, Greelish J., et al., 2000]. Наиболее часто метастазы в легких выявляют при раке яичка, почки, толстой кишки, остеогенной саркоме и хорионэпителиоме.
Внедрение в клиническую практику компьютерных томографов с высокой разрешающей способностью, позитронно-эмиссионной томографии позволило выявлять изменения в легких, плевре и внутригрудных лимфатических узлах, которые не определялись при стандартном рентгенологическом исследовании [Седых С.А. с соавт., 2002, Seemann MD. et al., 2000, Detterbeck FC. et al., 2004]. При появлении очагов в легких, изменений на плевре и увеличении внутригрудных лимфатических узлов у больных, ранее леченных по поводу различных злокачественных новообразований, возникает проблема их трактовки. Является ли это проявлением прогрессирования заболевания или самостоятельной неопухолевой патологией? В этой ситуации клиницист находится перед дилеммой: проводить лекарственной противоопухолевое лечение или нет? Даже выявление единичных и множественных теней в легких на этапе начальной диагностики или после излеченной первичной опухоли не всегда свидетельствует о метастатическом их поражении. В этой ситуации, порой только оперативное вмешательство с последующим гистологическим исследованием удалённого препарата помогает установить правильный диагноз. С появлением видеоторакоскопии стало возможным решать сложные дифференциально-диагностические задачи по верификации выявленных изменений в легких, плевре и внутригрудных лимфатических узлах с минимальной травмой для больного. Применение малоинвазивных технологий позволяет верифицировать диагноз и выбрать оптимальную лечебную тактику у этой многочисленной категории больных [Сигал Е.Н. с соавт., 2001, Landreneau RJ., et al., 2000, Cardillo G. et al., 2003]
История хирургического лечения метастазов в легких насчитывает более ста лет. Первые попытки удаления метастаза из легкого были предприняты Kronlein и Gross еще в конце XIX века. До сих пор, среди исследователей нет единого мнения в отношении лечебной тактики при метастазах в легких, особенно единичных и множественных. Большинство исследователей проводят химио-гормоно-иммунотерапию в зависимости от гистогенеза злокачественной опухоли, хотя в последние годы появляется все больше сторонников хирургического метода, как компонента комбинированного и комплексного лечения [Pastorino U., et al., 1997, Friedel G., et al., 1999, Pfannschmidt J., et al., 2002, Kanemitsu Y., et al., 2004, Negri F., et al., 2004, Yamamoto K. et al., 2004, Presicci P. et al., 2005]. Несмотря на возрастающий интерес к проблеме использования хирургического метода в лечении больных с метастазами в легких, в большинстве исследований отсутствует научно-обоснованная стратегия лечения этого контингента больных.
В ведущих клиниках расширяют критерии отбора больных для хирургического лечения. Выявление метастазов в печени, головном мозге синхронно или последовательно с поражением легких не считают противопоказанием к оперативному вмешательству [Headrick J. et al., 2001, Yamada H. et al., 2002, Reddy R. et al., 2004,]. Полученные первые результаты подобных оперативных вмешательств внушают оптимизм, что диктует необходимость накопления клинического опыта. Несмотря на расширение показаний к операциям при внутрилегочных метастазах, по отношению ко всем больным с метастазами в легких операцию удается выполнить не более чем у 5 – 10% из них. В структуре оперативных вмешательств торакальных клиник частота операций по поводу внутрилегочных метастазов не превышает 2,5 – 4%, несмотря на огромный контингент больных, нуждающихся в специализированной помощи. Это объясняется все еще настороженным отношением большинства торакальных хирургов к проблеме лечения внутрилегочных метастазов.
Актуальной является проблема повторных операций при «рецидиве» метастаза в лёгких, который возникает в среднем у 25 – 35% больных [Weiser MR. et al., 2000, Jaklitsch M. et al., 2001, Ogata Y. et al., 2005]. До сих пор повторные операции по поводу «рецидивных» метастазов являются редкостью даже в специализированных клиниках.
При планировании хирургического лечения больных с внутрилегочными метастазами чрезвычайно важно провести комплексную оценку наиболее значимых прогностических факторов, что в конечном итоге определит судьбу оперированного больного.
Таким образом, проблема лечения больных с метастазами в легких несомненно актуальна. Анализ отечественной и зарубежной литературы показал, что остаются нерешенными вопросы:
- лечебной тактики при одновременном выявлении первичной опухоли и метастаза/метастазов в легких;
- обоснованности видеоторакоскопических операций при метастазах в легких, особенно их двусторонней локализации;
- выбора оптимальной лечебной тактики при единичных и множественных метастазах и места хирургического метода в лечении этой сложной категории больных;
- целесообразности сочетанных операций при локализации метастазов в нескольких органах;
- лечебной тактики при «рецидивных» метастазах.
Наиболее сложным является выбор лечебной тактики при единичных и множественных метастазах. Последовательность использования тех или иных методов воздействия зависит от гистогенеза первичной опухоли и чувствительности метастазов к консервативному противоопухолевому лечению. Только взвешенный подход с учетом всех прогностических факторов позволит определить стратегию лечения этого многочисленного контингента больных. Все это обуславливает целесообразность проведения данного научного исследования.
Цель и задачи исследования
Целью исследования является оптимизация диагностики и улучшение результатов лечения больных с метастазами в легких опухолей различных локализаций на основе дифференцированного подхода к использованию хирургического метода.
Для реализации поставленной цели были поставлены следующие основные задачи:
- Определить в сравнительном аспекте возможности рутинного рентгенологического, КТ исследования и видеоторакоскопии в диагностике метастазов в легких.
- На основе анализа послеоперационных осложнений и летальности разработать оптимальную хирургическую тактику при повторных и одномоментных вмешательствах.
- Определить место хирургического метода как компонента комплексного лечения метастазов в легких.
- Определить место видеоторакоскопии в хирургии внутрилегочных метастазов.
- Разработать методику видеоассистированного удаления двусторонних метастазов.
- Обосновать лечебную тактику при одновременном выявлении первичной опухоли и метастазов в легких.
- Обосновать целесообразность повторных операций при так называемых «рецидивных» метастазах.
- Разработать стратегию лечения больных с метастазами в легких на основе моно- и многофакторного анализа отдаленных результатов.
Научная новизна исследования
Впервые определено место хирургического метода, как компонента комплексного лечения больных с метастазами в легких опухолей различных локализаций и разработана научно-обоснованная стратегия их лечения на основании всестороннего анализа репрезентативной группы больных из двух ведущих научно-исследовательских учреждений страны.
Уточнены дифференциально-диагностические критерии первичной и метастатической опухоли легкого на основании комплексной методики оценки изображения получаемого при компьютерной томографии.
Обоснована целесообразность использования видеоторакоскопического метода удаления солитарного внутрилегочного метастаза на основе сравнительного анализа результативности рутинного рентгенологического, КТ методов исследования с данными операционных находок и их сопоставления с результатами планового гистологического исследования.
Доказана высокая информативность видеоторакоскопии в дифференциальной диагностике изменений легочной ткани, плевры и внутригрудных лимфатических узлов у больных, леченных ранее по поводу злокачественных новообразований.
Разработана и применена (впервые в России) методика видеоассистированного удаления двусторонних метастазов.
На репрезентативном клиническом материале обоснован дифференцированный подход к использованию хирургического метода у больных с единичными и множественными метастазами в зависимости от их чувствительности к лекарственному противоопухолевому лечению с учетом основных факторов прогноза.
Обоснована целесообразность оперативных вмешательств при одновременном выявлении первичной опухоли и метастазов в легких, а также локализации метастазов колоректального рака в печени и легком.
Доказана эффективность повторных операций при возникновении «рецидивных» метастазов в легких.
На основе моно- и многофакторного анализа выделены независимые факторы благоприятного и неблагоприятного прогноза.
Практическая значимость
Разработанная стратегия лечения больных с метастазами в легких опухолей различных локализаций на основе дифференцированного подхода к использованию хирургического метода позволила улучшить результаты лечения этой сложной категории больных.
Показано, что двусторонние и повторные операции при метастазах в легких не сопровождаются достоверным увеличением частоты послеоперационных осложнений и летальности по сравнению с группой больных оперированных однократно.
Разработана и применена методика видеоассистированного удаления билатеральных метастазов, которая может быть альтернативой стернотомии и билатеральной торакотомии.
Показано, что отдаленные результаты повторных операций по поводу «рецидивных» метастазов в легких не уступают таковым при солитарном метастазе.
Одновременное выявление первичной опухоли и метастаза в легком не является противопоказанием к хирургическому лечению обеих локализаций. Отдаленные результаты оперативных вмешательств у этого контингента больных удовлетворительные.
У больных с метастазами колоректального рака в легком и печени оправданы одномоментные или последовательные операции по удалению выявленных метастазов.
На основе моно- и многофакторного анализа установлено, что состояние внутригрудных лимфатических узлов и характер выполненной операции являются независимыми прогностическими факторами, определяющими исход лечения у больных с метастазами в легких.
Апробация работы
Апробация диссертации состоялась 15 декабря 2005 года на совместной конференции диагностических и клинических отделений ФГУ «МНИОИ им. П.А. Герцена Росздрава». Основные положения и материалы диссертации доложены и представлены на:
- XII Национальном конгрессе по болезням органов дыхания, Москва, 2002г.
- IV Всероссийской конференции молодых ученых, Москва, 2003г.
- XII Европейском онкологическом конгрессе, Будапешт, 2004г.
- V Международном медицинском форуме, Нижний Новгород, 2004г.
- 519 заседании Московского онкологического общества, 2005г.
- VI Всероссийском съезде онкологов, Ростов-на-Дону, 2005г.
Публикации
По теме диссертации опубликовано 26 печатных работ.
Объем и структура диссертации
Диссертация состоит из введения, обзора литературы, семи глав собственных исследований, заключения, выводов, практических рекомендаций и списка литературы, включающего 263 публикации отечественных и зарубежных авторов. Диссертация изложена на 225 страницах машинописного текста, содержит 47 таблиц и 68 рисунков.
Материалы и методы исследования
В исследование включено 412 больных в возрасте от 18 до 79 лет (медиана 56,4 года), оперированных в торакальном отделении МНИОИ им. П.А. Герцена и в отделении хирургии легких и средостения РНЦХ РАМН по поводу метастазов в легких опухолей различных локализаций с января 1970 по декабрь 2004 года. Распределение больных в зависимости от локализации и гистогенеза первичной опухоли представлено в таблице 1.
Таблица 1.
Гистологическая структура и локализация первичной опухоли у больных оперированных по поводу метастазов в легких
| Гистогенез, локализация | Число больных | |
| Абс. | % | |
| Саркома остеогенная хондросаркома остеобластокластома мягкотканная Рак почки толстой кишки молочной железы шейки матки тела матки дна полости рта гортани слюнной железы яичка печени пищевода желудка щитовидной железы базальноклеточный Гранулезоклеточная опухоль яичников Меланома | 117 16 5 8 88 266 75 72 58 18 11 7 6 6 5 3 1 1 1 2 2 27 | 29,6 3,9 1,0 1,6 23,1 63,4 18,2 17,5 14,1 4,4 2,8 1,4 1,2 1,2 1,0 0,6 0,2 0,2 0,2 0,4 0,4 6,6 |
| Всего | 412 | 100,0 |
Интервал от момента окончания лечения первичной опухоли до выявления метастазов варьировал от 0 до 240 месяцев (медиана – 29,3+1,9 мес.). Это так называемый DFI (disease free interval, т.е. интервал свободный от болезни или безметастатический период).
Следует отметить, что метастазы в легких выявлены одновременно с первичной опухолью (DFI=0) у 46 (11,2%), из них рак почки диагностирован у 17 (37,4%), саркома – у 13 (28,2%), рак толстой кишки – у 11 (23,9%), молочной железы – у 2 (4,2%), меланома – у 2 (4,2%) и рак яичка – у 1 (2,1%) больного.
Мы придерживаемся общепринятой классификации, согласно которой метастазы в легких подразделяют по количеству на солитарный (1 узел), единичные (2 – 3 узла) и множественные (>3 узлов), а по локализации на одно- и двусторонние.
Солитарный метастаз диагностирован у 245 (59,4%), единичные – у 80 (19,4%), множественные – у 87 (21,2%) больных. Преимущественно отмечена односторонняя локализация метастазов – у 363 (88,1%), а двустороннее поражение диагностировано у 49 (11,9%) больных.
При отборе больных для хирургического лечения по поводу метастазов в легких придерживались разработанных в клинике критериев:
- отсутствие рецидива первичной опухоли;
- поражение только легких, за исключением колоректалього рака;
- возможность удаления всех выявленных метастазов;
- удовлетворительные функциональные резервы сердечно-сосудистой и дыхательной систем;
- неэффективность лекарственного противоопухолевого лечения.
Одновременное выявление первичной опухоли и метастаза в легком не считали противопоказанием к оперативному вмешательству.
Отношение к проблеме использования хирургического метода в лечении больных с внутрилегочными метастазами менялось с течением времени. Если в первый период работы (1970 – 1984гг.) преимущественно оперировали больных с солитарным метастазом, то в течение последних десяти лет (1995 – 2004гг.) две трети оперативных вмешательств выполнили по поводу единичных и множественных метастазов, что отражает эволюцию наших взглядов на проблему лечения этой сложной категории больных (рис. 1).

Рис.1. Соотношение оперированных больных по поводу солитарного и единичных/множественных метастазов в зависимости от периода деятельности
Принципиальным моментом считаем дифференцированный подход к выбору лечебной тактики у больных с метастазами в легких. В зависимости от чувствительности метастазов к химио-гормоно-иммунотерапии выделили 2 группы:
I группа – метастазы, чувствительные к лекарственному противоопухолевому лечению (злокачественные опухоли яичка, остеогенная саркома, хорионэпителиома, рак молочной железы, высокодифференцированный рак эндометрия и др.).
II группа – метастазы, резистентные или обладающие низкой чувствительностью к указанному методу терапии (рак толстой кишки, шейки матки, меланома, саркома мягких тканей, хондросаркома).
При морфологически подтвержденных легочных метастазах I группы на первом этапе предпочтение отдавали лекарственному противоопухолевому лечению и только при его неэффективности решали вопрос об оперативном вмешательстве. У больных с метастазами II группы в первую очередь рассматривали возможность их удаления.
До операции на легком лекарственное противоопухолевое лечение по поводу метастазов проведено 60 (14,6%), из них химиогормонотерпия – 23 (38,3%), полихимиотерапия – 23 (38,3%), гормонотерапия – 9 (15,0%) и иммунотерапия – 5 (8,4%) больным. Больным проводили 4 – 6 курсов полихимиотерапии, эффективность лечения оценивали после каждых 2 курсов.
Вопрос о целесообразности хирургического вмешательства по поводу метастазов в легких решали коллегиально после комплексного обследования и оценки функционального состояния больного. При хирургическом лечении метастазов в легких предпочтение отдавали щадящим оперативным вмешательствам: атипичная резекция легкого, классическая сегментэктомия и прецизионное удаление метастаза выполнена у 271 (65,8%), лобэктомия – у 118 (28,6%), а пневмонэктомия – лишь у 23 (5,6%) больных. Таким образом, у 2/3 больных выполнена сублобарная резекция (табл. 2).
Таблица 2
Распределение больных в зависимости от объема выполненной операции
| Операция | Число больных | |
| Абс. | % | |
| Сублобарная резекция атипичная прецизионная сегментэктомия Лобэктомия Пневмонэктомия | 271 225 36 10 118 23 | 65,8 54,7 8,7 2,4 28,6 5,6 |
| Всего | 412 | 100,0 |
По поводу метастазов и в других органах оперированы 7 больных: у 3 предшествовало удаление солитарного метастаза в головном мозге, резекция печени – у 3, а одному больному выполнили синхронно вмешательства на легком и печени. Объем оперативного вмешательства на печени: гемигепатэктомия – 2, атипичная резекция – 2. Симультанные оперативные вмешательства на первичном очаге и легком выполнены 4 (4,6%) больным (при раке почки – у 2, толстой кишки – у 2).
Одновременное поражение паренхимы легкого и внутригрудных лимфатических узлов отмечено у 70 (16,9%) больных.
Оперативный доступ выбирали в зависимости от количества метастазов и их локализации в паренхиме легких. Предпочтение отдавали торакотомному доступу – 387 (94,4%). Видеоторакоскопическое удаление метастазов выполнили 20 (4,9%), стернотомию – 3 (0,7%) больным. При двусторонней локализации метастазов чаще оперировали последовательно (24 больных) с интервалом в 3 – 4 недели, реже – одномоментно (11 больных). Вопрос о возможности билатеральной резекции легких решали после всестороннего функционального обследования больного. Всего выполнено 487 оперативных вмешательств, из них двусторонних резекций легких – 35, повторных операций по поводу новых метастазов – 40 у 29 больных. Удалить все выявленные очаги удалось у 358 (86,9%) больных. Подобные операции условно рассматривали как «радикальные». При невозможности удаления всех выявленных метастазов или при отказе от запланированного второго этапа хирургического лечения при двустороннем поражении оперативные вмешательства считали «паллиативными», которые выполнены 58 (13,1%) больным.
После операции 127 (30,8%) больным проведено лекарственное противоопухолевое лечение (из них полихимиотерапия – 86 (67,6%), химио-гормонотерапия – 14 (11,1%), иммунотерапия – 14 (11,1%), гормонотерапия – 13 (10,2%)) в зависимости от гистогенеза первичной опухоли и чувствительности к нему метастазов.
При опухолях чувствительных к гормонотерапии (рак молочной железы, тела матки) определяли уровень рецепторов эстрогена, прогестерона в метастазе иммуногистохимическим методом. Состояние рецепторов в метастазе рака молочной железы изучено у 10 (17,2%), из них положительные рецепторы к эстрогенам выявлены у половины больных, что позволило обосновать назначение гормонотерапии. Статус рецепторов в ткани метастаза изучен у 5 больных раком тела матки, из них у 3 – иммуногистохимическая реакция к рецепторам эстрогена и прогестерона в клетках опухоли оказалась отрицательной. Неэффективность ранее проведенной гормонотерапии и данные иммуногистохимического исследования позволили воздержаться от проведения гормонотерапии в послеоперационном периоде.
Помимо общеклинических методов обследования применяли стандартную рентгенографию в 2-х проекциях, томографию, полипозиционную рентгеноскопию, компьтерную (КТ) или спиральную компьютерную томографию (СКТ) органов грудной клетки, бронхоскопию (бронхоскоп “Olympus”, Япония), ультразвуковое исследование органов брюшной полости (аппарат ультразвуковой диагностики “Siemens Antares”с набором датчиков), малого таза, периферических непальпируемых лимфатических узлов, а при необходимости КТ органов брюшной полости, головного мозга, сцинтиграфию костей скелета, эзофаго-, гастро- или колоноскопию. Комплекс диагностических методов был направлен на возможное выявление рецидива первичной опухоли, уточнение локализации метастазов и их количества в паренхиме легких. С целью морфологической верификации периферического образования в легких выполняли трансторакальную пункцию под контролем рентгеноскопии, компьютерной томографии и УЗИ. При бронхоскопии выполняли прямую, щеточную биопсию, а также брали аспират из дистальных отделов соответствующего сегментарного или субсегментарного бронха. До операции диагноз метастатического поражения легких был верифицирован у 184 (44,7%). Трансторакальная пункция оказалась результативной у 102 (77,3%) из 132 больных, а у 82 (результативность – 19,9%) – диагноз был подтвержден после морфологического исследования материала, полученного при бронхоскопии. КТ или СКТ органов грудной клетки выполнили 127 (30,8%) больным.
При оценке изображения использовали следующие методики КТ исследования: стандартную, тонких срезов, внутривенного «струйного» усиления, «капельного» усиления, «болюсного» усиления, денситометрической обработки изображений (графики гистограмм плотности, программа высвечивания дисперсии плотности Highlighting). КТ-число определяли в единицах «рентгеновской плотности», т.е. единицах Хаунсфилда, гда каждому тканевому элементу соответствуют конкретные показатели коэффициента плотности. Комплексную методику оценки изображения с целью дифференциальной диагностики применили у 56 больных солитарным метастазом. Полученное изображение узлового образования оценивали в трех режимах: легочном, мягкотканном и жестком окне.
В зависимости от локализации и гистогенеза первичной опухоли больным исследовали уровень маркеров сыворотки крови до операции (РЭА у 25 больных колоректальным раком; СА 19-9, СА 72-4 у 10 больных той же локализации; SCC – у 8 плоскоклеточным раком шейки матки; ХГЧ (хорионический гонадотропин), АФП (альфафетопротеин), ЛДГ (лактатдегидрогенеза) – у 5 раком яичка; TuМ2-РК – у 10 раком почки; ингибин в – у 2 гранулезоклеточной опухолью яичников) и далее каждые три месяца при динамическом наблюдении. Повышение уровня маркера от исходного являлось основанием для углубленного обследования с целью выявления рецидива или новых метастазов.
Статистическая обработка результатов
Для сравнения эффективности различных методик КТ в диагностике солитарного метастаза использовали принцип решающей матрицы, оценивая показатели информативности – прогностические тесты (ложноотрицательная фракция, истинноположительная фракция, истинноотрицательная фракция, ложноположительная фракция), а также – информативность данных признаков (чувствительность, специфичность, диагностическая точность теста, предсказуемость положительного теста, предсказуемость отрицательного теста).
Статистические показатели диагностических свойств параметров рассчитывали по формулам:
Чувствительность = (ИП/ИП+ЛО)х100%
Специфичность = (ИО/ИО+ЛП)х100%
Диагностическая точность метода = (ИП+ИО/ИП+ИО+ЛП+ЛО)х100%
Предсказуемое значение положительного теста = (ИП/ИП+ЛП)х100%
Предсказуемое значение отрицательного теста = (ИО/ИО+ЛО)х100%
ИП – истинно-положительные результаты, ИО – истинно-отрицательные результаты, ЛП – ложноположительные результаты, ЛО – ложноотрицательные результаты.
Различия данных оценивали по стандартной ошибке средней величины с использованием коэффициента Стьюдента (t). Статистически значимыми с достоверностью 95% считали различия при величине t>=2 и р<0,05. Выживаемость больных рассчитывали по методу Cutler-Ederer (1958). Ошибку репрезентативности интервальных показателей выживаемости (mi) определяли по формуле Greenwood. Достоверность различий показателей выживаемости оценивали при помощи непараметрического критерия (log-rank test). Моно- и многофакторный регрессионный анализ (регрессионная модель Кокса пропорционального риска) проводили с использованием пакета прикладных программ для персонального компьютера Statistica 6.0.
Результаты собственных исследований и их обсуждение
Диагностика метастазов в легких
Всем больным проведено стандартное рентгенологическое исследование органов грудной клетки, у 127 – компьютерная томография, при которой у каждого пятого (21,3%) были выявлены рентгенонегативные метастазы. При рентгенологическом исследовании солитарный метастаз определялся у 89, единичные – у 27, множественные – у 8, а у 3 больных патологии при стандартном исследовании не выявлено. Компьютерная томография позволила выявить дополнительные очаги у 27 (21,3%) больных. Совпадение рентгенологического и компьютернотомографического заключения отметили у 100 (78,7%) больных. Во время оперативного вмешательства у 14 (11,0%) больных выявили образования в легких, не определявшиеся при компьютерной томографии. Таким образом, только тщательной пальпация паренхимы легкого позволяет установить истинное количество метастазов в паренхиме легкого. Сравнительная результативность рентгенологического метода, компьютерной томографии и интраоперационной ревизии в диагностике метастазов в легких представлена в таблице 3.
Таблица 3
Сравнительная результативность рентгенологического метода, КТ и интраоперационной ревизии при метастазах в легких в зависимости от их количества
| Характер метастазирования | Метод исследования | ||
| рентгенологический | КТ | Операция | |
| Солитарный Единичные Множественные Метастазы не выявлены | 89 27 8 3 | 73 (82%)* 41 (152%) 13 (162%) + | 69 (77%) 38 (141%) 20 (250%) + |
* в скобках указана относительная результативность по сравнению с рентгенологическим методом
При стандартном рентгенологическом исследовании выявлено 178 узлов в легких, компьютерной томографии – 221, а во время оперативных вмешательств удалено – 248. Следовательно, компьютерная томография позволила диагностировать на 24,2% больше очагов, чем рентгенологическое исследование. При тщательной ревизии паренхимы легких выявлено на 39,2% образований больше, чем при рентгенологическом исследовании и на 12,2% - чем при компьютерной томографии. При плановом гистологическом исследовании удаленных препаратов установлено, что у 5 (3,9%) больных дополнительные образования, трактовавшиеся как метастазы по данным КТ, оказались доброкачественными.
Мы отдельно провели анализ частоты выявления дополнительных образований при интраоперационной ревизии по сравнению с компьютерной томографией, когда изменения в легком трактовались как солитарный метастаз. Из 73 больных с солитарной тенью в легком по данным КТ истинно солитарный характер тени подтвержден у 67 (91,8%). Дополнительные образования выявлены у 6 (8,2%) больных, из них у 2 – природа дополнительной тени в легком оказалась доброкачественной. Таким образом, риск пропустить дополнительный метастаз снизился до 5,4%. Проведенный сравнительный анализ результативности рентгенологического, компьютернотомографического методов исследования, интраоперационной ревизии с плановым гистологическим исследованием позволил нам обосновать целесообразность более широкого использования видеоторакоскопической резекции легкого при солитарном метастазе в клинической практике.
Характерными особенностями метастаза при КТ исследовании являются преимущественно округлая, реже овальная форма образования, четкость и ровность его очертания, однородность структуры, отсутствие лимфогенной дорожки к корню и признаков увеличения внутригрудных лимфатическх узлов, плотность в пределах 20 – 60 ед.Н, локальная компактная дисперсия солидных участков (30 – 50 ед.Н) по периферии, многофазность гистограммы плотности с асимметрией графика вправо или влево от экстремума и гиперваскуляризация узла после внутривенного усиления с хаотичным распределением контраста. При стандартной методике истинноположительные результаты констатированы в 52, при комплексной – в 54 наблюдениях, ложноотрицательные в 4 и 2 наблюдениях соответственно. Использование количественных и качественных характеристик при анализе КТ изображения позволило повысить чувствительность метода в диагностике солитарного метастаза с 92,8% до 96,4%, специфичность с 96,0% до 98,8%, диагностическую точность с 95,3% до 98,3% соответственно.
Диагностическая видеоторакоскопия выполнена 34 больным ранее леченных по поводу злокачественных опухолей различных локализаций. У всех из них при рентгенологическом исследовании, включая компьютерную томографию органов грудной клетки, определялись изменения в легочной ткани, плевре и/или внутригрудных лимфатических узлах, которые трактовали как метастатическое поражение. Изолированное поражение легкого констатировано у 24 (70,6%), плевры – у 4 (11,8%), внутригрудных лимфатических узлов – у 2 (5,8%). Сочетание изменений легочной паренхимы и лимфатических узлов диагностировали у 2 (5,8%), легкого и плевры – у 2 (5,8%) больных. Стабильная рентгенологическая картина выявленных изменений на фоне проводимого лечения заставила усомниться в правильности предполагаемого диагноза. Метастатический характер изменений диагностирован у 22 (65,0%), неопухолевая патология – у 12 (35,0%) больных.
Таким образом, видеоторакоскопия является информативным методом завершающей диагностики патологии легкого, плевры и средостения, выявленной при динамическом наблюдении онкологических больных. Только гистологическое исследование позволяет установить истинную природу выявленных изменений и выбрать оптимальную лечебную тактику у этой многочисленной категории больных.
Непосредственные результаты оперативных вмешательств (послеоперационные осложнения и летальность)
Послеоперационные осложнения констатированы у 43 (10,4%) больных. Основными «хирургическими» осложнениями были гнойно-воспалительные (нагноение раны (2,5%), бронхо-плевральный свищ (2,1%), эмпиема плевры (0,7%) и внутриплевральное кровотечение (0,4%)). Они констатированы у 23 (5,8%) больных. Другие осложнения (негерметичность швов легочной ткани, гиповентиляция оставшейся доли, остаточная полость, желудочное кровотечение) развились у 6 (1,5%) больных.
Среди «нехирургических» осложнений наиболее частыми были пневмония – у 1,7%, сердечная недостаточность – у 0,96%, нарушение сердечного ритма – у 0,48% и тромбоэмболия легочной артерии – у 0,48%.
Практически у каждого третьего больного перенесшего пневмонэктомию констатировано осложненное течение послеоперационного периода (30,4%), что в 2,5 раза превышает таковые показатели при лобэктомии (12,7%) и в 4 раза – сублобарной резекции (7,7%) (p<0,05) (табл.4). После видеоторакоскопических резекций легкого осложнений не было.
Таблица 4
Количество послеоперационных осложнений и летальность в зависимости от объема оперативного вмешательства
| Операция | Число больных | Количество осложнений | Летальность | ||
| Абс. | % | Абс. | % | ||
| Сублобарная резекция Лобэктомия Пневмонэктомия | 271 118 23 | 21 15 7 | 7,7+1,6 12,7+3,1 30,4+9,6 | 1 1 3 | 0,4+0,3 0,9+0,8 13,0+7,0 |
После одномоментных операций послеоперационные осложнения диагностированы у 3 из 11 больных (27,3%) и у одного из 24 (4,2%) после двухэтапных вмешательств. Летальных исходов не было. Наблюдаемая тенденция к увеличению частоты осложнений после билатеральных резекций легких статистически не значима (р>0,05), что делает их оправданными у селективного контингента больных с удовлетворительными функциональными резервами. Осложнения повторных оперативных вмешательств констатированы у 6 (20,7%) больных, что также достоверно не отличается группы больных, оперированных однократно (р>0,05).
Послеоперационная летальность, как один из основных показателей непосредственных результатов хирургического лечения, составила 1,2% (5 из 412 больных). Следует отметить, что за последние десять лет летальных исходов у больных, оперированных по поводу метастазов в легких, не было. Летальность после пневмонэктомии (13,0%) оказалась достоверно выше по сравнению с органосохранными оперативными вмешательствами (0,7%) (p<0,05) (табл.4). Принимая во внимание высокую частоту осложнений и летальность, пневмонэктомию у больных с метастазами в легких следует признать рискованным оперативным вмешательством. Учитывая особенности клинического течения метастазов в легких (высокая вероятность появления метастазов в контралатеральном легком), показания к расширению объема оперативного вмешательства должны быть обоснованы. После повторных операций летальность составила 6,7% (2 из 29 больных), что достоверно не отличается от такового показателя после односторонних вмешательств.
Отдаленные результаты лечения больных с метастазами в легких с использованием хирургического метода
Пятилетняя выживаемость больных после удаления солитарного метастаза составила в целом 34,9%+3,1, единичных – 21,7%+4,8 и множественных – 14,7%+4,5. После удаления солитарного метастаза рака эндометрия 5 и 10-летняя выживаемость составила 50,0%+8,1, почки – 40,2%+3,2 и 23,7%+3,1, толстой кишки – 33,4%+6,4 и 28,2%+5,8, молочной железы – 31,6%+4,3 и 15,8%+5,2, сарком мягких тканей – 32,5%+4,2 и 9,8%+5,0 больных соответственно. При метастазе остеогенной саркомы 5 лет пережили 36,0%+10,4, рака органов головы и шеи – 31,2%+7,2 и шейки матки – 25,0%+7,8 больных. Ни один больной после удаления метастазов меланомы не пережил пять лет. Четверо больных оперированных по поводу метастазов колоректального рака в печень и легком живы 12, 16, 24 и 36 мес. после операции без признаков прогрессирования опухолевого процесса. Эффективность хирургического метода подтверждают показатели длительной безрецидивной выживаемости (рис. 2).
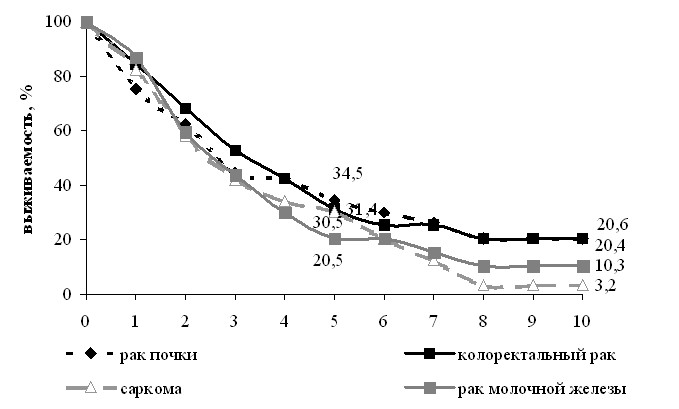
Рис.2. Безрецидивная выживаемость после удаления солитарного внутрилегочного метастаза в зависимости от гистогенеза и локализации первичной опухоли
Хирургическая тактика в комбинации с лекарственными методами лечения с учетом чувствительности к ним позволила добиться 5-летней выживаемости при единичных метастазах рака почки (37,5%+10,8), эндометрия (20,0%+10,2), толстой кишки (17,0%+9,2), молочной железы (16,7%+9,1) и сарком мягких тканей (29,3%+6,2), из них без прогрессирования заболевания этот срок пережили 31,2%, 11,2%, 17,6% и 16,7% больных соответственно (рис.3).

Рис.3. Безрецидивная выживаемость больных после удаления единичных метастазов в зависимости от гистогенеза и локализации первичной опухоли
Даже после удаления множественных метастазов рака почки, толстой кишки и сарком мягких тканей 5 лет пережили 15,0%+6,1, 13,0%+9,4 и 7,7%+4,6 больных, из них без прогрессирования заболевания 12,9%, 0% и 3,8% больных соответственно. Полученные нами результаты подтверждают целесообразность комплексного подхода в лечении этой сложной категории больных (рис.4).
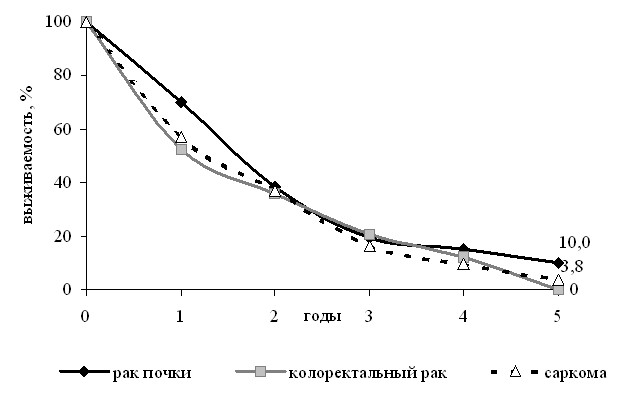
Рис.4. Безрецидивная выживаемость больных после удаления единичных метастазов в зависимости от гистогенеза и локализации первичной опухоли
Для сравнительной оценки эффективности хирургического метода нами проведен анализ результатов лекарственного противоопухолевого лечения у 100 больных с верифицированными метастазами в легких сарком, рака почки, молочной железы и толстой кишки. Группы больных были сопоставимы по полу, возрасту, количеству метастазов, величине DFI и характеру лекарственного лечения. Отдаленные результаты лечения больных (n=15) с метастазами колоректального рака получавших химиотерапию оказались малоутешительны. При солитарном метастазе 1 год пережили 87,5%+7,4 (7 из 8), 2 года – 50,0%+8,2 (4 из 8), 3 года – 25,0%+9,1 (2 из 8), а единичных – 71,4%+8,5 (5 из 7), 28,6%+10,3 (2 из 7), 14,3%+10,1 (1 из 7) больных соответственно. Четырехлетней выживаемости не отмечено. В группе больных (n=25), которым проводили только иммунотерапию по поводу метастазов рака почки 1, 3-х и 4-летняя выживаемость составила 68,0%+10,3 (15 из 25), 28,0%+7,4 (7 из 25) и 8,0%+6,2 (2 из 25), что достоверно хуже результатов хирургического лечения (р<0,05, log-rank). Результаты химиогормонотерапии метастазов рака молочной железы также уступают таковым с использованием хирургического метода: 1, 3 и 5-летняя выживаемость составила 70,4%+4,6, 18,5%+5,1 и 7,4%+3,6 соответственно (р<0,05, log-rank). Результаты лекарственного противоопухолевого лечения больных с метастазами сарком напрямую зависели от гистогенеза опухоли. Закономерно, что эффективность химиотерапии больных с метастазами остеогенной саркомы превосходила таковую мягкотканной, но значительно уступала по этому показателю хирургическому методу. В группе больных (n=13) с метастазами остеогенной саркомы в легких, получавших полихимиотерапию 1, 3-х и 5-летняя выживаемость составила 53,9%+13,8, 15,4%+8,4 и 7,6%+4,2 а при единичных – ни один не пережил трех лет. Различия выживаемости между группами хирургического и консервативного лечения статически достоверны (p<0,05, log-rank). Неудовлетворительные результаты лекарственного лечения больных (n=18) с метастазами сарком мягких тканей. 1 и 2-летняя выживаемость в этой группе составила 64,7%+11,6 и 5,9%+4,3, из них ни один не пережил 3 лет. Различия показателей выживаемости достоверны (p<0,05, log-rank). Таким образом, на значительное увеличение продолжительности жизни можно рассчитывать только при метастазах опухолей чувствительных к химио-гормоно-иммунотерапии (остеогенная саркома, рак молочной железы, почки) (рис.5).
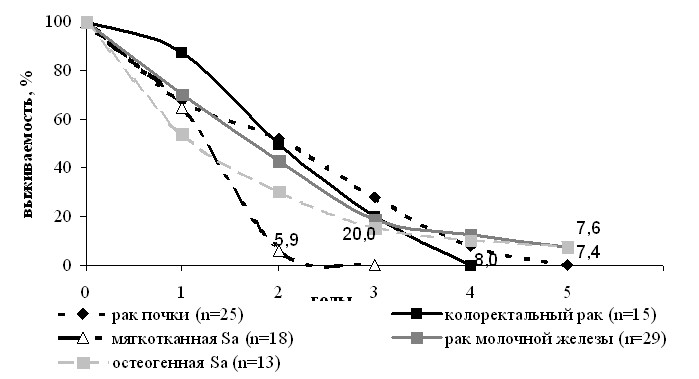
Рис.5. Выживаемость больных после консервативного противоопухолевого лечения метастазов в легких в зависимости от локализации и гистогенеза первичной опухоли
В онкологической клинике к настоящему времени сформулированы основные показания к видеоторакоскопии, однако ее целесообразность при легочных метастазах остается спорной. Видеоторакоскопическую резекцию легкого при метастазах выполнили 20 больным, из них видеоассистированную с мини-доступом – 4 больным. Интраоперационное торакоскопическое ультразвуковое исследование выполнили 15 больным с целью уточнения локализации метастаза в паренхиме легкого. Метастаз удалось визуализировать у 12 (80,0%) больных, из них у 4 (33,3%) образование в легком не пальпировалось инструментом. Использование торакоскопического УЗИ легкого в этой ситуации позволило избежать конверсии на торакотомию. Торакоскопическое УЗИ было неинформативным у 3 (20,0%) больных в связи с неполным коллапсом легкого.
У 2 больных при двусторонней субплевральной локализации метастазов использовали методику видеоассистированного их удаления из доступа под мечевидным отростком (рис.6).
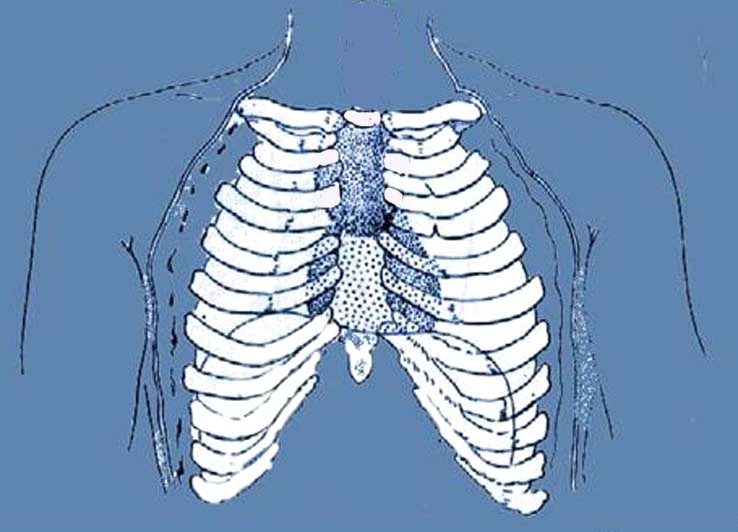
------- Линия кожного разреза ---------- Места введения торакопортов
Рис.6. Схема оперативного доступа для видеоассистированного удаления двусторонних метастазов
Преимуществами указанного доступа является возможность адекватной ревизии обоих легких, одноэтапное удаление билатеральных метастазов и меньшая травматичность по сравнению со стернотомией и тем более – билатеральной торакотомией.
После видеоторакоскопической резекции легкого 6 (30,0%) больных наблюдаются более 3-х лет, 5 – умерли от отдаленных метастазов (25,0%) через 12, 16, 18, 22 и 25 мес. после операции, 9 – живы в сроки до 3-х лет, из них без признаков прогрессирования болезни – 5. У одного (5,0%) больного диагностирован «рецидив» в области скрепочного шва в сочетании с метастазами в других органах. Наши данные и анализ зарубежных публикаций подтверждают, что результаты видеоторакосокпической резекции легкого не уступают таковым открытой хирургии при солитарном метастазе.
После «радикальных» двусторонних резекций легких по поводу синхронных билатеральных метастазов 5-летний срок пережили 13,5% больных (медиана выживаемости – 26,2 мес.). Все больные, которым выполнены паллиативные вмешательства, погибли в течение двух лет (медиана выживаемости – 6,5 мес.). Таким образом, «радикальность» выполненной операции является значимым прогностическим фактором (р<0,01, log-rank).
Примерно у 25 – 35% больных после хирургического лечения могут возникать новые метастазы в легких, которые в литературе принято называть «рецидивными». При изолированном их поражении у селективного контингента больных возможно выполнить повторное оперативное вмешательство. Нами повторные операции выполнены у 29 больных, причем за последние 10 лет выполнили более половины подобных операций. Общая 1, 3-х и 5-летняя выживаемость после первой операции составила 92,7%+4,9, 71,1%+5,0 и 47,5%+7,5, а после повторной – 74,5%+8,3, 45,3%+4,7 и 25,7%+5,9 соответственно. Различия показателей выживаемости статистически достоверны (р<0,05, log-rank).
При планировании лечения больных с метастазами в легких чрезвычайно важно выделить группу наиболее значимых прогностических факторов, которые и будут определять судьбу оперированного больного (табл 5).
Таблица 5
Результаты хирургического лечения больных с внутрилегочными метастазами в зависимости от различных прогностических факторов (монофакторный анализ)
| Прогностический фактор | Число больных | Жили более 5 лет, % | р |
| Пол м ж Гистогенез метастаза рак саркома меланома DFI >=36 мес. <36 мес. DFI (солит. метастаз) >=36 мес. <36 мес. Количество метастазов 1 2 – 3 >3 Локализация метастазов** Односторонняя Двусторонняя Тип операции Сублобарная резекция Лобэктомия Пневмонэктомия Характер операции Радикальная паллиативная Состояние внутригрудных л/у N- N+ | 155 203 233 102 23 160 198 87 122 228 69 61 95 35 229 109 20 358 54 342 70 | 27,6+3,8 25,5+2,3 29,7+2,1 18,5+3,1 0,0 37,9+4,1 20,3+2,9 52,4+5,3 22,6+3,6 34,9+3,1 21,7+4,8 14,7+4,5 30,1+4,2 13,5+5,4 26,7+3,1 35,8+5,2 17,8+9,2 32,5+2,2 7,4+4,3 36,2+1,9 0 | 0,1900 0,01* 0,0434* 0,02* 0,0243* 0,0115* 0,0672 <0,001* <0,001* |
* различия статистически значимы
** для больных с единичными и множественными метастазами
Анализ однородных групп больных показал, что прогностическая значимость величины DFI максимальна у больных солитарным метастазом, перенесших радикальную операцию при отсутствии поражения внутригрудных лимфатических узлов. В случае одновременного выявления первичной опухоли и метастаза в легком (DFI=0) следует рассмотреть возможность радикального лечения обеих локализаций с учетом чувствительности опухоли к химио-гормоно-иммунотерапии. Вопрос о симультанной или последовательной операции необходимо решать индивидуально в зависимости от функционального состояния больного. Трех и пятилетняя выживаемость в этой группе больных составила 17,3%+5,6 и 13,0%+4,9 соответственно, что не уступает результатам лечения при DFI<36 мес. (p>0,05) (рис.7).

Рис.7. Выживаемость больных при DFI=0
В целом прямая зависимость отдаленных результатов от величины DFI характерна для всей группы больных, однако при единичных и множественных метастазах этот фактор не является решающим. Также не отмечено статистически значимых различий выживаемости в зависимости от гистогенеза опухоли, за исключением больных, оперированных по поводу метастазов меланомы, клиническое течение которых отличается крайне неблагоприятным прогнозом (пять лет не пережил ни один больной). Отдаленные результаты лечения больных с солитарным метастазом оказались лучше, чем единичными и множественными. Статистически значимых различий выживаемости между последними группами больных в случае радикального характера операции не отмечено. В случае паллиативной операции и выявлении метастазов во внутригрудных лимфатических узлах прогноз хирургического лечения плохой.
Таким образом, благоприятными факторами прогноза (на основе монофакторного анализа) являются: солитарный метастаз, DFI>=36 мес.(у больных с солитарным метастазом), одностороннее поражение легкого при единичных и множественных метастазах, отсутствие метастазов во внутригрудных лимфатических узлах, «радикальный» характер операции, а неблагоприятными – единичные/множественные метастазы, DFI<36 мес., метастаз меланомы, двустороннее поражение легких, наличие метастазов во внутригрудных лифатических узлах и паллиативный характер операции.
Многофакторный анализ показал, что состояние внутригрудных лимфатических узлов и характер выполненной операции являются независимыми показателями, определяющими судьбу больного оперированного по поводу метастазов в легких (табл. 6).
Таблица 6
Результаты многофакторного анализа у больных, оперированных по поводу метастазов в легких (регрессионная модель Кокса пропорционального риска)
| Фактор | Относительный риск | 95% ДИ* | р |
| Количество метастазов 1 >1 Локализация односторонняя двусторонняя DFI >36 мес. <36 мес. Состояние внутригрудных л/у N+ N- Характер операции паллиативная радикальная | 1 1,910 1 1,371 1 1,630 1 0,352 1 0,352 | 0,595-6.130 0,543-2,526 0,524-4,230 0,142-0,875 0,170-0,726 | 0,2765 0,6879 0,5670 0,0246 0,0047 |
* доверительный интервал
Иными словами, удаление всех выявленных метастазов («радикальная» операция) и их отсутствие в лимфатических узлах легкого и средостения являются независимыми благоприятными факторами прогноза и наоборот, паллиативная операция и поражение внутригрудных лимфатических узлов – неблагоприятными.
Таким образом, стратегия лечения больных с метастазами в легких должна основываться на дифференцированном подходе к выбору лечебной тактики в зависимости от чувствительности первичной опухоли и ее метастазов к лекарственному противоопухолевому лечению; комплексной оценке совокупности прогностических факторов; агрессивной тактике в отношении единичных, множественных, включая двусторонние, а также «рецидивных» метастазов. Одновременное выявление первичной опухоли и метастаза, наличие метастазов колоректального рака в легком и печени не является противопоказанием к активной лечебной тактике.
Выводы
- Хирургический метод является основным в лечении больных с метастазами в легких опухолей обладающих низкой чувствительностью к химио-гормоно-иммунотерапии (рак толстой кишки, почки, шейки матки, саркома мягких тканей), а при метастазах чувствительных к указанному лечению (рак молочной железы, эндометрия, опухоли яичка, остеогенная саркома) – составной частью комплексного подхода.
- Хирургический метод в лечении солитарного метастаза обоснован и позволяет добиться пятилетней выживаемости у 34,9% больных, а после удаления метастаза рака толстой кишки, почки, молочной железы, саркомы мягких тканей 28,2%, 23,7%, 15,8% и 9,8% больных соответственно переживают десятилетний срок наблюдения.
- Хирургическая тактика у больных с единичными/множественными метастазами является прерогативой современной клинической онкологии и в сочетании с лекарственным противоопухолевым лечением позволяет достигнуть удовлетворительных отдаленных результатов. Пятилетняя выживаемость – 21,7% и 14,7% соответственно.
- При одновременном выявлении первичной опухоли и метастаза в легком рака почки, толстой кишки и саркомы мягких тканей оправдана активная тактика по отношению к обеим локализациям. Трех- и пятилетняя выживаемость после удаления первичной опухоли и метастаза составила 17,3% и 13,0%.
- Повторные оперативные вмешательства при «рецидивных» метастазах оправданы у ограниченного контингента больных с изолированным поражением легких. Отдаленные результаты подобных операций удовлетворительные – 45,3% и 25,7% больных переживают трех- и пятилетний срок наблюдения.
- Отдаленные результаты видеоторакоскопической резекции легкого при солитарном метастазе не уступают стандартной хирургии (трехлетняя выживаемость – 30,0%).
- При двусторонних метастазах методика видеоассистированного их удаления является альтернативой стернотомии и билатеральной торакотомии. Двусторонние одномоментные и повторные (по поводу «рецидивных» метастазов) оперативные вмешательства относительно безопасны, частота осложнений (27,3% и 20,7%) и летальность (0% и 6,7%) достоверно не отличается от таковых показателей в группе больных оперированных однократно (10,4% и 1,2%) (p>0,05).
- Наиболее значимыми факторами, определяющими прогноз лечения больных с метастазами в легких, являются: гистогенез опухоли, количество метастазов, одно- или двусторонняя их локализация (для единичных и множественных метастазов), величина безметастатического периода (для солитарного метастаза), характер выполненной операции («радикальная» или паллиативная) и состояние внутригрудных лимфатических узлов. Паллиативный характер операции и наличие метастазов во внутригрудных лимфатических узлах являются независимыми факторами крайне неблагоприятного прогноза: пятилетняя выживаемость составляет 7,4% и 0% соответственно.
- Информативность компьютерной томографии в диагностике метастазов в легких значительно превышает таковую стандартного рентгенологического исследования, позволяя выявить дополнительные образования у 21,3% больных, что может повлиять на выбор лечебной тактики.
- Комплексная методика компьютернотомографического исследования высокоинформативна в дифференциальной диагностике солитарной метастатической опухоли легкого (чувствительность – 96,4%, специфичность – 98,8%, диагностическая точность – 98,3%).
- Видеоторакоскопия – малотравматичный метод окончательной диагностики изменений в легких, плевре и внутригрудных лимфатических узлах, при этом у 35,0% больных ранее леченных по поводу злокачественного новообразования внелегочной локализации удается исключить прогрессирование опухолевого процесса.
Практические рекомендации
- Компьютерную томографию органов грудной клетки следует включать в обязательный алгоритм обследования больных с метастазами в легких.
- При невозможности верификации изолированных изменений в легких, плевре и внутригрудных лимфатических узлах малоинвазивными методами (трансторакальная пункция, бронхологическое исследование) у больных ранее леченных по поводу злокачественной опухоли внелегочной локализации целесообразно использовать видеоторакоскопию как наиболее надежный метод окончательной диагностики.
- Исследование уровня сывороточных маркеров (РЭА, Tu M2PK, SCC, CA 19-9 и др.) необходимо проводить на всех этапах лечения больных с метастазами в легких в зависимости от локализации и гистогенеза первичной опухоли с целью мониторинга и оценки эффективности противоопухолевого воздействия. При повышении уровня маркера от исходного в процессе динамического наблюдения показано углубленное обследование больного с целью выявления субклинического рецидива болезни.
- Выбор метода лечения у больных с метастазами в легких зависит от гистогенеза первичной опухоли и чувствительности метастазов к лекарственной противоопухолевой терапии. При морфологически подтвержденных метастазах высокочувствительных опухолей (опухоли яичка, остеогенная саркома, рак молочной железы, эндометрия) на первом этапе следует проводить лекарственное лечение, а при его неэффективности – рассмотреть вопрос об оперативном вмешательстве. При невозможности морфологической верификации солитарного образования в легком операцию выполняют с диагностической и лечебной целью. Адъювантную лекарственную противоопухолевую терапию назначают после планового морфологического исследования в зависимости от гистогенеза опухоли. При метастазах опухолей, чувствительных к гормонотерапии (рак молочной железы, эндометрия) обосновано определение уровня рецепторов к эстрогену, прогестерону иммуногистохимическим методом, как в ткани первичной опухоли, так и в удаленном метастазе, что позволяет выбрать оптимальную лечебную тактику. При резектабельных метастазах опухолей резистентных к химио-гормоно-иммунотерапии оперативное вмешательство является методом выбора.
- Основной тип операции при метастазах в легких – сублобарная резекция (атипичная, прецизионное удаление, сегментэктомия). Показания к пневмонэктомии должны быть строго обоснованы.
- При солитарном метастазе допустима видеоторакосокпическая резекция легкого с использованием интраоперационного ультразвукового исследования.
- При двусторонних метастазах и удовлетворительных функциональных резервах больного целесообразна одномоментная операция из билатерального торакотомного или стернотомного доступа и как альтернатива – методика их видеоассистированного удаления. При сомнениях в переносимости одномоментного вмешательства следует разделить его на два этапа с интервалом в 3 – 4 недели.
- При «рецидивных» метастазах показаны повторные оперативные вмешательства, которые следует выполнять в специализированных учреждениях, обладающих достаточным опытом подобных операций.
- При одновременном выявлении первичной опухоли и метастаза в легком рака почки, толстой кишки и саркомы мягких тканей оперативное вмешательство по поводу метастаза целесообразно только при условии радикального удаления первичного очага. Симультанные операции допустимы у больных с удовлетворительными функциональными резервами.
- Сочетание нескольких неблагоприятных прогностических факторов (метастазы во внутригрудных лимфатических узлах, двусторонние метастазы в легких, короткий DFI, метастаз меланомы) ставит под сомнение целесообразность оперативного вмешательства ввиду крайне неудовлетворительных отдаленных результатов.
Список работ опубликованных по теме диссертации
- Хирургическая тактика при метастазах рака молочной железы в легких// Материалы конференции «Современные проблемы клинической онкопульмонологии». Мурманск, 2002 г., стр. 112 – 114 (соавт.: Трахтенберг А.Х.).
- Видеоторакоскопия в диагностике и лечении больных с заболеваниями легких, плевры и средостения// Эндоскопическая хирургия, 2003г., приложение, стр. 137 – 138 (соавт.: Трахтенберг А.Х., Гришин Н.А., Поляков В.А.).
- Метастаз базалиомы в легком у больной с первично-множественными злокачественными опухолями// Российский онкологический журнал, 2003г., № 4, стр. 45 – 47 (соавт.: Трахтенберг А.Х., Рудаков Р.В.)
- Современные возможности хирургии метастазов в легких// Материалы IY Всероссийской конференции молодых ученых «Актуальные вопросы клинической и экспериментальной онкологии», Москва, 2003г., стр. 110 – 111.
- Хирургия метастазов в легких// Материалы 13 Национального конгресса по болезням органов дыхания. Санкт-Петербург, 2003г., стр.127 (соавт.: Трахтенберг А.Х., Паршин В.Д.)
- Роль хирургии в лечении метастатических опухолей легких// Материалы научно-практической конференции онкологов Федерального управления «Актуальные вопросы онкологии и онкологической помощи в системе Федерального управления медико-биологических и экстремальных проблем». Москва, 2004г., стр. 124 – 127 (соавт.: Трахтенберг А.Х., Паршин В.Д.)
- Место хирургии в лечении метастатических опухолей легких// Материалы научно-практической конференции «Здоровье человека: реалии и перспективы». Ростов-на-Дону, 2004г., стр. 79 – 81 (соавт.: Трахтенберг А.Х., Паршин В.Д.)
- Surgery of pulmonary metastases: a multimodality concept// Eur J Surg Oncol, 2004, V. 30, № 2, p. 198 (соавт.: Трахтенберг А.Х., Паршин В.Д.).
- Хирургия двусторонних метастазов в легких// Российский онкологический журнал, 2004г., № 1, стр. 4 – 7 (соавт.: Чиссов В.И., Трахтенберг А.Х., Паршин В.Д.)
- Метастатические опухоли легких: современные подходы к хирургическому лечению// Российский онкологический журнал, 2004г., № 1, стр. 49 – 51.
- Циторедуктивные операции при метастатическом колоректальном раке// Вестник Московского онкологического общества, 2004г., № 2, стр. 2 – 3 (соавт.: Чиссов В.И., Вашакмадзе Л.А., Сидоров Д.В., Хомяков В.М.)
- Одномоментные операции у онкологических больных// Материалы межрегиональной научно-практической конференции «Дифференциальная диагностика и лечение рака легкого». Пермь, 2004г., стр. 84 – 87 (соавт.: Трахтенберг А.Х., Колбанов К.И.).
- Роль торакоскопии в диагностике внутригрудных изменений у больных ранее леченных по поводу злокачественных опухолей// Материалы межрегиональной научно-практической конференции «Дифференциальная диагностика и лечение рака легкого». Пермь, 2004г., стр. 87 – 90 (соавт.: Трахтенберг А.Х., Колбанов К.И.).
- Хирургия метастазов сарком в легких// Материалы межрегиональной научно-практической конференции «Дифференциальная диагностика и лечение рака легкого». Пермь, 2004г., стр. 81 – 84 (соавт.: Трахтенберг А.Х., Паршин В.Д.).
- Хирургия двусторонних метастазов в легких// Материалы межрегиональной научно-практической конференции «Дифференциальная диагностика и лечение рака легкого». Пермь, 2004г., стр. 77 – 80 (соавт.: Трахтенберг А.Х., Паршин В.Д.).
- Ошибки в диагностике и лечении злокачественных опухолей легкого// Терапевтический архив, 2004г., №10. стр. 5 – 12 (соавт.: Чиссов В.И., Трахтенберг А.Х., Колбанов К.И.).
- Роль хирургии в комплексном лечении больных с внутрилегочным солитарным метастазом рака молочной железы// Российский онкологичекий журнал, 2004г., № 6, стр. 26 – 29 (соавт.: Трахтенберг А.Х., Пикин О.В.).
- Циторедуктивные вмешательства при генерализованном раке почки// Материалы конференции «Онкологическая урология: от научных исследований к клинической практике (современные возможности диагностики и лечения опухолей предстательной железы, мочевого пузыря и почки). Москва, 2004г., стр. 127 (соавт.: Русаков И.Г., Шевчук И.М.).
- Место хирургического метода в лечении метастатических опухолей легких// Вестник Московского онкологического общества, 2005г., № 6 – 8., стр. 3 – 4 (соавт.: Чиссов В.И., Трахтенберг А.Х., Колбанов К.И.).
- Хирургическое лечение метастазов колоректального рака в легких// Российский онкологический журнал, 2005г., № 4, стр. 18 – 21 (Трахтенберг А.Х., Паршин В.Д.)
- Хирургия метастазов сарком в легких// Российский онкологический журнал, 2005г., № 5, стр. 4 – 7 (Чиссов В.И., Трахтенберг А.Х., Паршин В.Д.)
- Место хирургии в лечении метастазов в легких// Материалы YI Всеросийского съезда онкологов в книге «Современные технологии в онкологии». Ростов-на-Дону, 2005г.. том.1, стр. 340 – 341 (соавт.: Трахтенберг А.Х., Паршин В.Д.)
- Циторедуктивные операции в лечении метастатического колоректального рака// Материалы YI Всеросийского съезда онкологов в книге «Современные технологии в онкологии». Ростов-на-Дону, 2005г.. том.1, стр. 237 – 239 (соавт.: Вашакмадзе Л.А., Трахтенберг А.Х., Сидоров Д.В., Хомяков В.М., Ложкин М.В.)
- Резекция отдаленных метастазов при генерализованном раке почки// Материалы YI Всероссийского съезда онкологов в книге «Современные технологии в онкологии». Ростов-на-Дону, 2005г.. том.1, стр. 416 (соавт.: Русаков И.Г., Шевчук И.М.)
- Возможности циторедуктивной хирургии при метастатическом колоректальном раке// Материалы Российской научно-практической конференции с межднародным участием «Новые технологии в онкологической практике». Барнаул, 2005г., стр. 15 – 16.
- Циторедуктивные операции при метастазах рака почки// Российский онкологический журнал, 2006г., №1, стр.12 – 16 (соавт.: Русаков И.Г., Трахтенберг А.Х., Паршин В.Д., Шевчук И.М.).

