Кинетические эффекты совместного ингибирующего действия – токоферола с природными соединениями изопреноидного строенния и фосфолипидами
На правах рукописи
ДАРЮХИНА
ЕЛЕНА НИКОЛАЕВНА
КИНЕТИЧЕСКИЕ ЭФФЕКТЫ СОВМЕСТНОГО
ИНГИБИРУЮЩЕГО ДЕЙСТВИЯ
– ТОКОФЕРОЛА С ПРИРОДНЫМИ СОЕДИНЕНИЯМИ ИЗОПРЕНОИДНОГО СТРОЕННИЯ И ФОСФОЛИПИДАМИ
Специальность 02.00.04 – Физическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
Тюмень, 2004
Работа выполнена в ГОУ ВПО
«Тюменская государственная медицинская академия Минздрава России»
Научный руководитель:
доктор химических наук, профессор Сторожок Н.М.
Официальные оппоненты:
доктор химических наук, профессор Касаикина О.Т.
доктор химических наук, профессор Паничева Л.П.
Ведущая организация:
Московская государственная академия тонкой химической
технологии им. М.В. Ломоносова
Защита состоится « 29 » декабря 2004 г. в 13 часов на заседании диссертационного совета Д 212.273.06 в Тюменском государственном нефтегазовом университете.
По адресу: 625000, г. Тюмень, ул. Володарского, 38, аудитория 219, ТюмГНГУ.
С диссертацией можно ознакомиться в библиотеке ТюмГНГУ.
Автореферат разослан « » ноября 2004 г.
Ученый секретарь
диссертационного совета,
доктор химических наук,
профессор И.Г. Жихарева
ВВЕДЕНИЕ
Актуальность проблемы. В настоящее время из природных источников выделено и идентифицировано множество соединений изопреноидного строения. К ним относят витамины группы D (D2 – D7), а также обширную группу природных пигментов - каротиноидов, включающих более 700 веществ /Спиричев В.Б., 1989, Бауман В.К., 1989, Бриттон Г., 1986, Edge R. 2000, Ладыгин В.Г., 2001, Barros M.P., 2001, Jackson H.L.,2004, McArdle F., 2004, Li W., 2003, 2004/. Каротиноиды, имеющие в своей структуре от 10 до 13 двойных связей, окрашены в оттенки желтого, розового, оранжевого, красного, фиолетового цвета. Находясь в природе минорных количествах, они определяют окраску многих растений и живых организмов. Ряд соединений этого класса синтезированы и стали объектом всестороннего изучения их физико-химических свойств, антиоксидантного (АО), биологического и лечебного действия.
Значительный интерес представляет исследование влияния природных пигментов и витаминов на процесс окисления, поскольку существуют широкие перспективы практического использования биоантиоксидантов (биоАО) для стабилизации окисления полиненасыщенных липидов природного, биотехнологического происхождения, пищевых масел, лекарственных препаратов, нутрицевтиков, косметических средств.
Исследованию роли изопреноидов в процессе окисления посвящено ряд работ, касающихся преимущественно -каротина (провитамина А) /Krinsky N.I., 1993, Касаикина О.Т., 1975, 1995, 1998, Сторожок Н.М., 1996, 1997, Terao J., 1994, Miller N., 1996, Grabtree D.V., 1997, Edge R., 1997, 2000, Chen G. 2001, Kasaikina O.T., Vedutenko V.V. 2002, McArdle F.,2004, Hix L.M., 2004/ и витамина D2 /Спиричев В.Б., 1971, 1975, 1977/. Показано, что -каротин является ингибитором свободнорадикального окисления /Krinsky N.I., 1993, Tsuchihashi H., 1995, Miller N., 1996, Grabtree D.V., 1997, Edge R., 1997, 2000/, а витамин D2 может инициировать этот процесс /Спиричев В.Б., 1975, 1977/ Имеются единичные работы, в которых при изучении модельных систем, а также в опытах на животных отмечалась возможность инверсии и значительного усиления реакции окисления в присутствии высоких доз -каротина /Сторожок Н.М., 1996, Ланкин В.З., 1999/ или витамина D2 /Спиричев В.Б., 1975, 1977, Исаева В.А., 1975/.
При клиническом применении показано иммуномоделирующее, антиоксидантное действие -каротина в малых дозах /Буюклинская О.В., 1992, Утешев Б.С., 1998, 1999, Тихазе А.К., 1999/, при длительном приеме высоких доз установлено увеличение риска и смертности от онкозаболеваний /Mayne S.T., Handelman G.J., 1996, Albanes D., 1999, Baker D.L., Krol E.S., 1999/. Эти данные указывают на необходимость дальнейшего изучения особенностей действия -каротина, исследования характера зависимости доза-эффект.
Среди идентифицированных к настоящему времени изопреноидов повышенный интерес вызывает астаксантин (3,31-дигидрокси – 4,41-дикето-бета-каротин) /Di Mascio Р., 1989, Oshima S., 1993, Lim B.H., 1992, Terao J., 1992, Jyonouchi, 1993, Tanaka, 1994, Lee S.J., 2003, Li W., Hellsten A. 2004, Jacobsson L.S. 2004/ и холекальциферол (витамин D3) /Кузьменко А.И., Морозова Р.П., 1997, 1999, Ku'menko A.I. Morozova R.P. 1997, 1999/.
В современной литературе имеются единичные данные об антиоксидантной активности астаксантина /Lim B.H., 1992, Oshima S., 1993, Miki W., 1991/ и витамина D3 /Кузьменко А.И., Морозова Р.П, 1997, 1999/, которые, однако, достаточно противоречивы.
Известно, что каротиноиды и витамины группы D в фосфолипидном бислое биологических мембран присутствуют вместе с -токоферолом (-ТФ) - основным природным антиоксидантом (АО) /Milon A., 1986, Barclay L.R.C., 1994/. В связи с этим немаловажным представляется изучение характера совместного действия каротиноидов и -ТФ, являющихся важнейшими компонентами системы АО защиты клетки. В литературе имеются единичные сведения о возможности взаимодействия биоАО в процессе окисления. Ранее были получены данные, констатирующие при окислении яичного фосфатидилхолина (ФХ) эффекты синергизма в совместном действии -каротина и -ТФ /Terao J., 1980, Palozza P., 1991, Olma F., 1993, Tesoriere L., 1996/. Известны также работы, показывающие, что без фосфолипидов в действии указанные биоАО проявляется эффект антагонизма /Сторожок Н.М., 1996, Сторожок Н.М., Кутузова И.В., 1995, 1996, 1997/.
Работ, посвящённых изучению совместного действия -ТФ и астаксантина или витамина D3 в модельных системах различной сложности, в современной литературе не найдено. Таким образом, отсутствие исследований и противоречивость имеющихся в литературе данных свидетельствуют о необходимости системного изучения кинетических эффектов действия индивидуальных природных антиоксидантов и их смесей на процесс окисления модельных систем различной сложности, выявления особенностей концентрационных зависимостей, установления взаимосвязи между строением и ингибирующими свойствами изопреноидов.
Целью настоящей работы являлось сравнительное изучение закономерностей окисления модельных систем в присутствии индивидуальных природных соединений изопреноидного строения (-каротина, астаксантина, витамина D3), исследование кинетических эффектов их совместного действия с -токоферолом, поиск путей усиления эффективности в композиции с синтетическими АО и фосфолипидами.
Задачи исследования.
- Исследовать кинетику инициированного окисления модельного субстрата метилолеата (МО) в присутствии индивидуальных -каротина, астаксантина и витамина D3. Выявить особенности брутто-ингибирующего действия веществ от концентрации всех исследуемых АО в среде неполярного растворителя (хлорбензола) и в микрогетерогенной системе, образованной добавками анионного ПАВ (додецилсульфата натрия).
- Методом термохемилюминесценции изучить антирадикальную активность указанных соединений, оценить значение константы k7.
- Исследовать кинетические эффекты совместного ингибирующего действия бинарных смесей -ТФ с -каротином, астаксантином или витамином D3.
- Количественно изучить кинетику расходования -токоферола в присутствии витамина D3 и -каротина методом УФ- и ИК– спектроскопии.
- Установить характер и кинетические закономерности совместного ингибирующего действия композиций, включающих дополнительно к -ТФ, -каротину или витамину D3 фосфолипиды (яичный фосфатидилхолин).
- Показать возможности стабилизации систем, содержащих -каротин, при введении нового нетоксичного синтетического антиоксиданта – (бис-3-(4/-гидрокси-3/,5/-дитрет.бутил фенил)-пропил сульфида) (СО-3).
Материалы и методы исследования. В работе использованы манометрический метод поглощения кислорода, метод термохемилюминесценции, методы УФ- и ИК-спектроскопии, метод Ребиндера определения критической концентрации мицелообразования.
Исследуемые пинменты (-каротина, астаксантин) предоставлены ФГУ Институт витаминов, использовали витамин D3 (холекальциферол), дибунол фирмы (Sigma), Германия, -токоферол фирмы «Serva» США. Синтетический антиоксидант (СО-3) -бис-3-(4/-гидрокси-3/,5/-дитрет. бутилфенил)н.-пропил сульфид и метилолеат (МО) синтезированы в НИОХ им. В.В. Ворожцова СО РАН. МО очищен перегонкой под вакуумом при остаточном давлении 5 мм. рт. ст. Применяли эмульгатор додецилсульфат натрия (SDS) и яичный фосфатидилхолин фирмы «Serva», США. В качестве растворителей использовали хлорбензол, четырёххлористый углерод марки «ОСЧ» сорт 2. Растворители очищали методом простой перегонки.
Достоверность результатов
Результаты экспериментов обработаны статистически с использованием компьютерной программы на языке QBasic. Достоверность результатов определялась с использованием t-критерий Стьюдента (Г.Корн, Т.Корн, 1970).
Научная новизна. Впервые изучены особенности ингибирующего действия астаксантина в модельной системе инициированного окисления метилолеата в микрогетерогенной системе, образованной добавками анионного поверхностно активного вещества (ПАВ) (додецилсульфата натрия) к водно-органической среде. Показан экстремальный характер изменения эффективности от количества астаксантина в системе окисления. Показаны диапазоны концентраций, обеспечивающие максимальное торможение процесса. Установлено, что витамин D3 участвует в инициировании окисления. Впервые оценены константы элементарной реакции взаимодействия астаксантина с пероксильными радикалами (k7). Показано, что астаксантин проявляет антирадикальную активность, на порядок превосходящую активность -каротина. Холекальциферол в указанной реакции не активен.
В диссертационной работе впервые кинетически изучены эффекты совместного ингибирующего действия -ТФ с астаксантином и витамином D3. Установлена общая для всех закономерность изменения эффективности действия композиций -ТФ с -каротином, астаксантином или витамином D3. Было показано, что при разных молярных соотношениях в действии компонентов возможно проявление аддитивности, эффектов синергизма или антагонизма. При одном и том же количестве -ТФ зависимость изменения эффективности от концентрации -каротина или атаксантина описывается U-образной кривой, а для смеси -ТФ -холекальциферол носит линейный характер.
Показано, что эффективность действия смесей зависит от молярных соотношений -ТФ и полиена, количества в его структуре сопряженных -связей. Установлены соотношения концентраций -ТФ и -каротина, астаксантина или витамина D3 в смесях, которые будут обеспечивать высокую эффективность совместного действия за счет проявления эффектов синергизма. Показано, что синергизм в совместном действии -ТФ с витамином D3 наблюдается при отношении их концентраций, превышающей 100:1, для композиций -ТФ с -каротином - при молярном соотношении, большем чем 4:1. Для бинарной системы -ТФ: астаксантин – область синергизма отвечает соотношению указанных компонентов, больших 12:1.
Предложен способ увеличения действия -каротина в композиции с новым синтетическим ингибитором окисления (бис-3-(4/-гидрокси-3/,5/-дитрет.бутил фенил)-пропил сульфид (СО-3) или яичным фосфатидилхолином (ФХ).
Практическая значимость работы заключается в установлении концентрационных диапазонов, обеспечивающих максимальное ингибирование окисления в присутствии природных пигментов: -каротина, астаксантина. Сведения о максимальной эффективности этих соединений могут послужить основой для разработки новых рецептур составов, применяемых для стабилизации окисления липидных субстратов различного происхождения, лекарств, косметических средств, пищевых продуктов (масел, маргарина, йогуртов и других молочных продуктов). В расчете на липиды оптимальное содержание индивидуальных - токоферола, астаксантина и -каротина должно составлять 0,3% и 0,095%, 0,003% соответственно.
Показано, что для обеспечения окислительной стабильности систем, включающих витамин D3, требуется дополнительное введение -ТФ или его синергической композиции с фосфатидилхолином.
Результаты настоящей работы позволяют заключить, что применение в медицинской практике высоких доз -каротина, астаксантина или витамина D3 может способствовать ускоренному расходованию основного природного АО - -ТФ, что может привести к ослаблению антиоксидантной системы организма в целом и увеличению интенсивности пероксидного окисления липидов (ПОЛ) биологических мембран. Учитывая патогенетическое значение процессов ПОЛ должны быть проведены дополнительные фармакологические испытания действия разных доз -каротина, астаксантина и витамина D3, разработаны рекомендации их длительного безопасного применения.
Полученные в работе данные необходимо учитывать в технологии производства пищевых продуктов и нутрицевтиков, фармпрепаратов, косметики с целью длительного сохранения их биологической ценности и повышения окислительной устойчивости. Предложены способы стабилизации окисления смесей липидов с -каротином за счет дополнительного введения фосфолипидов или синтетического пространственно-затрудненного фенола (СО-3). Подобраны оптимальные соотношения компонентов, позволяющих значительно увеличить эффективность ингибирующего действия композиций.
Апробация работы. Материалы диссертации докладывались на международной конференциии “Биоантиоксидант”, Москва, 2002 г.; международных симпозиумах “Медицина и охрана здоровья” Тюмень, 1997, 1999, 2000, 2001, 2002, 2004 гг.; III международном симпозиуме “Биологически активные добавки – нутрицевтики и их использование с профилактической и лечебной целью при наиболее распространенных заболеваниях” Тюмень, 1997; международной конференции “Химия органических и элементорганических пероксидов”, Москва, 1998 г.; V Национальном конгрессе “Человек и лекарство”, Москва, 1998; международной конференции “Свободнорадикальные процессы: фармакологические, клинические, биологические аспекты”, Санкт-Петербург, 1999; «Терапевтическом форуме», Тюмень, 2000 г.; региональных и всероссийских межвузовских конференциях молодых ученых и студентов “Актуальные проблемы теоретической, экспериментальной и клинической медицины”, Тюмень, 2001, 2002, 2003, 2004 гг., VI конгрессе молодых учёных и специалистов «Науки о человеке», Томск, 2003 г.
Публикации. Основной фактический материал и выводы диссертации опубликованы в 21 работе (8 журнальных статей и 13 тезисов докладов).
Положения работы, выносимые на защиту:
1. Антирадикальная активность (k7) и особенности брутто-ингибирующего действия непредельных соединений (астаксантина, -каротина и витамина D3).
2. Кинетика совместного ингибирующего действия -токоферола с астаксантином, -каротином или витамином D3.
3. Кинетика расходования -токоферола в присутствии витамина D3 и -каротина.
4. Кинетические закономерности совместного ингибирующего действия композиций, включающих фосфолипиды (фосфатидилхолин), -токоферол и -каротин или витамин D3.
5. Перспективы стабилизации окисления липидов и -каротина за счет введения нового синтетического АО - (бис-3-(4/-гидрокси-3/,5/-дитрет.бутил фенил)-пропил сульфида) (СО-3).
Объём и структура диссертации. Диссертация изложена на 159 страницах, содержит 14 таблиц 32 рисунка. Диссертация состоит из введения, обзора литературы, материалов и методов исследования, результатов собственных исследований, обсуждения, выводов, списка литературы.
СОДЕРЖАНИЕ РАБОТЫ
Глава 1. Исследование особенностей ингибирующего действия -каротина, астаксантина и витамина D3 (холекальциферола)
В сравнении изучено ингибирующее действие витамина D3, -каротина и астаксантина, которые включают в своей структуре 3, 11 и 13 сопряженных двойных связей соответственно (см. формулы, схема 1).
Схема 1
Формулы исследуемых соединений
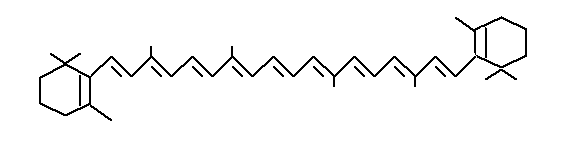 | |
| – КАРОТИН | |
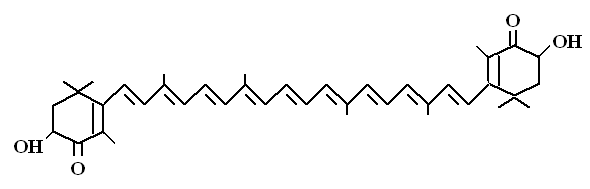 | |
| АСТАКСАНТИН, 3,31дигидрокси -4,41-дикето-бета-каротин | |
 Витамин D3 (холекалыциферол) 9,10,-секохолеста - 5, 7,10, (19)-триен-3-ол. Витамин D3 (холекалыциферол) 9,10,-секохолеста - 5, 7,10, (19)-триен-3-ол. | 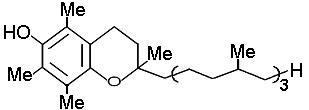 IV -токоферол 2,5,7,8 – тетраметил- 2-(4,8,12 триметилтридецил) хроман-6-ол IV -токоферол 2,5,7,8 – тетраметил- 2-(4,8,12 триметилтридецил) хроман-6-ол |
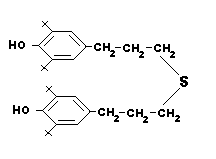 V (бис-3-(41–гидрокси-31,51-дитрет.бутилфенил)-пропил сульфида) (СО-3) V (бис-3-(41–гидрокси-31,51-дитрет.бутилфенил)-пропил сульфида) (СО-3) | 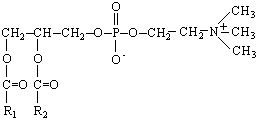 VI Фосфатидилхолин VI Фосфатидилхолин |
Брутто-ингибирующее действие веществ изучалось при инициированном окислении модельного субстрата МО в среде неполярного растворителя хлорбензола при их соотношении 1:1; а также в микрогетерогенной среде, образованной дополнительными добавками воды и анионного ПАВ додецилсульфата натрия (DDS). Концентрация ПАВ в опытах соответствовала критической концентрации мицеллообразования, установленной экспериментально (2,510-2 М). Микрогетерогенность системы с ПАВ была подтверждена методом электронной микроскопии, показано, что в выбранных условиях формируются обращенные мицеллы. Процесс инициировали за счет термического разложения азобисизобутиронитрила (АИБН) при 333 К.
Закономерности, полученные при изучении действия антиоксидантов и их смесей при окислении субстрата в среде неполярного растворителя, могут быть применены для описания окислительных превращений жиров, масел различного происхождения. Кинетика окисления в системе липид-вода в присутствии ингибиторов и их композиций могут использоваться для характеристики процесса окисления водно-жировых эмульсий, которые широко применяются как основы лекарственных и косметических средств, являются пищевыми продуктами (сметана, иогурты, майонезы, маргарины).
Известно, что важной характеристикой ингибиторов окисления является активность в реакции с пероксильными радикалами (RO2•), характеризуемая величиной константы k7. Тестирование методом хемилюминесценции антирадикальной активности астаксантина, -каротина и витамина D3 показало, что в реакции с пероксильными радикалами участвуют только пигменты (табл.1). Значение k7 эф. для астаксантина и -каротина составляет (1,3105)М-1с-1 и 1,4104 М-1с-1 соответственно (табл.1). Видно, что в сравнении с -ТФ, для которого было подтверждено известное из литературы значение k7, равное 3,6106 М-1с-1 /Кухтина Е.Н, 1983/, антирадикальная активность астаксантина и -каротина существенно ниже (соответственно в 27 и 260 раз). Для -каротина подтверждены литературные данные /Ozhogina O.A. 1995, Kasaikina O.T. 2002/. Антирадикальная активность астаксантина по сравнению с -каротином выше практически в 10 раз. Этот факт объясняется дополнительным введением в кольца ионона электроноакцепторов - гидрокси (-ОH) и оксо- (С=О) групп.
Витамин D3 в тех же условиях окисления не проявлял антирадикальной активности, что позволяет заключить, что он не является АО (табл.1).
При изучении кинетики окисления липидов в присутствии витамина D3, установлено увеличение скорости инициирования, окисляемости системы, характеризуемой кинетическим показателем k2/ k6 (рис. 1). Дибунол не влиял на величину этого кинетического показателя (рис. 1). При высоких количествах витамина D3 величина k2/ k6 уменьшается, что связано с увеличением скорости обрыва цепей в реакциях кросс - диспропорционирования. Исследовали начальную скорость поглощения кислорода смесей, включающих различные концентрации МО.
Таблица 1
Кинетические характеристики окисления МО в разных условиях окисления в присутствии -ТФ, -каротина, астаксантина и витамина D3, САИБН=3,010-3М, Т=333К
| № п/п | АО | Диапазон, соответствующий максимальному ингибирующему действию АО 10-4 М | Концентрация АО, соответствующая максимальному ингибирующему действию АО, 10-3 М | Период индукции в точке экстремума, мин | K7 10-4, М-1 с-1 | |||
| гомоген-ная среда | микроге-тероген-ная среда | гомогенная среда | микро-гетеро-генная | гомоген-ная среда | микроге-тероген-ная среда | |||
| 1 | -ТФ | 12,50 - 35,00 | 7,50-35,00 | 2,500 | 2,500 | 960 | 1800 | 360 |
| 2 | -каротин | 0,20 - 0,40 | 0,25- 0,75 | 0,027 | 0,027 | 100 | 115 | 1,4 |
| 3 | Астаксантин | - | 1,5-12,00 | - | 0,80 | - | 125 | 130 |
| 4 | Витамин D3 | 2,5-10,0 | - | 0,25 | - | 76 | - | - |
Из рис. 2 видно, что скорость процесса возрастает прямо пропорционально увеличению количества окисляемого вещества (рис.2, кривая 1). Кривая скорости окисления для композиций МО и витамина D3 располагается выше указанной линейной зависимости и носит экстремальный характер (рис.2, кривая 2). Эти данные указывают на то, что витамин D3 служит дополнительным источником свободных радикалов, что связано с его строением. Витамин D3 по сравнению с -каротином и астаксантином имеет существенно меньшую степень сопряжения системы -связей. Снижение длины, а, следовательно, и энергии делокализации сопряжённых связей приводит к образованию активных радикалов, способствующих дополнительному инициированию процесса. В присутствии витамина D3 наблюдалось повышение периодов индукции по сравнению с контролем (табл.1), что является следствием кросс-диспропорционирования радикалов, образующихся в системе окисления.
В литературе, однако, приводятся сведения об ингибирующем действии витамина D3, полученные при введении экспериментальным животным холекальциферола на фоне его недостаточности /Кузьменко А.И., 1997/, а также при изучении in vivo окисления липопротеидов низкой плотности,
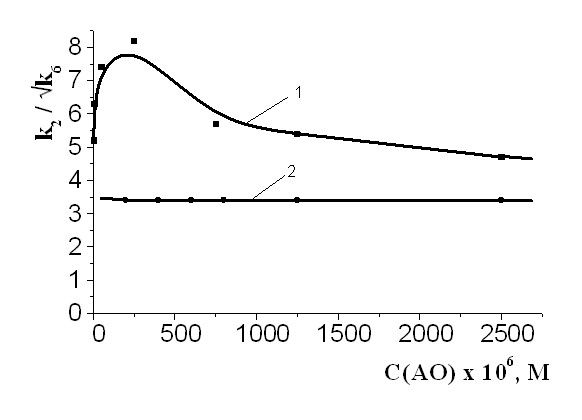 |  |
| Рис. 1 Зависимость окисляемости метилолеата (МО), содержащего витамин D3 (1) и дибунола от их концентрации, САИБН= 3,010-3 М. | Рис. 2 Зависимость начальной скорости окисления при различной концентрации МО (1), то же с постоянной концентрацией витамина D3 (2,510-4) М (2); САИБН=3,010-3М. |
микросомальной и митохондриальной фракций печени крыс /Кузьменко А.И., 1999/. Можно полагать, что описываемые в работах /Кузьменко А.И. 1997, 1999/ эффекты ингибирования обусловлены не витамином D3 а действием его метаболитов, образующихся в организме в результате реакций гидроксилирования. Ингибирующим действием может обладать, в частности, 1,25-дигидрокси витамин D3. Имеются данные, косвенно подтверждающие антиоксидантные свойства метаболитов холекальциферола /Brasitus T.A., 1986/. Таким образом, совокупность полученных нами данных показывает, что индивидуальный холекальциферол не является АО, он вовлекается в реакцию подобно субстрату и способствует дополнительному инициированию окисления.
При окислении МО в присутствии -ТФ в среде хлорбензола подтвержден описанный ранее в литературе экстремальный характер зависимости эффективности действия от концентрации АО /Храпова Н.Г., 1977, 1988, Бурлакова Е.Б., 1998/ (рис.3). Было показано, что при окислении в мицеллярных растворах воспроизводится аналогичная по форме концентрационная кривая. Обращает внимание, что вне зависимости от среды окисления положение точек экстремума, соответствующих наиболее эффективным концентрациям ингибитора, отвечают одному и тому же диапазону (7,50-35,00)10-4 М (табл.1). Значения периодов индукции в точках экстремума при окислении МО в среде неполярного растворителя и в системе, образованной добавками воды и ПАВ, различаются практически в 2 раза (960 мин и 1800 мин соответственно) (рис. 3).
Показано, что в водно-органических системах в присутствии анионного ПАВ - додецилсульфата натрия, формируются обращенные мицеллы /Карташева З.С., Максимова Т.В., Коверзанова Е.В., Касаикина О.Т., 1997/. В работе /Галявин А.А., Касаикина О.Т., 2003/ на примере гидропероксида кумила установлено, что концентрирующиеся в микрореакторах гидропероксиды в присутствии додецилсульфата автокаталитически распадаются с образованием молекулярных продуктов окисления (додецилового спирта – стабилизатора эмульсий 2 рода – обращенных мицелл и, по-видимому, фенолсульфокислоты). Предложенная концепция объясняет большую эффективность действия исследуемых веществ при окислении субстрата в микрогетерогенной среде по сравнению с гомогенатами липидов в хлорбензоле.
При исследовании действия -каротина показано, что как и для -ТФ, концентрационная кривая имеет экстремум (рис. 4, 5), который относится к узкому диапазону концентраций (табл.1). Концентрации, соответствующие максимальному действию -каротина, относительно малы (2-7)10-5М, однако, именно они соответствуют уровню каротиноидов в плазме крови /Шашкина М.Я., 1999/. Превышение содержания -каротина по сравнению с указанным уровнем приводит к значительному уменьшению эффектов торможения окисления.
Считают, что -каротин легко присоединяет алкильные и пероксильные радикалы, которые в дальнейшем обратимо присоединяют кислород. Эта реакция определяет сильную зависимость скорости расходования -каротина от концентрации кислорода в условиях инициированного окисления /Ведутенко В.В., Карташева З.С., Касаикина О.Т., 2002/. Авторы считают, что большую роль в торможении окисления играют продукты превращения -каротина в радикальных реакциях.
Показано, что в микрогетерогенной среде действие -каротина на 15% выше, чем при окислении в гомогенной системе, что обусловлено действием DDS /Галявин А.А., Касаикина О.Т., 2003/.
Ингибирующее действие астаксантина было изучено в среде неполярного растворителя с добавками воды и DDS. В сравнении с -каротином астаксантин более эффективен, его действие как ингибитора окисления проявляется в широком диапазоне концентраций (0,15-1,20)10-3М (табл. 1). Концентрационная кривая носит экстремальный характер (рис. 4). Указанные свойства биоАО обусловлены особенностями их структуры и различиями в стабильности их радикальных продуктов Модификация у астаксантина кольцевых структур электроноакцепторными –OH и С=О группами способствует увеличению жёсткости полиеновой -электронной системы и большей стабилизации по сравнению с -каротином образующихся при его окислении радикалов. Влияние указанных фрагментов приводит к некоторому увеличению брутто-ингибирующего действия астаксантина.
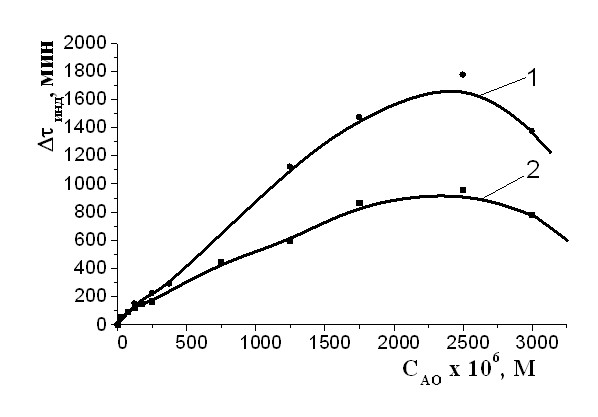 Рис. 3 Зависимость периодов индукции от концентрации -ТФ при окислении МО в водно-эмульсионной среде (1) и среде хлорбензола (2), СМО=0,85 М, САИБН=3,010-3М. Рис. 3 Зависимость периодов индукции от концентрации -ТФ при окислении МО в водно-эмульсионной среде (1) и среде хлорбензола (2), СМО=0,85 М, САИБН=3,010-3М. | 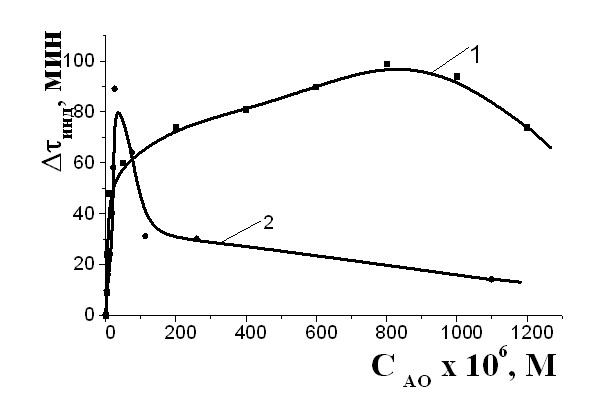 Рис. 4. Зависимость периодов индукции от концентрации астаксантина (1), -каротина (2) при окислении в водно-эмульсионной среде, СМО=0,85М, САИБН=3,010-3М. Рис. 4. Зависимость периодов индукции от концентрации астаксантина (1), -каротина (2) при окислении в водно-эмульсионной среде, СМО=0,85М, САИБН=3,010-3М. |
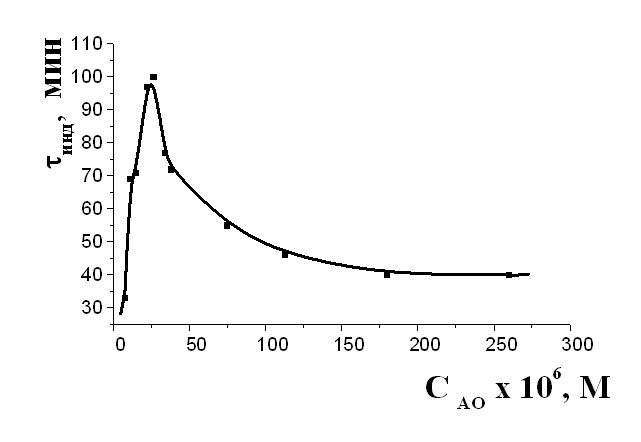 Рис. 5 Зависимость периодов индукции от концентрации -каротина при окислении в гомогенной среде. САИБН=3,010-3М. Рис. 5 Зависимость периодов индукции от концентрации -каротина при окислении в гомогенной среде. САИБН=3,010-3М. | |
Таким образом, для изучаемых нами природных АО установлен экстремальный характер зависимости между ингибирующим действием и количеством их в системе окисления. Можно полагать, что эта закономерность имеет важное регуляторное значение. Биологический смысл кривых заключается в том, что интенсивность неферментативных окислительных процессов может поддерживаться на стационарном уровне при изменении концентрации -ТФ или астаксантина в достаточно широком интервале. Нецелесообразно введение в организм высоких количеств природных ингибиторов в течение длительного времени, поскольку это может приводить не к повышению, а к ослаблению антиоксидантной защиты.
Сведения о максимальной эффективности - токоферола, -каротина и астаксантина полученные в настоящей работе, могут послужить основой для разработки составов, используемых для стабилизации окисления липидных субстратов различного происхождения, лекарственных препаратов, косметических средств, пищевых продуктов (масел, маргарина, молочных продуктов). В расчете на липиды оптимальное содержание индивидуальных - токоферола, астаксантина и -каротина должно составлять 0,3% и 0,095%, 0,003% соответственно.
Глава 2. Кинетика совместного антиоксидантного действия -токоферола с -каротином, астаксантином и витамином D3
Известно, что в природных объектах изучаемые нами соединения (-ТФ, витамин D3, -каротин, атаксантин) локализованы совместно. В связи с этим одной из задач настоящего исследования являлось выявления характера их взаимоотношений в процессе окисления липидов.
Попарно изучали ингибирующее действие смесей -ТФ с одним из перечисленных выше соединений. Сопоставляли между собой сумму периодов индукции опытов, в которых окисление МО ингибировалось индивидуальными соединениями (i), с эффектом, получаемым при совместном действии компонентов (). Эффективность действия смеси количественно оценивали по абсолютному значению, определяемому по уравнению = - i, либо в относительных единицах (/ i)х100%.
Количество -ТФ в опытах оставалось постоянным, а концентрация второго компонента изменялась в широком диапазоне. Совместное действие веществ исследовалось при окислении МО в среде хлорбензола и в системе липиды - вода, стабилизированной DDS.
Вне зависимости от условий окисления была установлена общая для всех закономерность изменения эффективности действия композиций -ТФ с -каротином, атаксантином или витамином D3 от их концентрации (рис. 6, 7, 8). Было показано, что при разных молярных соотношениях в действии компонентов возможно проявление аддитивности, эффектов синергизма или антагонизма. При одном и том же количестве -ТФ зависимость изменения эффективности от концентрации -каротина или атаксантина описывается U-образной кривой (рис. 7, 8), а для смеси -ТФ с холекальциферолом носит линейный характер (рис.6). Общность этих кривых заключается в том, что они располагаются в области синергизма и в области антагонизма. Для смесей с постоянным уровнем -ТФ показано, что знак эффекта: (+) - синергизм, (-) - антагонизм - определяется количеством второго компонента. При малых концентрациях пигментов или витамина D3 в их совместном действии с -ТФ констатируются эффекты синергизма. По мере роста количества соединений с сопряженными связями, уменьшается брутто-эффективность смеси за счет проявления эффектов антагонизма в действии составляющих (рис.6, 7, 8).
Изучен характер взаимосвязи между действием смесей и концентрацией -ТФ. Показано, что для композиций с одинаковым уровнем астаксантина эффективность смеси пропорциональна количеству антиоксиданта фенольной природы (-ТФ) (рис.9). Эта закономерность подтверждается для композиций -ТФ с другими полиненасыщенными сопряженными соединениями (-каротином и витамином D3).
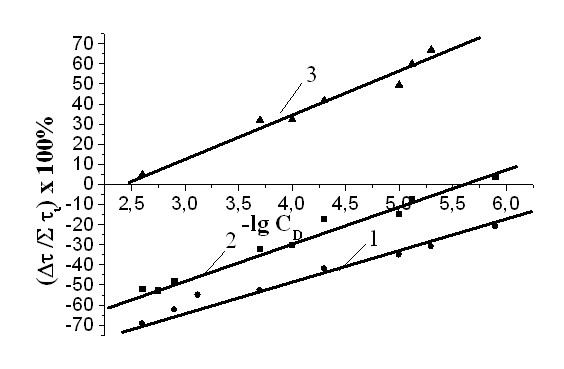 | 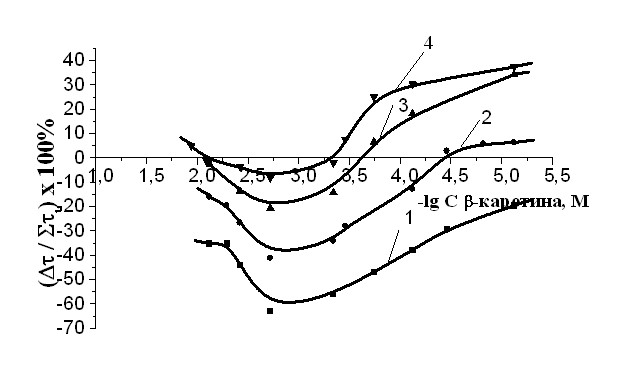 |
| Рис. 6 Полулогарифмические анаморфозы зависимостей эффективности смесей от концентрации витамина D3 в бинарных смесях с -ТФ (2,510-5) М (1) и (1,2510-4) М (2) и тройной смеси, включающей -ТФ (1,2510-4) М и яичный ФХ (1,010-3)М (3), САИБН=3,010-3 М. | Рис. 7 Полулогарифмические анаморфозы эффективности смесей от концентрации -каротина в бинарной смеси с -ТФ (2,510-5) М (1), (1,2510-4) М (2), (2,510-4) М (3) и тройной смеси, включающей дополнительно к смеси 3 яичный ФХ (1,010-3) М (4), САИБН=3,010-3 М. |
Величина эффекта антагонизма обратно пропорциональна количеству сопряженных связей в структуре полиена. При сравнимых концентрациях, например С-ТФ =1,2510-4М, Сполиена=1,810-3М, показано, что эффект антагонизма наиболее выражен для смесей -ТФ с витамином D3 (50%), для смеси -ТФ с -каротином он достигает 41,2%, а для композиции -ТФ с астаксантином – 15% (рис. 6, 7, 8). Видно, что возможность проявления эффектов антагонизма в совместном действии уменьшается пропорционально увеличению степени делокализации в сопряженной системе -связей.
В работе изучали влияние витамина D3 и -каротина на скорость окислительного превращения -ТФ. Методами и ИК- УФ- спектроскопии была изучена кинетика расходования -ТФ в смесях с различным содержанием - каротина и витамина D3. Показано, что кинетически выявляемый эффект антагонизма в действии -ТФ с полиенами сопровождается ускоренным расходованием наиболее эффективного антиоксиданта. Скорость расходования -ТФ связана экстремальной зависимостью с количеством полиена в смеси и может увеличиваться в 10-15 раз (рис. 10, 11). Таким образом, введение в субстрат дополнительно к -ТФ высоких доз -каротина или витамина D3 может способствовать ускоренной потере фенольного ингибитора и снижению окислительной стабильности системы в целом.
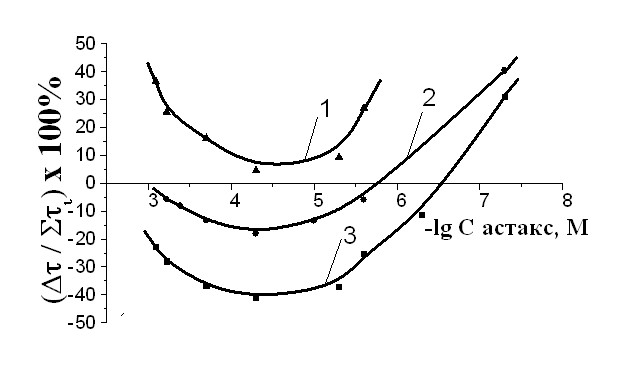 | 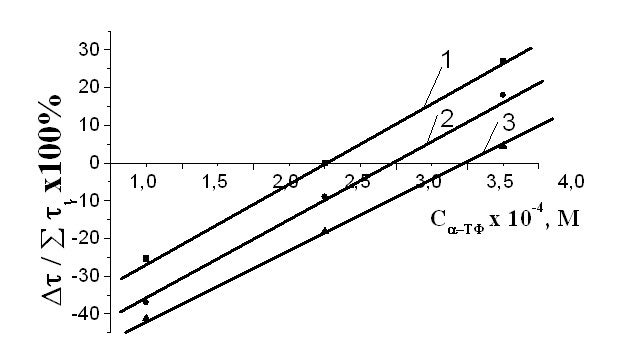 |
| Рис. 8 Зависимость эффективности смесей от концентрации астаксантина, при равных количествах -ТФ: 1 - (3,7510-4) М; 2 - (2,510-4) М ; 3 - (1,2510-4) М, САИБН=3,010-3М. | Рис. 9 Зависимость эффективности смеси от концентрации -ТФ с равными концентрациями астаксантина : 1 - (2,510-6) М; 2- (2,010-4) М; 3 - (5,010-5) М; САИБН=3,010-3М. |
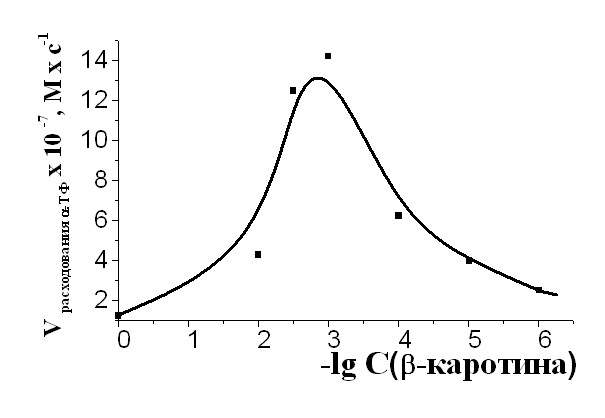 | 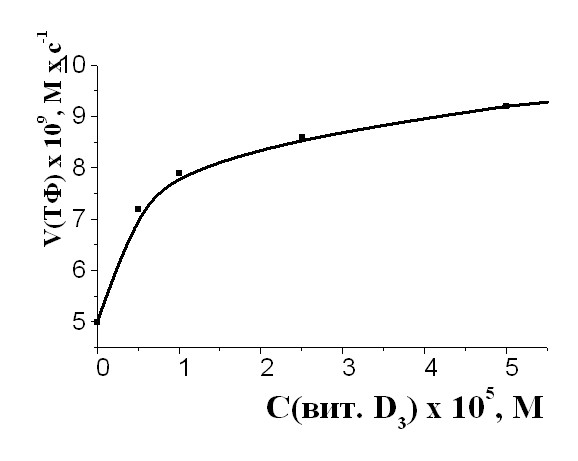 |
| Рис. 10 Зависимость скорости расходования -ТФ (3,010-3) М от концентрации -каротина в смеси, САИБН=9,010-3 М, Т=333К | Рис. 11 Зависимость скорости расходования -ТФ от концентрации витамина D3, С-ТФ =const= 2,510-5 М, САИБН=3,010-3М, Т=333К |
В свете полученных данных целесообразно пересмотреть практику применения высоких доз -каротина или холекальциферола с лечебной или профилактической целью. В том случае, если в организм будут длительно вводиться указанные соединения, то их концентрация в липидах биологических мембран может стать аномально высокой, что в свою очередь приведет к уменьшению пула -ТФ и интенсификации неферментативного окисления. Усиление процессов свободнорадикального окисления имеет патогенетическое значение и может являться пусковым механизмом развития многих заболеваний /Владимиров Ю.А., Арчаков А.И. 1972, Ланкин В.З., Тихазе А.К.2000, 2001/.
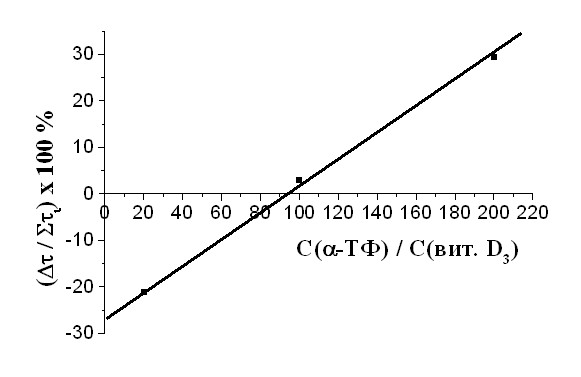 | 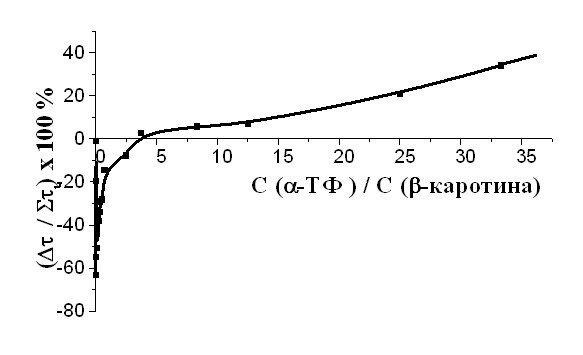 |
| Рис. 12 Зависимость эффективности действия смеси витамина -ТФ и D3 от их количественного соотношения в системе окисления, САИБН=3,010-3 М. | Рис. 13 Зависимость эффективности действия смеси -ТФ и -каротина от их количественных соотношений в системе окисления, САИБН=3,010-3 М. |
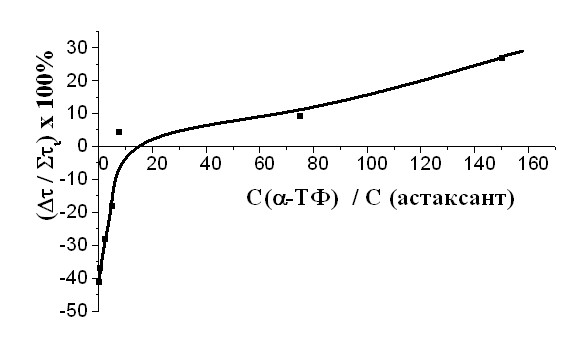 | |
| Рис. 14 Зависимость эффективности действия смеси -ТФ и астаксантина от их количественных соотношений в системе окисления, САИБН=3,010-3 М. | |
Была проанализирована взаимосвязь брутто-ингибирующего действия композиций от соотношения молярных концентраций -ТФ и второго компонента смеси (полиена). Было показано, что смена знака эффекта, переход совместного действия смеси из области антагонизма в область синергизма происходит при различных соотношениях -ТФ/полиен и зависит от количества в его структуре сопряженных -связей. Так, синергизм в совместном действии -ТФ с витамином D3 в структуре которого имеется 3 двойные связи, наблюдается при отношении концентраций, превышающей 100:1 (рис.12). Для композиций -ТФ с -каротином, включающим в молекуле 11 -связей, синергизм проявляется при отношении, большем чем 4:1 (рис.13). Для системы -ТФ: астаксантин – в водно-эмульсионной среде – область синергизма отвечает отношению компонентов, превышающему 12:1(рис.14).
Результаты настоящей работы имеют важное практическое значение, поскольку обосновывают отношения концентраций компонентов: -ТФ и -каротина или астаксантина или витамина D3, смеси которых будут обеспечивать высокую эффективность совместного действия за счет проявления эффектов синергизма.
Глава 3 Способы повышения окислительной устойчивости систем, содержащих соединения изопреноидного строения
Одной из задач работы являлся поиск способов стабилизации окисления ненасыщенных липидов, содержащих соединения изопреноидного строения, за счет введения в субстрат либо синтетических АО, либо синергических композиций.
Изучали пути стабилизации окисления систем, включающих пары веществ (-ТФ и витамин D3), (-ТФ и -каротин) в соотношениях, при которых в их совместном действии констатировался эффект антагонизма (глава 2). Были исследованы возможности повышения окислительной стабильности системы за счет дополнительного введения фосфолипидов. Использовали яичный лецитин фосфатидилхолин (ФХ).
Известно, что фосфолипиды (ФЛ) выполняют роль синергистов ингибиторов окисления /Hudson B.J., 1984, Hildebrant D.H. 1984, Oshima F. 1993, Tisoriere L. 1996, Сторожок Н.М. 1996/. Считают, что синергическая активность ФЛ обусловлена возможностью регенерации активной фенольной формы АО при взаимодействии феноксилов с остатками полиненасыщенных жирных кислот, входящих в структуру ФЛ. При этом азотистое основание полярной головки ФЛ способно разрушать гидропероксиды нерадикальным путём, что приводит к уменьшению роли реакций вырожденного разветвления, способствующих инициированию процесса. /Сторожок Н.М. 1996/.
Было показано, что дополнительное включение ФХ в систему с витаминами Е и D3 приводит к увеличению величины периодов индукции и существенному уменьшению значений начальной и максимальной скоростей окисления. Так, добавки ФЛ в количестве 1,010-3 М по сравнению с действием бинарной смеси увеличивают значения периодов индукции на 60%, а величину начальной и максимальной скоростей окисления в 4,8 и 1,6 раза соответственно. Анализ зависимости изменения эффективности тройной композиции от количества витамина D3 показывает, что во всем изученном диапазоне в действии смеси проявляется эффект синергизма. Концентрационная кривая (рис. 6, кривая 3) располагается в верхнем квадрате, относящемся к области синергизма. Таким образом, введение ФЛ существенно увеличивает окислительную устойчивость системы. Приведенные данные позволяют рекомендовать использовать для увеличения сроков хранения лекарственных препаратов с витамином D3 композиции –ТФ с ФЛ, например яичным лецитином. Найдены оптимальные молярные соотношения компонентов, обеспечивающие наибольшее брутто-ингибирующее действие композиции -ТФ : витамин D3 : ФХ, составившие 0,125 : 0,005 : 1,00 соответственно.
Таблица 2
Кинетические параметры окисления МО в присутствии -ТФ (2,510-4) М (const) и -каротина (1,8910-3) М (const) и их смесей с различными концентрациями фосфатидилхолина, САИБН = 3,010-3 М, Т=333К
| С-ТФ =const = 2,510-4 М, =160 мин, С-кар.=1,8910-3 М, =47 мин. | |||||||
| № п/п | Концентрация ФХ, СФЛ10-3 М | адд, мин | , мин | = – адд, мин | (/ адд) 100% | Начальная скорость окисления WО2 нач 107 Мс-1 | Максималь-ная скорость окисления WО2 макс 107 Мс-1 |
| 1 | 0 | - | - | - | - | 1,5±,002 | 5,2±0,08 |
| 2 | 0,1 | 207 | 150,3 ±2,25 | -56,7 | -27,4 | 1,46±0,02 | 5,1±0,07 |
| 3 | 0,5 | 207 | 174,5 ±2,78 | -32,5 | -15,7 | 1,45±0,02 | 5,1±0,07 |
| 4 | 1,0 | 207 | 190,2 ±3,04 | -16,8 | -8,1 | 1,3±0,01 | 5,0±0,08 |
| 5 | 5,0 | 207 | 220,3 ±3,52 | 13,3 | +6,4 | 0,49±0,007 | 4,9±0,07 |
| 6 | 10,0 | 207 | 236,5 ±3,30 | 29,5 | +14,2 | 0,4±0,006 | 4,5±0,07 |
| 7 | 13,0 | 207 | 282,6 ±4,51 | 75,6 | +36,5 | 0,35±0,005 | 4,2±0,06 |
p0,05
Аналогично было исследовано влияние ФХ на эффективность смеси –ТФ и -каротина (рис. 7, кривая 4). Сравнение между собой действия бинарной смеси –ТФ и -каротина (рис. 7, кривая 3) и тех же количеств биоАО с добавкой ФЛ (рис. 7, кривая 4) показывает, что во всем изученном диапазоне концентраций -каротина эффективность действия тройной смеси выше (в среднем на 15-20 %). Практически полностью кривая 4 располагается в области синергизма, достигающего при определенных соотношениях компонентов 40%. Отмечается закономерное увеличение величины эффекта синергизма с ростом количества ФЛ в смеси (табл. 2).
Приведённые данные показывают, что для более эффективного ингибирования окислительных превращений липидных препаратов, включающих -каротин и -ТФ, целесообразно вводить ФЛ. Молярные соотношения компонентов, обеспечивающие наибольшее ингибирующее действие составляют: -ТФ : -каротин : ФХ, равные 0,25 : 0,0075 : 1,00 соответственно.
Полученные результаты могут найти применение в пищевой технологии, производстве лекарственных и косметических средств, включающих указанные природные соединения.
При окислении МО исследовали ингибирующее действие смесей -каротина и нетоксичного синтетического АО (бис-3-(41–гидрокси-31,51-дитрет.бутилфенил)-пропил сульфида) (СО-3) /Сорокина И.В., 1987/. ЛД50 10000 мг/кг. По своей структуре СО-3 относится к пространственно затрудненным бисфенолам, разделенным мостиковой алкилсульфидной группой (схема 1). Ранее было установлено, что АО проявляет антирадикальную активность (k7 =1,3104 М-1с-1) /Сторожок Н.М., Крысин А.П., 2001/, способен разрушать гидропероксиды без образования свободных радикалов /Гуреева Н.В., 2003/.
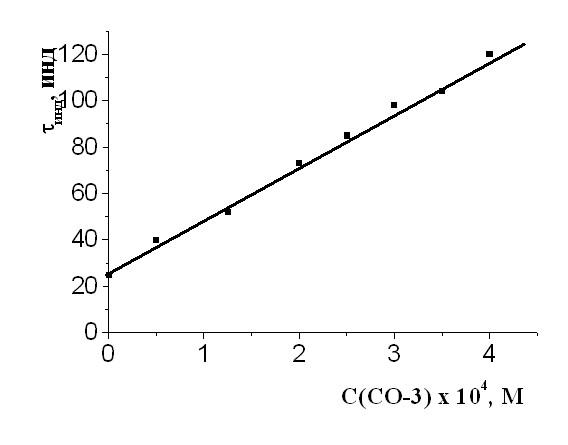 | 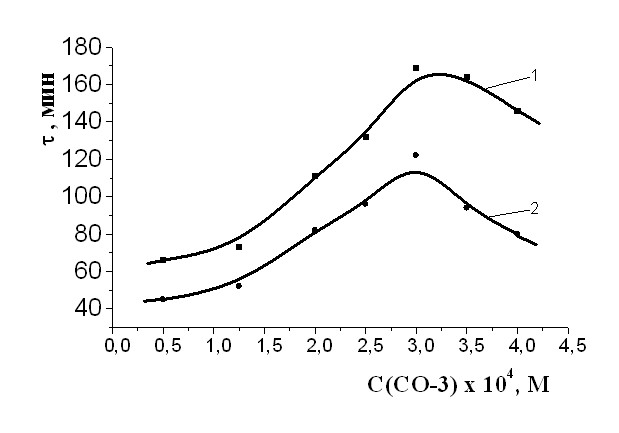 |
| Рис. 15 а Зависимость периодов индукции от концентрации СО-3, САИБН=9,010-3М, Т=333К. | Рис. 15 б Зависимость периодов индукции от концентрации СО-3 при окислении МО в присутствии -каротина, равными: 1 – (2,6510-5) М; 2 - (1,1310-4) М, САИБН=9,010-3М, Т=333К. |
Исследовано ингибирующее действие индивидуального СО-3 и эффективность его бинарных смесей с -каротином. Показано, что в присутствии индивидуального АО зависимость величины периодов индукции от концентрации носит линейный характер (рис. 15 а). Указанная положительная корреляционная связь выполняется для большинства известных синтетических АО.
При изучении действия этого соединения с постоянными добавками -каротина показано, что концентрационные зависимости отклоняются от прямолинейности. На рис. 15 б видно наличие экстремумов на параллельных кривых с разным количеством -каротина. Обращает внимание, что брутто-ингибирующее действие смеси тем выше, чем ниже концентрация -каротина. Полученные результаты свидетельствуют о том, что -каротин образует активные радикалы, которые взаимодействуют не только с субстратом, но и, по всей вероятности, с фенольным АО, приводя к его дополнительному расходованию.
В сравнении с действием индивидуального -каротина периоды торможения для системы, дополнительно включающей ингибитор фенольной природы (СО-3), существенно выше (табл.3).
Таблица 3
Зависимость кинетических параметров инициированного окисления смесей, содержащих -каротин и СО-3 от его концентрации, САИБН=9,010-3 М, Т=333К
| № п/п | Концентрация СО-3, С10-4, М | Период индукции смеси, мин | Начальная скорость окисления, WО2нач107, Мс-1 | ||
| Концентрация -каротина в смеси | Концентрация -каротина в смеси | ||||
| (2,6510 -5), М | (11,310 -5), М | (2,6510-5), М | (11,310-5), М | ||
| 1 | 0,0 | 40,3±0,46 | 18,7±0,2 | 14,9±0,17 | 19,4±0,22 |
| 2 | 0,5 | 66,5±0,75 | 45,5±0,5 | 5,7±0,06 | 4,3±0,05 |
| 3 | 1,25 | 73,1±0,83 | 52,4±0,6 | 4,5±0,05 | 2,9±0,03 |
| 4 | 2,0 | 111,4±1,27 | 82,8±0,9 | 4,4±0,05 | 3,0±0,03 |
| 5 | 2,5 | 132,3±1,51 | 88,3±1,0 | 2,6±0,03 | 2,7±0,03 |
| 6 | 3,0 | 169,5±1,94 | 122,2±1,4 | 2,2±0,02 | 2,4±0,02 |
| 7 | 3,5 | 164,2±1,88 | 84,5±0,9 | 2,7±0,03 | 2,9±0,03 |
| 8 | 4,0 | 146,1±1,67 | 80,5±0,9 | 3,4±0,04 | 3,5±0,04 |
p0,05
Можно видеть, что при различном содержании -каротина в смеси наиболее эффективными являются одни и те же концентрации бисфенола (2,5-3,5)10-4 М (рис. 15б). Указанные концентрации можно рекомендовать для практического использования в целях стабилизации процессов окисления липидных препаратов, содержащих -каротин (лекарств, пищевых добавок, косметических средств).
Работа поддержана грантом РФФИ 02-04-49452 и контрактом Федеральной целевой программы "Содействие интеграции высшего образования и фундаментальной науки" ("Интеграция") И 0566/1653.
ВЫВОДЫ
1. При окислении метилолеата в среде хлорбензола и в мицеллярной системе липид-вода, стабилизированной добавками додецилсульфата натрия, исследовано ингибирующее действие природных пигментов (астаксантина, -каротина) в сравнении с -токоферолом. Установлено, что при разных условиях окисления зависимость ингибирующего действия от концентрации указанных веществ описываются кривыми с экстремумом. Установлены области концентраций, обеспечивающие максимальное ингибирующее действие, составляющие для астаксантина, -каротина, -токоферола (1,5-12,0)10-4М, (0,25-0,75)10-4М, (1,25–3,50)10-3М, соответственно. В мицеллярной системе действие биоантиоксидантов выше, чем в гомогенной среде.
2. Хемилюминесцентным методом изучена антирадикальная активность астаксантина и -каротина. Значение k7 указанных каротиноидов составляет 1,3105 М-1с-1 и 1,4104 М-1с-1, соответственно. Витамин D3 не проявляет антирадикальной активности. Показано, что с увеличением количества - сопряжённых связей в открытой цепи соединений изопреноидного строения, при введении электроноакцепторных заместителей (оксо- и гидроксигрупп) происходит усиление антирадикальной активности и брутто-ингибирующего действия.
3. Установлено, что холекальциферол (витамин D3) не ингибирует процесс окисления, введение его в систему увеличивает скорость инициирования, начальную и максимальную скорости поглощения кислорода, кинетический показатель k2/ k6, характеризующий окисляемость.
4. Изучены кинетические эффекты совместного ингибирующего действия -токоферола с -каротином, астаксантином и витамином D3. При одном и том же количестве -токоферола зависимость изменения эффективности действия смесей от концентрации -каротина или атаксантина описывается U-образной кривой, а для смеси -ТФ - холекальциферол носит линейный характер.
5. Показано, что при разных соотношениях в действии бинарных композиций -токоферола с изопреноидами (-каротином, астаксантином, витамином D3.) возможно проявление аддитивности, эффектов синергизма или антагонизма. Показано, что на фоне проявления эффекта антагонизма происходит существенное увеличение скорости расходования -токоферола при увеличении концентрации витамина D3 и -каротина. Установлено, что при окислении в среде хлорбензола эффект синергизма в совместном действии -токоферола с изопреноидами проявляется при соотношениях с витамином D3, -каротином, превышающих 100:1; 4:1. Для бинарной системы -токоферол : астаксантин – в мицеллярной среде – эффект синергизма констатируется при соотношениях, больших 12:1.
6. Показано, что дополнительное включение фосфолипидов в бинарные системы витамина Е с -каротином или холекальциферолом приводит к увеличению тормозящего действия композиций (до 60%). Найдены оптимальные молярные соотношения компонентов, обеспечивающие наибольшее брутто-ингибирующее действие композиции -токоферол : витамин D3 : фосфатидилхолин, составившие 0,125 : 0,005 : 1,00 соответственно. Для составляющих смеси -токоферол : -каротин : фосфатидилхолин оптимальными являются молярные соотношения 0,25 : 0,0075 : 1,00 соответственно.
7. Предложен способ увеличения эффективности индивидуального -каротина за счет дополнительного введения нового синтетического ингибитора окисления (бис-3-(4/-гидрокси-3/,5/-дитрет.бутил фенил)-пропил сульфид (СО-3) в количестве (2,5-3,5)10-4 М. Добавки синтетического антиоксиданта увеличивают эффективность ингибирования в 3-7 раз.
СПИСОК ПУБЛИКАЦИЙ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Сторожок Н.М. Антиоксидантные свойства аурола/ Н.М. Сторожок, Н.В. Гуреева, Е.Н. Дарюхина и др // Химико-фармацевтический журнал- 2002.-т.36.-№ 2.-с. 14-18.
2. Дарюхина Е.Н. Перспективы стабилизации окисления бета-каротина /Дарюхина Е.Н., Сторожок Н.М. //Медицинская наука и образование Урала. – 2004. – Т.33-34.- №3-4. – С.190-191.
3. Дарюхина Е.Н. Молекулярные механизмы сочетанного действия -токоферола и витамина D3 /Е.Н. Дарюхина, Е.Ю. Парис, Н.М. Сторожок //В сб. материалов международной конференции «Биоантиоксидант». – М. – 2002. – с. 153-155.
4. Дарюхина Е.Н.. Ингибирующие свойства астаксантина /Е.Н. Дарюхина, Н.М. Сторожок // В сб. материалов международной конференции «Биоантиоксидант». – М. – 2002. – с. 155-157.
5. Сторожок Н.М. Изучение неаддитивности в совместном ингибирующем действии -токоферола и -каротина /Н.М. Сторожок, В.Е., Кутузова, Е.Н. Дарюхина //В сб. «Биоантиоксидант». – Тюмень. - 1997. – с.34.
6. Сторожок Н.М.. Сравнение антиоксидантных свойств природных жирорастворимых витаминов /Н.М. Сторожок, Е.Н. Дарюхина // В сб. материалов международного симпозиума «Медицина и охрана здоровья». – Тюмень. – 1999. – с. 160.
7. Дарюхина Е.Н. Молекулярные механизмы сочетанного применения -токоферола и витамина D3 /Е.Н. Дарюхина, Е.Ю. Парис, Б.А. Бердичевский, Н.М. Сторожок // В сб. материалов международного симпозиума «Медицина и охрана здоровья». – Тюмень. – 2000. – с.41.
8. Дарюхина Е.Н. Биоантиоксиданты изопреноидного строения /Е.Н. Дарюхина // В сб. материалов международного симпозиума «Медицина и охрана здоровья». – Тюмень. – 2001. –с.71.
9. Дарюхина Е.Н. Совместное антиоксидантное действие астаксантина и -токоферола /Е.Н. Дарюхина // В сб. материалов международного симпозиума «Медицина и охрана здоровья». – Тюмень. – 2001. –с.71-72.
10. Дарюхина Е.Н. Закономерности расходования -токоферола в присутствии витамина D3 /Е.Н. Дарюхина // В сб. материалов международного симпозиума «Медицина и охрана здоровья». – Тюмень. – 2002. – с. 86.
11. Сторожок Н.М. Особенности расходования альфа-токоферола в присутствии бета-каротина /Н.М., Сторожок, В.Е. Борисенко, Е.Н. Дарюхина и др. // В сб. материалов III международного симпозиума «Биологически активные добавки – нутрицевтики и их использование с профилактической и лечебной целью при наиболее распространённых заболеваниях». – Тюмень. – 1997. - с. 103-104.
12. Сторожок Н.М. Модификация молекулярной структуры и уровня гидропероксидов под воздействием токоферола и фосфолипидов /Н.М. Сторожок, В.М. Игнатова, Е.Н. Дарюхина и др. // В сб. материалов Х Международной конференции «Химия органических и элементорганических пероксидов». – М. – 1998. – с.30.
13. Гуреева Н.В. О взаимосвязи строения и активности природных и синтетических антиоксидантов /Н.В. Гуреева, Е.Н. Дарюхина, А.П. Крысин и др. // В сб. материалов международной конференции «Свободнорадикальные процессы: фармакологические, клинические, биологические аспекты». – С.-Пб. – 1999. – с. 814-815.
14. Сторожок Н.М. Особенности антиоксидантного действия природных антиоксидантов /Н.М. Сторожок, Е.Н. Дарюхина // В сб. Западно-Сибирского терапевтического форума «Актуальные вопросы диагностики, лечения, профилактики наиболее распространённых заболеваний внутренних органов» - Тюмень. – 2000. –с. 114.
15. Дарюхина Е.Н. Кинетическое обоснование стабилизации окисления липидов с применением -каротина, -токоферола и синтетического антиоксиданта СО-3 /Е.Н. Дарюхина, Н.В. Гуреева // В сб. Материалы XXXV юбилейной межвузовской научной конференции «Актуальные проблемы теоретической, экспериментальной и клинической медицины». – Тюмень. – 2001. – с. 47-49.
16. Дарюхина Е.Н. Эффекты совместного ингибирующего действия -токоферола и -каротина /Е.Н. Дарюхина // В сб. Материалы XXXV юбилейной межвузовской научной конференции «Актуальные проблемы теоретической, экспериментальной и клинической медицины». – Тюмень. – 2001. – с. 49-51.
17. Дарюхина Е.Н. Сравнительное изучение антиоксидантных свойств астаксантина и -каротина /Е.Н. Дарюхина // В сб. Материалы XXXVI Всероссийской научной конференции «Актуальные проблемы теоретической, экспериментальной и клинической медицины». – Тюмень. – 2002. – с. 88-89.
18. Дарюхина Е.Н. Кинетические особенности окисления липидов в присутствии астаксантина /Е.Н. Дарюхина // В сб. Материалы XXXVII Всероссийской научной конференции «Актуальные проблемы теоретической, экспериментальной и клинической медицины». – Тюмень. – 2003. – с. 61.
19. Дарюхина Е.Н. Изучение механизма действия витамина D3 в процессе окисления модельных систем и липидов плазмы крови /Е.Н. Дарюхина, Е.Ю. Цветкова // В сб. Материалы XXXVIII Всероссийской научной конференции «Актуальные проблемы теоретической, экспериментальной и клинической медицины». – Тюмень. – 2004. – с. 81-82.
20. Сторожок Н.М. Межмолекулярные взаимодействия витамина D3 с -токоферолом и фосфолипидами /Н.М. Сторожок, Е.Н. Дарюхина, Е.Ю. Цветкова // В сб. «Биоантиоксиданты». Научный вестник мед. акад. – Тюмень. – 2003. – с.36-43.
21. Дарюхина Е.Н., Сторожок Н.М. К вопросу о механизме антиоксидантного действия астаксантина /Е.Н. Дарюхин, Н.М. Сторожок // В сб. статей IV конгресса молодых учёных «Науки о человеке». – Томск. – 2003. – с.150-151.

