Компьютерная система поддержки принятия решения при диагностике острых лучевых поражений человека
На правах рукописи
ХАМИДУЛИН ТИМУР МАРАТОВИЧ
Компьютерная система поддержки принятия решения при диагностике острых лучевых поражений человека
03.01.01 – Радиобиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата биологических наук
Москва – 2011
Работа выполнена в ФГУ Федеральный медицинский биофизический центр им. А.И.Бурназяна ФМБА России (г. Москва)
Научный руководитель:
доктор биологических наук Соловьев Владимир Юрьевич
Официальные оппоненты:
доктор медицинских наук, Калистратова Валентина Сергеевна
профессор
доктор биологических наук Кипор Геннадий Викторович
профессор
Ведущая организация:
Уральский научно-практический центр радиационной медицины ФМБА России (г. Челябинск)
Защита состоится 13 октября 2011 г. в 10.00 на заседании диссертационного совета Д 462.001.01 при ФГУ Федеральный медицинский биофизический центр им. А.И.Бурназяна ФМБА России (123182, г. Москва, ул. Живописная, 46)
С диссертацией можно ознакомиться в библиотеке ФМБЦ им. А.И.Бурназяна
Автореферат разослан „ ” июля 2011 г.
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор Н.К.Шандала
Список сокращений
ОЛБ – Острая лучевая болезнь
ФМБА – Федеральное медико-биологическое агентство
ФМБЦ им. А.И.Бурназяна ФМБА России – Федеральное государственное учреждение Федеральный медицинский биофизический центр им. А.И.Бурназяна ФМБА России
ЧАЭС – Чернобыльская атомная электростанция
ICRP – International Committee on Radiation Protection
MCNP - Monte Carlo N-Particle Transport Code
MS - Microsoft Corporation
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Опыт диагностики и лечения острых лучевых поражений человека накопленный в ФМБЦ им. А.И.Бурназяна ФМБА России является уникальным. По оценкам экспертов это более половины мирового опыта по острым лучевым поражениям человека. В том числе совершенно уникальная ситуация имела место при диагностике и лечении пострадавших при широкомасштабной радиационной аварии на ЧАЭС 1986 г. Такая уникальная информация сохранена, в том числе и в виде базы данных компьютеризированных историй болезни.
Учитывая, что в будущем нельзя исключить радиационные инциденты как техногенного происхождения, так и с участием т.н. «человеческого фактора», задача обобщения предшествующего опыта и дополнения его с использованием новых технологий является весьма актуальной.
Целью исследования является создание информационного ресурса для поддержки принятия решения при диагностике острых лучевых поражений человека.
Задачи исследования:
- Разработка пользовательского интерфейса к базе данных по острым лучевым поражениям человека, работающего в режиме многопользовательского удаленного доступа, с включением элементов анализа имеющейся информации.
- Разработка метода прогноза последствий острого радиационного поражения при неравномерном аварийном облучении с использованием воксел-фантомной технологии.
- Апробация метода путем ретроспективного анализа реальных случаев неравномерного облучения
- Исследование прогностической ценности гематологических критериев оценки степени тяжести острых лучевых поражений человека.
Научная новизна диссертационной работы
В данной работе впервые создана распределенная база данных по острым лучевым поражениям человека с использованием интернет-совместимых технологий и на ее основе построена система поддержки принятия решения при диагностике и лечении острых лучевых поражений.
Разработан и реализован алгоритм расчета распределения доз по телу человека при крайне неравномерном аварийном облучении с использованием воксел-фантома ICRP стандартного человека и прогноза течения острого периода лучевой болезни.
На основе созданной системы исследована прогностическая ценность гематологических критериев прогноза степени тяжести лучевого поражения с учетом неопределенностей, присущих данным критериям.
Научно-практическая значимость диссертационной работы
В результате выполненного исследования уточнены критерии диагностики степени тяжести острых лучевых поражений человека при равномерном и неравномерном по телу облучении. Разработана методика количественного расчета распределения дозы по телу при неравномерном аварийном облучении на основании использования ICRP-фантома стандартного человека и осуществления на основании подобного расчета прогноза течения острого периода лучевой болезни. Разработан пользовательский интерфейс к базе данных по острым лучевым поражениям человека и на его основе создана система поддержки принятия решения при диагностике и лечении острых лучевых поражений человека. База данных получила свидетельство о Государственной регистрации, №2010620390 от 23.07.2010.
Положения и результаты, выносимые на защиту:
- Система поддержки принятия решения при диагностике и лечении острых лучевых поражений человека
- Метод прогноза течения острого лучевого поражения при крайне неравномерном аварийном облучении с использованием расчетной воксел-фантомной технологии
- Уточненные гематологические критерии оценки степени тяжести лучевого поражения
Внедрение результатов исследования
Результаты исследований внедрены в клиническую практику ФМБЦ им. А.И. Бурназяна ФМБА России.
Апробация работы
Результаты проведенного диссертационного исследования доложены и обсуждены на научной конференции отдела № 2 ФГУ «Федеральный медицинский биофизический центр им. А.И. Бурназяна ФМБА России» 30 марта 2011г, протокол № 4.
По материалам диссертационной работы опубликовано 5 научных работ в рекомендованных ВАК изданиях и получено 1 авторское свидетельство.
Структура и объем диссертации
Диссертационная работа изложена на 113 страницах, иллюстрирована 29 рисунками, 6 таблицами, состоит из введения, 3 разделов, выводов, списка литературы, содержащего 87 источников (43 на русском и 44 на английском языке), 2 приложения.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Материал и методы
К началу работы над проблемой был создан информационный массив компьютеризированных историй болезни пострадавших в радиационных авариях в виде базы данных, функционирующей на персональном компьютере. Это давало возможность оперативного использования имеющейся информации, ее дополнения и коррекции только на одном рабочем месте.
Одной из первых задач являлась подготовка и преобразование базы данных для удаленной и одновременной работы с ней множества пользователей, с применением интернет-совместимых технологий. Общая схема функционирования такой системы приведена на рисунке 1 [2].


Рисунок 1 - Организация работы с базой данных по острым лучевым поражениям человека на основе технологии «клиент-сервер» [2].
К данной системе автором был реализован дружественный пользователю интерфейс, позволяющий легко осуществлять поиск информации по базе данных по любым сложным запросам, осуществлять ввод и коррекцию информации одновременно несколькими пользователями, а также в автономном режиме дополнение существующих списков регистрируемых параметров, характеризующих состояние пациента [2]. Кроме того, реализована возможность экспорта информации в стандартных форматах MS Excel и графических форматах для дальнейшей обработки и использования в публикациях.
База данных по острым лучевым поражениям человека ФМБЦ им. А.И.Бурназяна содержит информацию с 357 историями болезни случаев облучения пострадавших в радиационных авариях (из общего количества 757). В частности, в базе данных содержится информация по пострадавшим в наиболее тяжелой по последтвиям радиационной аварии на ЧАЭС 1986 г. Среди 134 человек с диагнозом ОЛБ было зафиксировано: 21 случай ОЛБ IV степени тяжести, 22 случая III степени тяжести, 50 случаев II степени тяжести и 41 случай ОЛБ I степени.
Данные сведения являются уникальными по своей информативности и включают в себя ежедневные результаты лабораторных анализов (гематологических, биохимических, иммунологических, физиологических и др.). Кроме этого имеются сведения о лучевых поражениях кожи и подлежащих тканей, данные о примененных лекарствах и других терапевтических мероприятиях а также другие клинико-лабораторные данные.
Всего в базе данных имеются полные сведения из историй болезни 198 пациентов. Общее количество записей только данных лабораторных анализов – около 450 тыс.
По завершении работы над созданием компьютерной системы, было проведено несколько этапов исследования.
В клинической практике ФМБЦ им. А.И.Бурназяна используются несколько диагностических критериев для оценки степени тяжести лучевого поражения, общая схема практического использования которых представлена на рисунке 2 [2].

Рисунок 2 - Общая схема использования основных диагностических критериев для оценки степени тяжести лучевого поражения [2].
Согласно схеме на рисунке 2 отдельные показатели периферической крови (лимфоциты, тромбоциты) могут наряду с другими сведениями, используемыми в биологической дозиметрии, дать информацию о степени тяжести лучевого поражения.
В работе А.Е.Баранова приводятся сведения об ошибке индивидуальной оценки дозы по гематологическим тестам, в среднем по всему дозовому диапазону.
Первый этап исследования был посвящен более подробному анализу прогностической ценности гематологических критериев, по данным лабораторных анализов пострадавших при радиационной аварии на ЧАЭС. Доза облучения определялась по среднему числу дицентриков в культуре лимфоцитов периферической крови и была скорректирована по результатам использования верифицированной методики В.Ю. Нугисом [4]. Значение уровня лимфоцитов периферической крови в соответствии с выбранным критерием оценено с погрешностью, учитываемой при использовании метода счета числа клеток лейкоцитарного ряда. При оценке предполагалось, что распределение сосчитанного числа клеток подчиняется закону Пуассона со всеми вытекающими из этого зависимостями.
Статистическая обработка данных производилась методом наименьших квадратов. В качестве результирующей зависимости принималось экпоненциальная функция для лимфоцитов периферической крови и кусочно-непрерывная функция, состоящая из трех участков для критерия «день 500 нейтрофилов».
В то время, как прогноз течения ОЛБ для относительно равномерного облучения не вызывает значимых затруднений, наибольшие сложности в клинической практике вызывает прогнозирование последствий неравномерного по телу облучения.
В соответствии с методом, предложенном А.Е.Барановым и апробированном в работах (Baranov A.E. еt.аl., 1979; Соловьев В.Ю. и др., 1991), пострадиационная динамика концентрации нейтрофилов в периферической крови при неравномерном по телу облучении определяется путем парциального «взвешивания» долей костного мозга, облученного в дозовых интервалах {Dmin, Dmax}, средней точке которых соответствует каждая из эмпирических дозовых кривых на рисунке 9.
Единственным, требующим решения вопросом, оставался расчет распределения доз для реальных случаев аварийного облучения. Трудность решения данного вопроса заключалась в трудоемкости проведения фантомных расчетов. С появлением воксел-фантомных технологий решение данной задачи оказалось возможным.
Воксел-фантомная технология предполагает использование трех этапов: снятие компьютерной томограммы конкретного человека, создание компьютерного воксел-фантомного образа исследуемого пациента и расчет с использованием сведений о геометрии облучения и программ расчета переноса излучения в среде, использующих метод Монте-Карло. В то же время, требуемая для практики точность позволяет в ряде случаев пренебречь различием в ряде параметров конкретного пострадавшего и т.н. «стандартного» человека. Это дает возможность для подобных оценок использовать унифицированные воксел-фантомы. Таковыми, в частности, являются стандартные воксел-фантомы мужчины и женщины ICRP, конструируемые исходя из национальных особенностей телосложения.
Если рассматривать функционирование костномозгового кроветворения в мозаичном приближении, когда каждый участок (сайт) костного мозга восстанавливается автономно после гибели части стволовых клеток в результате радиационного поражения, то нам необходимо оценить динамические характеристики производства форменных элементов периферической крови (нейтрофилов) в каждом участке костного мозга для различных значений поглощенной дозы, т.е. функцию N(t, Diкм), соотношение (1).
| (1) |
где N(t,Diкм), 1/л - усредненное значение концентрации нейтрофилов в периферической крови человека при равномерном облучении всех участков костного мозга в дозе Diкм, Гр; f(Diкм) – доля костного мозга, облученного в дозе Diкм; t – время (дни после облучения); N(t) – концентрация нейтрофилов в периферической крови, 1/л; суммирование ведется по всем n дозовым интервалам.
Метод интуитивно совершенно прозрачный: каждый участок костномозгового кроветворения вырабатывает форменные элементы крови, которые потом перемешиваются в кровеносном русле. Если мы «знаем» по какому закону каждый такой участок производит продукцию, то процесс перемешивания в кровеносном русле мы чисто технически можем заменить суммированием. А динамика ответа на разный уровень поражения (в дозовой шкале) в значительной мере воспроизводится ситуацией, когда все участки костного мозга поражены одинаковой дозой. В какой-то степени такая ситуация наиболее близко реализуется при относительно равномерном облучении. Однако, вследствие определенного экранирования телом костный мозг получает, в среднем, несколько меньшую дозу, чем она может быть зафиксирована «в отсутствие фантома». Кроме того, имеет место определенная неравномерность облучения костного мозга. Для корректного решения задачи необходимо определенное модельное приближение.
Облучение пострадавших в результате радиационной аварии на ЧАЭС происходило, в основном, от выпавших на поверхность земли радиоактивных продуктов или от радиоактивных аэрозолей окружающего воздуха. Используя этот факт, мы попытались оценить функцию N(t,Diкм), связав результаты расчетов двух модельных случаев и эмпирические дозовые кривые, полученные в результате усреднения данных по всем пострадавшим при аварии на ЧАЭС (Кончаловский М.В. и др, 1991).
В первом случае моделируется относительно равномерное облучение «стандартного» человека в поле радиоактивных выпадений на местности со спектром излучения, близком к оцененному в первый день радиационной аварии на ЧАЭС 1986 г. (Алексахин Р.М. и др., 2001), а во втором – в поле радиоактивных аэрозолей воздуха. По результатам расчета была оценена функция N(t,Diкм) (1), используя эмпирические дозовые кривые нейтрофилов для пострадавших при аварии на ЧАЭС (Кончаловский М.В. и др, 1991).
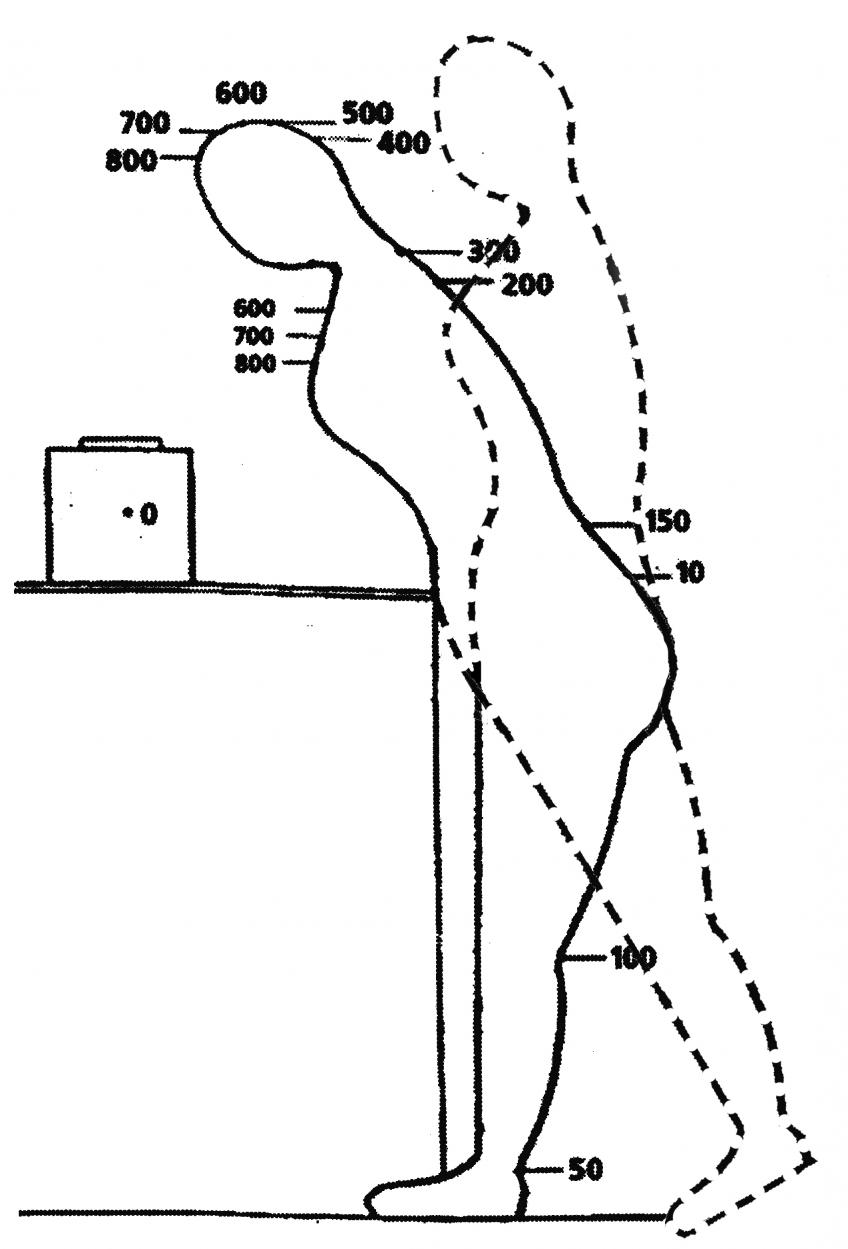
Для проверки работоспособности метода нами выполнен расчет распределения костного мозга по дозе для двух пострадавших в реальных случаях: пострадавшей Г. (Гуськова А.К., Байсоголов Д.Г., 1971; Ильин Л.А. и др., 2001) в результате инцидента с источником 60Co, имевшего место в 1961 г., пациент №3041 [2], рисунок 3а, и одного из пострадавших в инциденте 1982 г. (Barabanova A.V., 2001), когда военнослужащие по очереди носили в кармане плаща-накидки некий предмет, который впоследствии оказался источником 137Cs, пациент №3003 [2], рисунок 3б. С помощью полученной функции N(t,Diкм), см. выражение (1), был произведен расчет динамики концентрации нейтрофилов в периферической крови этих пострадавших.
![]()
(а) (б)
Рисунок 3 - а) Положение тела пострадавшей Г. в результате радиационного инцидента и схема преобразования геометрии для проведения воксел-фантомных расчетов (пунктирное выделение), переработано из (Гуськова А.К., Байсоголов Д.Г., 1971); б) Геометрия облучения пострадавшего Н., когда источник излучения (черный кружок) находится вблизи тела пострадавшего (Barabanova A.V., 2001).
На втором этапе исследования нами использовались воксел-фантомы стандартного человека ICRP из Публикации ICRP № 110, 2009. В качестве расчетной программы использовался комплекс MCNP5 версии 1.30. Т.к. формат представления данных фантома в приложении к Публикации не подходит для использования в MCNP, была написана специальная программа-конвертор на языке программирования C++. Воксел-фантом ICRP состоит из около 14 млн ячеек (вокселов), моделирующих органы и ткани человека. Каждая ячейка костной ткани имеет дополнительную информацию о доле содержащегося в ней красного костного мозга. Поглощенная доза на костный мозг рассчитывалась как «доза в костной ткани, содержащей костный мозг». При расчете распределения костного мозга по дозам облучения учитывалась доля содержания костного мозга в конкретной расчетной ячейке. Для контроля расчетов и преобразования информации из цифровой в графическую была написана специальная программа на языке C++.
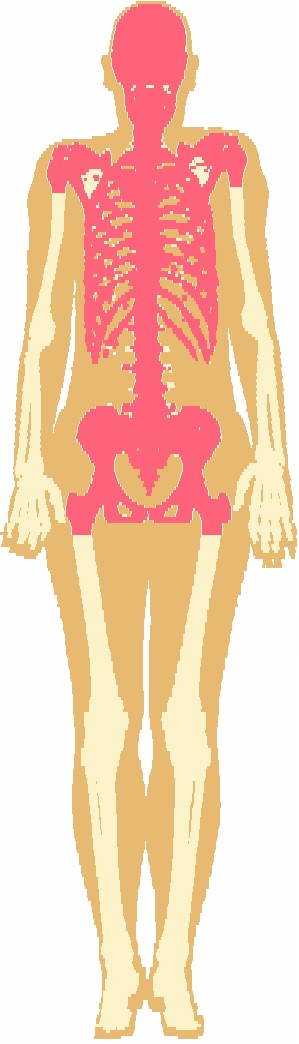 |
| Рисунок 4 - Образ стандартного воксел-фантома ICRP (женщина, сечение) с выделением области костной ткани, содержащей красный костный мозг. |
На рисунке 4 представлено обработанное изображение стандартного воксел-фантома ICRP женщины [3]. Расположение костной ткани, содержащей костный мозг, выделено на разрезе темно-серым цветом.
Результаты и обсуждение
На первом этапе было выполнено исследование по оценке прогностической ценности используемых критериев.
На рисунках 5-7 представлены результаты анализа для исследуемых гематологических тестов, предложенных в работе (A.E.Баранов, 1974). На всех рисунках в единообразном виде в координатах «значение параметра – доза облучения» представлены фактические данные по всем пациентам из рассматриваемой когорты в соответствии с данными, опубликованными в работе [4].
Для каждого гематологического теста оценены границы неопределенности результата с 66%-й доверительной вероятностью (пунктирные границы на графике). Полученные результаты являются более информативными для принятия решения при диагностике степени тяжести лучевого поражения кроветворной ткани.

(а) (б)


(в) (г)
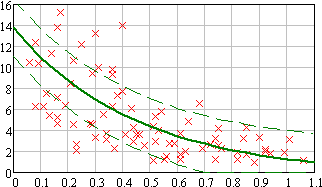
Рисунок 5 - Результаты анализа для лимфоцитарного теста 2-й (а), 3-й (б), 4-й (в) и 6-й (г) дни после облучения. Обозначения: x – фактические данные, усредненое значение соответствующего теста [4]. Ось абсцисс – уровень лимфоцитов, 109/л; ось ординат – доза, Гр.
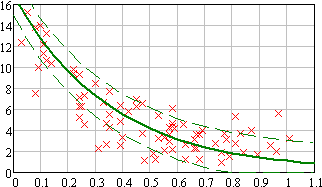
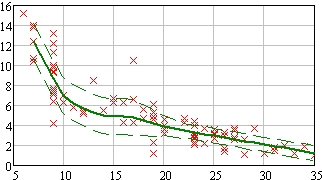
| Рисунок 6 - Результаты анализа для лимфоцитарного теста “среднее значение за 3-7-й дни” Обозначения: x – фактические данные, усредненое значение соответствующего теста [4]. Ось абсцисс – уровень лимфоцитов, 109/л; ось ординат – доза, Гр. | Рисунок 7 - Результаты анализа для теста “день 500 нейтрофилов”. Обозначения: x – фактические данные, усредненое значение соответствующего теста [4]. Ось абсцисс – уровень лимфоцитов, 109/л; ось ординат – доза, Гр. |
Из рассмотренного набора лимфоцитарных тестов наименьшую дисперсию и соответственно наибольшую информационную ценность имеет тест «среднее значение концентрации лимфоцитов за 3-6 дни после облучения».
Рассматривая наиболее информативный лимфоцитарный тест «среднее значение концентрации лимфоцитов за 3-6 дни после облучения» из полученных закономерностей можно сделать следующие выводы.
Если уровень лимфоцитов на указанное критериальное время (средний за 3-6 сутки) не выходит за пределы нормы (>1.2109/л), полученная доза равномерного облучения составляет не более 2 Гр. Уровню лимфоцитов 1.0-1.2109/л соответствует полученная доза равномерного облучения не более 3 Гр. Уровню 0.3-0.6109/л соответствует диапазон доз облучения 2-6 Гр. И, наконец, снижение уровня лимфоцитов до величины менее <0.2109/л соответствует дозе облучения более 6 Гр. Более точные оценки приведены в таблице 2 [4].
Таблица 2 - Оценка средней дозы облучения костного мозга по лимфоцитарному тесту, Гр
| Уровень лимфо-цитов, 109/л | Оценка дозы (Гр) с 66%-м ДИ на критериальное время | ||||
| 2-й день | 3-й день | 4-й день | 3-6-й дни среднее | 4-8-й дни среднее | |
| 0.05 | 12.3 (9.6 - 13.0) | 11.0 (8.7 - 13.3) | 13.4 (11.1 - 15.8) | 14.7 (12.7 - 16.6) | 14.7 (12.7 - 16.6) |
| 0.10 | 11.0 (8.3 - 12.0) | 9.7 (7.4 - 12.0) | 11.6 (9.3 - 14.0) | 12.8 (10.8 - 14.7) | 12.8 (10.8 - 14.7) |
| 0.15 | 9.8 (7.1 - 11.1) | 8.6 (6.3 - 10.9) | 10.1 (7.8 - 12.5) | 11.1 (9.1 - 13.0) | 11.1 (9.1 - 13.0) |
| 0.20 | 8.8 (6.1 - 10.3) | 7.6 (5.3 - 9.9) | 8.8 (6.5 - 11.1) | 9.6 (7.7 - 11.6) | 9.6 (7.7 - 11.6) |
| 0.25 | 7.8 (5.1 - 9.7) | 6.7 (4.5 - 9.0) | 7.6 (5.3 - 10.0) | 8.4 (6.5 - 10.3) | 8.4 (6.4 - 10.3) |
| 0.30 | 7.0 (4.3 - 9.0) | 6.0 (3.7 - 8.2) | 6.7 (4.3 - 9.0) | 7.3 (5.4 - 9.2) | 7.3 (5.4 - 9.2) |
| 0.40 | 5.5 (2.9 - 7.9) | 4.7 (2.4 - 7.0) | 5.1 (2.8 - 7.4) | 5.5 (3.6 - 7.5) | 5.5 (3.6 - 7.5) |
| 0.50 | 4.4 (1.7 - 7.0) | 3.7 (1.4 - 6.0) | 3.9 (1.6 - 6.2) | 4.2 (2.3 - 6.1) | 4.2 (2.3 - 6.1) |
| 0.60 | 3.5 (0.8 - 6.3) | 2.9 (0.7 - 5.2) | 3.0 (0.7 - 5.3) | 3.2 (1.3 - 5.1) | 3.2 (1.3 - 5.1) |
| 0.70 | 2.7 (0.0 - 5.6) | 2.4 (0.1 - 4.7) | 2.3 (0.0 - 4.7) | 2.4 (0.5 - 4.4) | 2.4 (0.5 - 4.4) |
| 0.80 | 2.1 (0.0 - 5.1) | 1.9 (0.0 - 4.2) | 1.8 (0.0 - 4.2) | 1.9 (0.0 - 3.8) | 1.9 (0.0 - 3.8) |
| 0.90 | 1.7 (0.0 - 4.7) | 1.6 (0.0 - 3.9) | 1.5 (0.0 - 3.8) | 1.4 (0.0 - 3.4) | 1.4 (0.0 - 3.4) |
| 1.00 | 1.3 (0.0 - 4.4) | 1.3 (0.0 - 3.7) | 1.2 (0.0 - 3.6) | 1.1 (0.0 - 3.1) | 1.1 (0.0 - 3.1) |
| 1.10 | 1.0 (0.0 - 4.1) | 1.1 (0.0 - 3.5) | 1.0 (0.0 - 3.4) | 0.9 (0.0 - 2.8) | 0.9 (0.0 - 2.8) |
Диагностический критерий D500 («день 500 нейтрофилов») имеет следующие прогностические свойства. Если D500 превышает 30 суток, то полученная доза с вероятностью 66% не более 1.5 Гр. Если D500 находится в пределах 25-30 суток, оценка дозы – не более 3 Гр, 20-25 сутки – не более 4 Гр, 10-20 сутки - от 3 до 6 Гр, и, наконец, если D500 менее 10 дней, то доза облучения превышает 6 Гр, а прогноз течения и исхода ОЛБ крайне неблагоприятный. Более точные значения оценки дозы по данному критерию приведены в таблице 3 [4].
Таблица 3 - Оценка средней дозы облучения костного мозга по «дню 500 нейтрофилов»
| D500 | Доза, Гр | D500 | Доза, Гр |
| 7 | 12.4 (10.6 - 14.2) | 23 | 3.3 (2.6 - 4.0) |
| 9 | 8.7 (6.9 - 10.5) | 24 | 3.1 (2.4 - 3.9) |
| 10 | 7.0 (5.2 - 8.8) | 25 | 3.0 (2.2 - 3.7) |
| 11 | 6.2 (4.4 - 8.0) | 26 | 2.8 (2.1 - 3.5) |
| 12 | 5.7 (3.9 - 7.5) | 27 | 2.6 (1.9 - 3.4) |
| 13 | 5.3 (3.5 - 7.1) | 28 | 2.4 (1.7 - 3.2) |
| 14 | 5.0 (3.2 - 6.8) | 29 | 2.3 (1.5 - 3.0) |
| 15 | 4.9 (3.1 - 6.7) | 30 | 2.1 (1.4 - 2.8) |
| 16 | 4.9 (3.1 - 6.7) | 31 | 1.9 (1.2 - 2.7) |
| 17 | 4.8 (3.0 - 6.6) | 32 | 1.8 (1.0 - 2.5) |
| 18 | 4.5 (3.0 - 6.0) | 33 | 1.6 (0.8 - 2.3) |
| 19 | 4.2 (2.9 - 5.5) | 34 | 1.4 (0.6 - 2.2) |
| 20 | 3.9 (3.0 - 4.9) | 35 | 1.2 (0.5 - 2.0) |
| 22 | 3.5 (2.7 - 4.2) | - | - |
На втором этапе исследования была использована воксел-фантомная технология расчетов, адаптированная к задачам аварийной дозиметрии. Распределение костного мозга по дозе для всех случаев приведено на рисунке 8.

Рисунок 8 - Распределение дозы по костному мозгу стандартного человека (воксел-фантом ICRP) в случае его расположения в поле гамма-излучения радиоактивных выпадений на поверхности земли (а) и в воздухе газо-аэрозольного выброса (б) смеси радиоактивных продуктов, характерной для первого дня аварии на ЧАЭС 1986 г. и для пострадавшей Г. (в), см. рисунок 3а, и Н. (г), см. рисунок 3б.
Из имеющегося набора исходных данных – расчета распределения дозы по костному мозгу пострадавших при аварии на ЧАЭС и эмпирических дозовых кривых концентрации нейтрофилов периферической крови точное значение функции N(t,Diкм) получить невозможно. Нами введено упрощение. Функция N(t,Diкм) далее принималась условно «сдвинутой» по дозовой шкале относительно эмпирических дозовых кривых для внешнего облучения, т.е доза бралась в k раз меньше в соответствии с отношением дозы в воздухе к рассчитанному медианному значению распределения костного мозга по дозе для случая 2.

Рисунок 9 - Пострадиационная динамика концентрации нейтрофилов в периферической крови человека для различных значений доз внешнего относительно равномерного по телу облучения (эмпирические дозовые кривые), построенные по материалам клинических наблюдений за пострадавшими при аварии на ЧАЭС (Кончаловский М.В. и др, 1991)
Т.е. фактически, в соотношении (1) мы условно заменяем -функцией распределение дозы по костному мозгу f(Diкм) с последующим ее сдвигом и, соответственно приходим к выражению
| (2) |
где N(t,Dвнеш) - усредненное значение концентрации нейтрофилов в периферической крови человека при равномерном облучении в дозе Dвнеш, Гр, внешнего облучения (рис. 10), k=1,75; Dкм – доза на костный мозг, Гр.
Оцененные значения функции N(t,Dкм) при различных дозах на костный мозг приведены на рисунке 10.

Рисунок 10 - Пострадиационная динамика концентрации нейтрофилов в периферической крови человека для различных значений доз, одинаковыми для всех участков костного мозга, рассчитано из [3].
На рисунке 11 дается сравнение вычисленной указанным выше способом пострадиационной динамики концентрации нейтрофилов периферической крови пострадавшей Г. с фактически измеренными значениями из базы данных по острым лучевым поражениям человека для данного случая [2]. Незначительные расхождения могут быть обусловлены как точностью самого метода, так и дополнительными погрешностями, связанными с неточностью восстановления геометрии тела пострадавшей, оценкой времени контакта с источником и использованием стандартизованного фантома вместо реального воксел-фантомного образа. В целом, удовлетворительная сходимость вычисленных значений с фактическими данными подтверждает работоспособность метода.

Рисунок 11 - Пострадиационная динамика концентрации нейтрофилов в периферической крови пострадавшей Г. () [2] и прогноз по изложенному алгоритму (+) из вычисленного распределения дозы по костному мозгу с использованием воксел-фантомных расчетов (см. рис. 3, 9)
В случае крайне неравномерного по телу облучения (пострадавший Н., пациент №3003 [2]) соответствующая оцененная и реальная пострадиационная динамика концентрации нейтрофилов периферической крови представлена на рисунке 12. Из рисунка отчетливо видно, что в этом случае минимальный уровень концентрации нейтрофилов в периферической крови в области т.н. «вторичного опустошения» находится значительно выше соответствующего уровня для тех же временных точек при равномерном облучении. Подобная форма динамической кривой является характерным признаком высокой неравномерности облучения отдельных участков костного мозга.
Данный факт является дополнительным подтверждением высказанной ранее гипотезы (Соловьев В.Ю. и др, 1991) о мозаичной структуре функционирования системы костномозгового кроветворения у человека. Ранее имело место альтернативное мнение (Bond V.P., Fliedner T.M., Archanbeau J.O., 1971), что выживаемость организма животных (и человека) определяется долей выживших стволовых клеток костного мозга.
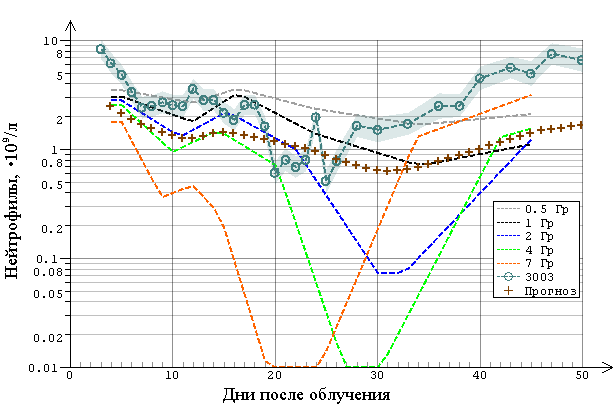
Рисунок 12 - Пострадиационная динамика концентрации нейтрофилов в периферической крови пострадавшего Н. (пациент №3003) [2] и прогноз по изложенному алгоритму (+) из вычисленного распределения дозы по костному мозгу с использованием воксел-фантомных расчетов (пунктирными линиями обозначены эмпирические дозовые кривые для случаев равномерного по телу облучения (Кончаловский М.В. и др, 1991) )
Согласно такой модели «любое неравномерное облучение можно свести к равномерному» путем расчета доли выживших стволовых клеток костного мозга при неравномерном облучении и перехода к ситуации равномерного облучения с той же долей выживших клеток. При этом в случае неравномерного облучения мы видели бы картину динамики концентрации нейтрофилов периферической крови, совпадающей с одной из «стандартных» дозовых кривых для равномерного облучения (рисунок 9). В то же время, на практике это не так, что иллюстрирует рисунок 12.
Это как раз связано с тем, что только часть костного мозга продуцирует форменные элементы крови, соответствующие определенному уровню опустошения в результате облучения. А так как кривые пострадиационной динамики для разных доз облучения имеют смещение по временной шкале, то как раз и имеет место наблюдаемый эффект после перемешивания продуцентов всех локальных участков костномозгового кроветворения. Другими словами, если рассматривать два альтернативных механизма: миграцию стволовых клеток из локальных участков с меньшим уровнем опустошения костного мозга к соответствующим участкам с большим уровнем опустошения и механизм локального независимого восстановления, то можно констатировать, что в диапазоне доз до 6 Гр преобладает второй механизм, что, в свою очередь, указывает на мозаичную структуру функционирования костномозгового кроветворения. Однако, в случае полного опустошения части сайтов костномозгового кроветворения, очевидно, что включается первый механизм – миграции стволовых клеток и их закрепление в опустошенных участках, с последующей наработкой рабочего уровня стволового пула. В этом случае использование предложенного метода является некорректным. Однако, как правило, при сильно неравномерном по телу облучении поражение системы кроветворения не является наиболее критичным событием и на первый план могут выходить поражения отдельных жизненно важных органов, а предложенный метод использования воксел-фантомной технологии также позволяет оценить распределение дозовых нагрузок на критические органы.
В результате проделанной работы отработан алгоритм последовательного расчета распределения дозы облучения по костному мозгу пострадавшего в результате неравномерного облучения в радиационном инциденте с помощью воксел-фантомной технологии и последующим прогнозом пострадиационной динамики концентрации нейтрофилов периферической крови с возможностью более адекватного прогноза клинического течения острой лучевой болезни.
Данная технология расчетов может быть использована для аварийной дозиметрии, а также для оптимизации локальной защиты организма человека при планируемом повышенном облучении в условиях массо-габаритных ограничений (например, в условиях космических полетов или при проектировании физической защиты рабочего места операторов критсборок) [3].
ВЫВОДЫ
- На основании созданной распределенной базы данных по острым лучевым поражениям человека с использованием интернет-совместимых технологий, получившей свидетельство государственной регистрации, построена система поддержки принятия решения при диагностике острых лучевых поражений, позволяющая оперативно использовать информационный ресурс с историями болезни пострадавших в радиационных авариях, и прогнозировать течение костномозгового синдрома острой лучевой болезни.
- Разработан и реализован алгоритм расчета распределения дозы по телу пострадавшего в результате неравномерного аварийного облучения с использованием воксел-фантомной технологии и дальнейшего прогнозирования течения костномозгового синдрома острой лучевой болезни. Расчет пострадиационной динамики концентрации нейтрофилов для двух реальных случаев, показал работоспособность данного метода в диапазоне дозы облучения красного костного мозга до 6 Гр.
- Неопределенность прогноза дозы облучения по критерию «среднее количество лимфоцитов за 3-6 сутки» составляет до 2 Гр. Если уровень лимфоцитов не выходит за пределы нормы (>1.2109/л), оценка дозы находится в пределах не более 2 Гр. Уровню лимфоцитов 1.0-1.2109 /л соответствует доза не более 3 Гр (нижняя граница доверительного интервала в обоих случаях равна нулю). Уровню 0.3-0.6109/л соответствует диапазон доз 2-8 Гр. И, наконец, снижение уровня лимфоцитов до величины менее <0.2109/л соответствует дозе более 8 Гр.
- В более поздний период (с 8 по 21 день) более информативным является тест «день 500 нейтрофилов». Неопределенность оценки дозы по данному тесту составляет до 1.8 Гр. После 21-го дня погрешность оценки дозы составляет 0.8 Гр.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- К.В.Котенко, А.В.Барабанова, А.Е.Баранов, А.Ю.Бушманов, И.А.Галстян, А.К.Гуськова, Ю.Е.Квачева, М.В.Кончаловский, В.И.Краснюк, Н.А.Метляева, Н.М.Надежина, В.Ю.Нугис, Ф.С.Торубаров, Т.М.Хамидулин. Свидетельство о государственной регистрации базы данных по острым лучевым поражениям человека, №2010620390 от 23.07.2010.
- В.Ю.Соловьев, А.Е.Баранов, А.В.Барабанова, А.Ю.Бушманов, И.А.Галстян, А.К.Гуськова, Н.В.Зиновьева, Ю.Е.Квачева, М.В.Кончаловский, В.И.Краснюк, Н.А.Метляева, Н.М.Надежина, В.Ю.Нугис, Ф.С.Торубаров, Т.М.Хамидулин. База данных по острым лучевым поражениям человека. Cообщение 1. Интеллектуальный интерфейс как составная часть системы поддержки принятия решения при диагностике острых лучевых поражений // Медицинская радиология и радиационная безопасность. - 2011. - Т. 56, № 3. - С. 5-13.
- В.Ю.Соловьев, А.Е.Баранов, Т.М.Хамидулин. База данных по острым лучевым поражениям человека. Cообщение 2. Прогнозирование пострадиационной динамики концентрации нейтрофилов периферической крови человека при неравномерном по телу аварийном облучении // Медицинская радиология и радиационная безопасность. - 2011. - Т. 56, № 4. - С. 24-31.
- Соловьев В.Ю., Нугис В.Ю., Хамидулин Т.М., Краснюк В.И. Исследование прогностической ценности гематологических критериев оценки степени тяжести лучевого поражения // Medline.ru: российский биомедицинский электронный журнал. – 2011. – Том 12, Ст. 35 (стр. 420 – 430). – URL: http://www.medline.ru/public/art/tom12/art35.html
- Хамидулин Т.М., Соловьев В.Ю. Оценка распределения дозы по телу пострадавшего при аварийном облучении с помощью воксел-фантомной технологии // Medline.ru: российский биомедицинский электронный журнал. – 2011. – Том 12, Ст. 40 (стр. 474 – 482). – URL: http://www.medline.ru/public/art/tom12/art40.html
- Соловьев В.Ю., Бушманов А.Ю., Барабанова А.В., Бирюков А.П. и Хамидулин Т.М. Анализ профессиональной принадлежности пострадавших в радиационных инцидентах на территории бывшего СССР // Медико-биологические и социально-психологические проблемы безопасности в чрезвычайных ситуациях, 2011, № 1, C. 5—9.

