<jylfhtyrj
Бондаренко Ирина Зиятовна
Особенности диагностики и лечения ИБС у больных сахарным диабетом типа 2
Автореферат диссертации на соискание
ученой степени доктора медицинских наук
14.00.03 – эндокринология
14.00.06 - кардиология
Москва, 2008
Работа выполнена в ФГУ Эндокринологическом Научном Центре Росмедтехнологий
Научные консультанты:
Академик РАН и РАМН, профессор, доктор медицинских наук Дедов Иван Иванович
Профессор, доктор медицинских наук Александров Андрей Алексеевич
Официальные оппоненты:
Доктор медицинских наук, профессор
Аронов Давид Меерович
Доктор медицинских наук, профессор
Арутюнов Григорий Павлович
Доктор медицинских наук
Токмакова Алла Юрьевна
Ведущее учреждение: Московский Государственный Медико-стоматологический Университет
Предполагаемая дата защиты 31 октября 2008 на заседании Специализированного Совета Д 001.13.01 при ГУ ЭНЦ Росмедтехнологий по адресу:117036, Москва, ул. Дм. Ульянова, 11
Общая характеристика работы
Актуальность:
Сахарный диабет типа 2 (СД 2) представляет собой быстрорастущую медицинскую и социальную проблему во всех индустриально развитых странах, благодаря ранней инвалидизации и высокой смертности прежде всего от сердечно-сосудистых осложнений. (И.И. Дедов, М.В.Шестакова, 2003). Ожидается, что количество заболевших диабетом к 2025 увеличится с 135 до 300 миллионов человек (King H., Aubert RE, 1998)
Несмотря на успешное развитие медицинских технологий в диагностике ИБС смертность от коронарной болезни сердца в популяции диабета не снижается. Острый коронарный синдром у лиц с СД 2 часто развивается в отсутствии значимого стеноза артерий сердца. В настоящее время Американская Ассоциация Сердца (AHA, S.C. Smith и соавт., 2006) и Европейское Общество Кардиологов (ESC, L. Rydn и соавт., 2007) рассматривают СД 2 как эквивалент ИБС в отношении риска последующих сердечно-сосудистых событий.
Высокая частота коронарной смерти среди пациентов с диабетом
обусловлена прежде всего объективными трудностями ранней диагностики ИБС. Бессимптомный характер ишемии миокарда при наличии доказанной ИБС регистрируется более, чем у 1/3 из них: по данным разных исследователей от 30 до 48 % (NakaM.1992,Caracciolo,1996, Brulport-CerisierV.,2000). А частое развитие кардиальной формы автономной нейропатии приводит к невозможности точного использования стандартных критериев достижения диагностического уровня стресс-теста, рекомендованного Американской ассоциацией сердца и Американской коллегии кардиологов (AHA/ACC, 1999) для верификации ИБС у больных СД. Поэтому выявление коронарной недостаточности на доклинической стадии ИБС в этой группе приобретает особое социальное значение.
Кроме того, для пациентов с СД 2 не разработаны столь же четкие рекомендации для коррекции ИБС, как для лиц, не страдающих СД, основанные на доказанных в крупных исследованиях методах лечения сердечно-сосудистой системы. Поэтому лечение ИБС у больных диабетом менее успешно (A.K. Gitt и соавт., 2003; W. Otter и соавт., 2004). Мало изучено влияние препаратов сульфанилмочевины на трансмембранный потенциал в кардиомиоцитах, лекарственной группы, наиболее часто используемой для нормализации уровня гликемии. В то же время известно, что вызываемые при этом электролитные нарушения могут менять чувствительность ЭКГ к ишемии, снижая диагностическую ценность данного метода в популяции диабета. Разработка рекомендаций в этой области имеет большое практическое значение.
У пациентов с диабетом статистически достоверно выше риск возникновения недостаточности кровообращения, коронарных событий и смерти, связанной с ИБС (A. Laukkanen и соавт., 2001, I.S Thrainsdottir и соавт, 2005). Данный факт подчеркивает значимость потенциального применения бета-блокаторов в этой популяции.
Ожидается, что новое поколение бета-блокаторов с высокой селективной защитой бета1- рецепторов и способностью корректировать дисфункцию эндотелия могут оказаться метаболически нейтральными и поэтому безопасными для лечения ИБС у пациентов с диабетом. Эта группа препаратов нуждается в дополнительном изучении.
В последние годы особое внимание мировых исследований направлено на улучшение методов оценки риска ИБС у каждого пациента с диабетом с целью выявления лиц, нуждающихся в "агрессивной" терапии. Разработка алгоритма ранней диагностики ИБС и пути ее коррекции являются актуальными проблемами эндокринной кардиологии.
Цель исследования:
Разработать алгоритм ранней диагностики ишемической болезни сердца у больных СД 2 в условиях современной сахароснижающей и кардипротективной терапии.
Задачи исследования:
1. Оценить возможности ЭКГ при проведении нагрузочного теста в диагностике ишемической болезни сердца у больных сахарным диабетом типа 2
2. Изучить роль спирометрических показателей в оценке «ишемического порога» у больных СД 2
3. Изучить особенности газообмена у больных СД 2 как фактора, влияющего на кардиальный прогноз.
4. Оценить роль стрессэхокардиографии в оценке нарушения локальной сократимости миокарда у больных СД 2 и степени ишемизации диабетического сердца.
5. Проанализировать чувствительность и специфичность стрессэхокардиографии в сравнении со стандартным нагрузочным тестом как методов ранней верификации ИБС у больных СД 2.
6. Оценить коронарный резерв у больных СД 2 и его вклад в показатели физической работоспособности диабетического сердца при ИБС
7. Оценить роль современных препаратов сульанилмочевины и бета-блокаторов в изменении "ишемического порога" при проведении диагностических нагрузочных тестов.
8. Разработать алгоритм ранней диагностики ИБС у больных сахарным диабетом типа 2
Научная новизна
1.Впервые в России разработан алгоритм ранней диагностики ИБС у больных сахарным диабетом типа 2, имеющих высокий риск развития ИБС, а так же у больных с бессимптомной ишемией миокарда
2.Впервые при разработке кардиологического тестирования комплексно оценены составляющие сахарного диабета, способные влиять на достоверность диагностики ИБС в этой популяции.
3. Разработаны пути коррекции ИБС с учетом особенностей влияния сахароснижающей терапии на степень ишемии миокарда у больных СД 2
4. Изучены метаболические последствия и разработан алгоритм выбора в наиболее востребованной группе лекарственных препаратов для коррекции ИБС у больных сахарным диабетом - бета-блокаторов
Практическая значимость
На основании результатов, полученных в ходе проведенных исследований разработан и предложен к внедрению в широкую практику алгоритм ранней диагностики ИБС для пациентов СД 2.
Сформулированы и обоснованы подходы к оптимальной коррекции ИБС с учетом течения сахарного диабета и его осложнений.
Апробация работы
Апробация диссертации проведена на заседании Диссертационного Совета Д 001.013.01 при ФГУ ЭНЦ Росмедтехнологий.
Представленные в работе результаты доложены на Российском Национальном конгрессе кардиологов (2002, 2003, 2004, 2005г), Втором и Четвертом Российском Диабетологическом Конгрессах (2002, 2004), Региональной научно-практической конференции в г.Томск (2003), 18-м Конгрессе Международной Диабетической Федерации (Париж, 2003), Региональной научно-практической конференции в г. Ростов (2008)
Публикации
Материалы диссертации опубликованы в виде 24 печатных работ в отечественных и зарубежных научных изданиях, из них 1 методические рекомендации для практического здравоохранения, 2 пособия для врачей
Структура и объем диссертации
Диссертация состоит из следующих разделов: введение, обзор литературы, характеристика материалов и методов исследования, результаты собственных исследований и их обсуждение, заключение, выводы, практические рекомендации, указатель литературы. Диссертация изложена на 209 страницах, содержит 29 таблиц, 26 рисунков, 2 схемы.
Внедрение результатов
Алгоритм неинвазивной диагностики ИБС при СД 2 внедрен в работу отделения кардиологии ФГУ ЭНЦ Росмедтехнологий. Результаты исследования используются в учебном процессе на кафедре диабетологии факультета усовершенствования врачей Московской медицинской академии им. И.М. Сеченова и кафедре поликлинической терапии Московского факультета Медицинского Государственного Университета им Н.И. Пирогова
Материалы и методы.
Обследовано 1015 пациентов с СД 2, обратившихся в ЭНЦ РАМН с 1998 по 2006 год, из них отобрано 248 пациентов в возрасте от 37 до 67 лет, не имеющих общепринятых противопоказаний для проведения нагрузочных тестов, а так же выраженных проявлений осложнений сахарного диабета. Не включались пациенты с ЭКГ и/или ЭХОКГ признаками крупноочагового поражения миокарда, а так же с измененной конечной частью желудочкового комплекса, затрудняющей интерпретацию ишемических изменений на ЭКГ при проведении нагрузочного теста. Все включенные больные соответствовали диагностическим критериям СД 2 по классификации ВОЗ (1997г). Так же в исследование было включено 12 здоровых добровольцев в качестве группы контроля. В общей сложности проведено 672 кардиологических исследований.
Обследуемые были разделены на группы с учетом целей и задач исследования.
Наличие жалоб, позволяющих заподозрить ИБС не являлось обязательным для включения в исследование. Всем участникам в целях верификации ИБС проводились ЭКГ, ЭХОКГ и стресс-спиро-эхокардиография. 13 пациентам с диабетом, имеющих положительный результат стресс-спиро ЭХОКГ была выполнена коронароангиография, У 12 пациентов с СД 2 и верифицированной ИБС исследовался коронарный резерв с помощью чреспищеводной допплерографии коронарных артерий. У этой же группы больных определялась чувствительность к инсулину клэмп -методом
Методы обследования:
Электрокардиографическое исследование в покое (ЭКГ) проводилось в 12 стандартных отведениях на аппарате Cardiosuny CK 620 AX фирмы Furuda (Япония). Признаками ЭКГ диагностики ишемии миокарда считались отрицательный коронарный зубец Т и ишемическая депрессия сегмента ST (глубина более 1 мм, форма горизонтальная или косонисходящая, регистрируется в 3 и более последовательных комплексах, в 2 и более отведениях)
Эхокардиографическое исследование проводилось на аппарате «HDI-5000c» (фирмы «ATL»,США).
Оценка локальной сократимости миокарда производилась из парастернальной позиции по длинной и коротким осям (на уровне папиллярных мышц) левого желудочка (ЛЖ) и из апикальной позиции в проекции 2-х, 4-х мерного камерного изображения ЛЖ. Оценка нарушений локальной сократимости осуществлялась согласно рекомендациям Американской Ассоциации эхокардиографистов с условным делением ЛЖ на 16 сегментов (Schiller N. Et all. 1989). На основании 16-сегментарной модели строения левого желудочка с целью качественного и количественного анализа движения стенок в режиме тканевого импульсно-волнового допплера проводились оценка локальной диастолической дисфункции. В двухмерном режиме с помощью 4-х балльной системы оценки определялись индекс нарушения локальной сократимости (ИНЛС) в покое и тотчас после нагрузки как отношение суммы баллов сократительной способности миокарда ЛЖ на общее количество сегментов. При этом за 1 балл принимался нормокинез, за 2 –гипокинез, за 3- акинез, за 4 –дискинез. В норме ИНЛС равен 1. Так же подсчитывалось количество сегментов с нарушенной сократимостью после нагрузки.
Стресс-cпироэхокардиография проводилась на ультразвуковом аппарате HDI-5000c (фирмы ATL, США) с интегрированной динамической цифровой стресс-программой с записью исследования на магнитооптический диск и на видеопленку, с использованием спироэргометрии и газоанализа выдыхаемого воздуха. Тест проводился на тредмиле «Wood Way EXO 43» (США) с автоматизированным управлением через встроенный интерфейс многофункциональной ЭКГ-станции «Cardiovit CS-100» фирмы «Shciller» (Швейцария).
Перед исследованием измерялся уровень АД, регистрировались ЭКГ и ЭХОКГ в покое с оценкой индекса нарушения локальной сократимости миокарда.
Стресс-тест проводился по протоколу, предложенному Bruce R.A. (1980)], согласно которому толерантность к физической нагрузке оценивалась по максимальному углу наклона дорожки, максимальной скорости ее движения, а также времени проведения пробы до критериев ее прекращения.
Запись ЭКГ во время нагрузки регистрировалась в конце каждой 3-й минуты, а также в момент прекращения пробы, в периоде восстановления - в конце 1-й, 3-й, 5-й, 7-й, 9-й минут и т.д. вплоть до восстановления исходной ЭКГ. Контроль за ритмом сердца осуществлялась по осциллоскопу во время нагрузки и в период восстановления.
Артериальное давление измерялось с помощью электронного тонометра «ВР-200» фирмы «Shсiller» (Швейцария) каждые 3 минуты исследования, в момент прекращения пробы, в первые 30 секунд после прекращения пробы, далее в конце 1-й, 3-й, 5-й, 7-й, 9-й и т.д. минут.
Оценивались следующие показатели стресс-теста:.
- Продолжительность теста,
- Продолжительность восстановительного периода,
- Пороговая частота ЧСС,
- Время появления и продолжительность патологической депрессии сегмента ST,
- Время появления, характер и продолжительность стенокардии или ее эквивалентов,
- Соотношение стенокардии (эквивалентов) с изменениями сегмента ST
- "Двойное произведение”, равное произведению ЧСС на САД на высоте нагрузки,( уд x мм. рт. ст x100/мин)
- С целью объективизации критериев прекращения нагрузочного теста использовался анализ показателей внешнего дыхания и газообмена с помощью непрерывной спирометрии.
Стресс-cпирометрия проводилась с помощью многофункциональной ЭКГ-станции «Cardiovit CS-100» фирмы «Shciller» (Швейцария) с встроенными модулем эрго-спирометрии, газовым анализатором B & К 1308 и стресс-программой EXEC III, позволяющей через встроенный интерфейс автоматически управлять тредмилом «Wood Way EXO 43» (США).
Анализировались следующие показатели:
1. Дыхательный коэффициент RQ=VCO2/VO2 (l/min), определяющий анаэробный порог (АП), уровень нагрузки, превышение которого сопровождается включением анаэробного источника энергообеспечения;
2. Максимальное потребление кислорода (VO2 ml/min), отражающий способность организма в условиях возрастающей нагрузки транспортировать кислород тканям ;
3. Максимальное выделение углекислого газа (VCO2 ml/min), отражающий аккумуляцию СО2 кардио-респираторной системой в тех же условиях;
4. VO2/HR, «кислородный пульс», количество кислорода, доставляемого в ткани с каждым сердечным сокращением.
5. VE (l/min), вентиляция легких, характеризующая объем внешнего дыхания во время стресс-теста.
6. VE/VC02, эквивалент углекислого газа, отражающий вентиляцию легких в пропорции к продукции С02
7. VE/V02, эквивалент кислорода, отражающий вентиляцию легких в пропорции к поглощенному кислороду.
8. Max METS (ml/min/kg V02), метаболический эквивалент, определяющий кратность увеличения потребности кислорода при нагрузке по сравнению с уровнем его потребления в состоянии покоя (1 МЕТ в состоянии покоя сидя=3,5 мл/мин/кг V02
Помимо общепринятых критериев прекращения нагрузочного теста использовался "дыхательный коэффициент" RQ. Превышение данного показателя более 1 в условиях непрерывной спирометрии указывало на то, что дальнейшее проведение исследования не эффективно (К.Weber, 1997). "Пороговая" ЧСС, согласно рекомендациям Американской Кардиологической и Американской Диабетологической ассоциаций (1999) считалась диагностически значимой, если достигала не менее 90% от максимально возможной по возрасту пациента.
Проба с нагрузкой расценивалась как положительная при появлении участков нарушения локальной сократимости не менее чем в двух близлежащих сегментах или усугублении диссинергии в исходно имеющихся зонах с нарушением сократимости миокарда. Критериями безболевой ишемии на ЭКГ при проведении стресс –теста считались: горизонтальное или косонисходящее смещение сегмента ST не менее чем на 1, 5 мм через 80 или более миллисекунд после точки “J”, не сопровождающееся типичным ангинозным приступом, при анализе ЭХОКГ тотчас после нагрузки – нарушение локальной сократимости в более чем двух рядом расположенных сегментах.
Чреспищеводная эхокардиография с дипиридамолом использовалась для измерения коронарного резерва. Проводилась чреспищеводная доплеровская оценка скоростей кровотока в коронарном синусе (КС), левой коронарной артерии (ЛКА), передней нисходящей артерии (ПНА) при проведении дипиридамоловой пробы. Коронарный резерв рассчитывался.как отношение диастолической скорости в исследуемых сосудах на пике введения дипиридамола к исходной диастолической скорости. В норме этот показатель должен находиться в диапазоне 2-3 усл.ед. (А.В. Врублевский, 2006).
Чувствительность к инсулину определяли методом одновременного введения глюкозы и инсулина (клэмп-метод). Использовался нормогликемический вариант клэмп-метода: исследование проводили при концентрации глюкозы в крови 5,3+0,3 ммоль/л. Для постоянного контроля гликемии и автоматического введения инсулина и глюкозы использовали аппарат «Биостатор», работающий в режиме 7:1. (Исследование проводил в.н.с. ФГУ ЭНЦ Росмедтехнологий Майоров А.Ю.)
В протокол исследования так же входили: осмотры, эндокринолога и окулиста, оценка содержания в крови натощак глюкозы, гликозилированного гемоглобина, липидов, креатинина, мочевины, определение суточной микроальбуминурии на каждом из этапов обследования пациентов..
Исследование концентрации мочевины, креатинина и глюкозы проводилось по стандартным методикам на автоматическом анализаторе фирмы “Abbott” (США), гликозилированного гемоглобина капиллярной крови - на аппарате “Dia Stat” фирмы “Bio-Rad” (Германия), липидов – стандартными наборами фирмы “Abbott” (США) на автоматическом анализаторе “Spektrum” (США). Суточная экскреция альбумина с мочой осуществлялась методом пламенной фотометрии на аппарате “Kone” (Финляндия).
Использовались протоколы открытого, двойного перекрестного метода обследования, а так же с применением контрольной группы
Методы статистического анализа
Статистический анализ осуществляли с использованием стандартных статистических пакетов SPSS (SPSS Inc.) для персональных компьютеров. В группах рассчитывали средние (M) и стандартные отклонения (). Для проверки гипотезы о равенстве средних величин вычисляли t-статистику и аппроксимацию t-статистики для предположения о неравенстве дисперсий в сравниваемых группах. Гипотезу о нормальности распределения величин анализируемых признаков проверяли по критерию 2. Сравнение относительных величин производили с использованием критерия 2. Применяли регрессионный и корреляционный анализ, использовали процедуру вычисления парных коэффициентов корреляции (r). Так же использована программа "Statistica" ("StatSoft", USA).Расчеты проводились с помощью непараметрических методов статистики. Результаты представлены в виде медианы с интерквартильным размахом (ИР, 25-й – 75-й процентиль). При сравнении групп использовался критерий Манн-Уитни
Результаты исследований и их обсуждение
По данным литературы у больных СД 2 без верифицированных заболеваний сердечно-сосудистой системы изменения на ЭКГ, зарегистированные при нагрузочных тестах являются статистически значимым независимым предиктором возникновения сердечно-сосудистых событий (P.M. Okin и соавт. 2004, A. Jimnez-Corona и соавт. 2006, A. De Santiago и соавт. 2007)
. Согласно рекомендациям Американской ассоциации сердца и Американской коллегии кардиологов (AHA/ACC) всем пациентам старше 50 лет, страдающим СД, при наличии атипичных болей в прекардиальной области должен быть проведен нагрузочный тест с одновременной регистрацией ЭКГ, в то время как пациенты без признаков ангинозных приступов, но старше 60 лет должны быть обследованы на наличие обструктивной ИБС (R.J. Gibbons и соавт., 2002). Особенности неинвазивной диагностики ИБС изучались у больных СД 2 с высоким риском развития ИБС (Stamler J. et all. 1993, Nathan D. Et all. 1997). Для увеличения чувствительности и специфичности неинвазивных методов выявления ИБС были оценены возможности нагрузочного теста с одновременной ультразвуковой визуализацией сердца и мониторированием показателей газообмена. Для данного этапа работы обследовано 59 пациентов, которые по результатам стресс теста были поделены на 3 группы: с болевой и безболевой формами ИБС, а так же с отсутствием ИБС. Общая клиническая характеристика пациентов представлена в табл. 1
Табл.1 Клиническая характеристика и факторы риска ИБС у больных СД 2 (М±)
| Показатель | Больные СД2 (n=59) |
| Возраст (г) Продолжительность СД 2 (г) Гликированный НВА1С (%) Гликемия натощак (моль/л) Больные на инсулинотерапии (n) Больные на пероральной сахароснижающей терапии (n) Индекс массы тела (кг/м2) Количество больных с ожирением (n) Количество больных с обдоминальным ожирением из числа лиц с ожирением (n) Артериальная гипертония (n) Курение (n) Семейный анамнез по ИБС (n) | 54,8±0,9 8,8±0,6 8,7±0,9 8,8±0,4 17 (29%) 42 (71%) 30,5±0,6 34 (57,6%) 33 (97%) 59 (100%) 17 (28,8%) 19 (32%) |
Распространенность микрососудистых осложнений СД2 среди этих пациентов представлена в табл. 2
Табл.2 Распространенность микрососудистых осложнений у больных СД 2 (%)
| Показатель | Больные СД 2 (n=59) |
| Диабетическая ретинопатия (n) Диабетическая нефропатия на стадии МАУ (n) на стадии протеинурии (n) на стадии ХПН 1 (n) | 28 (47,5%) 14 (23,7%0 4 (6,8%) 2 (3,4%) 8 (13,6%) |
При проведении стресс-спироэхокардиографии у больных сахарным диабетом 2 типа получены следующие показатели эффективности работы сердца с различными клиническими проявлениями ИБС).(табл.3)
Табл.3
Показатели работоспособности миокарда результатам стресс-спироэхокардиографии у больных сахарным диабетом 2 типа (M±m)
| Показатели | С болевой формой ИБС (n=20) | С безболевой формой ИБС (n=19) | Без ИБС (n=20) |
| Исходно | 1 | 2 | 3 |
| ЧСС (уд/мин) САД (мм рт ст) ДАД (мм рт ст) Двойное произведение ( | 82,7+2,1 139,2+3,8# 85,1+1,3 115,6+4,9 | 82,2+3,1 135,0+3,7 82,6+1,5 111,0+5,1 | 83,6+3,4 130,1+1,8# 82,2+1,2 108,4+4,3 |
| На пике нагрузки | 1 | 2 | 3 |
| ЧСС (уд/мин) САД (мм рт ст) ДАД (мм рт ст) Двойное произведение Длительность нагрузки (с) | 142,5+3,9# 179,3+6,1#* 94,5+3,0# 257,1+13,2# 307,4+30,7# | 146,4+4,4& 188,4+5,5&* 95,8+2,9& 278,5+13,5& 425,3+38,9& | 160,5+2,3#& 194,7+2,8#& 100,1+1,8#& 312,7+7,2#& 564,2+26,9#& |
| *- достоверное различие между 1 и 2 (p<0,05), &- достоверное различие между 2 и 3 (p<0,05), # - достоверное различие между 1 и 3 (p<0,05) | |||
Исходные показатели работоспособности сердца были примерно одинаковы во всех группах, за исключением более высокого уровня САД у пациентов с болевой формой ИБС и не имеющих ИБС (139,2+3,8 vs 130,1+1,8 [р=0,036]).
Как видно из табл. 3 основные гемодинамические параметры, такие как ЧСС, САД, ДАД на высоте нагрузки были достоверно выше (р<0,05) у пациентов с диабетом без ИБС по сравнению с группами как с болевой, так и бессимптомной формами ИБС. Статистически значимых различий по данному параметру между собой у больных с ИБС выявлено не было (р>0,05).
Показатели работоспособности у пациентов без ИБС так же существенно отличались по сравнению с пациентами в 1 и 2 группах. Значение «двойного произведения» на пике нагрузки достоверно превышало этот показатель в группе пациентов без ИБС, чем в группах с болевой (312,7+7,2 vs 257,1+13,2 [р=0,001]) и с безболевой формами ИБС (312,7+7,2 vs 278,5+13,5 [р=0,033]). Статистически значимых различий по данному параметру групп с ИБС между собой выявлено не было (р=0,261). Больные без ИБС имели достоверно большую продолжительность теста, чем больные с болевой (р=0,0001) и безболевой формами ИБС (р=0,032). Различия в группах с ИБС статистически не различались (р=0,201).
Таким образом, полученные данные подтверждают, что по результатам стресс-спироэхокардиографии пациенты СД 2 с клиническими проявлениями ИБС и с безболевой формой ИБС имели достоверно более низкие показатели работоспособности миокарда, чем больные сахарным диабетом 2 типа с отсутствием признаков ИБС. Больные СД 2 с болевой и безболевой формами ИБС не различались между собой по исследованным показателям работоспособности миокарда.
Проанализированы причины прекращения стресс-спироэхокардиографии у больных СД2 с различными клиническими формами ИБС (табл.4)
табл.4
Критерии прекращения стресс-спироэхокардиографии у больных сахарным диабетом 2 типа (%)
| Показатели | С болевой формой ИБС (n=20) | С безболевой формой ИБС (n=19) | Без ИБС (n=20) |
| Достижение анаэробного порога, n Появление ЭКГ-критериев, n Развитие болевого синдрома, n | 0 (0%)*# 12 (60%)# 15 (75%)*# | 7 (37%)*& 12 (63%)#& 0 (0%)* | 20(100%)#& 0 (0%)& 0 (0%)# |
| *- достоверное различие между 1 и 2, &- достоверное различие между 2 и 3, # - достоверное различие между 1 и 3 | |||
Частота ЭКГ-критериев достоверной ишемии миокарда была одинаковой в обеих группах с ИБС (2=0,17). В группе больных без ИБС ишемические изменения конечной части желудочкового комплекса отсутствовали, и эти изменения были достоверны по сравнению с группами больных с ИБС (60% vs 0% [2=18,6]; 63% vs 0% [2=20,2]).
Развитие типичного болевого синдрома как критерия прекращения пробы встречался в группе больных с болевой формой ИБС у 75% (15 из 20) больных, в то время как в группе больных с безболевой формой ИБС и группе без ИБС ангинозные боли отсутствовали. Эти различия были статистически достоверны (75% vs 0% [2=23,07]; 75% vs 0% [2=24,36]).
Обращает на себя внимание, что у 7 больных с безболевой формой ИБС не было традиционных ЭКГ-критериев наличия ишемии миокарда и причиной прекращения пробы у них явилось достижение анаэробного порога. У этих пациентов были выявлены только ЭХОКГ- критерии нарушения локальной сократимости миокарда.
При анализе результатов стресс-теста по чувствительности ЭКГ к ишемии миокарда в различных группах пациентов с ИБС получены следующие данные. (табл 5)
Таблица 5
Выявляемость ЭКГ-критериев ишемии при стресс-спироэхокардиографии у больных сахарным диабетом 2 типа с различными формами ИБС,%
| Результаты стресс-спироэхокардиографии по ЭКГ-критериям | С болевой формой ИБС (n=19) | С безболевой формой ИБС (n=19) |
| ЭКГ-позитивная, n | 17 (89,5%) | 12(63,2%) |
| ЭКГ-негативная, n | 0 (0%)* | 7(36,8%)* |
| Сомнительный результат по ЭКГ-критериям, n | 2 (10,5%) | 0 (0%) |
| *достоверные различия между группами | ||
Стресс-спироэхокардиография была положительной по ЭКГ–критериям (ЭКГ-позитивная) в группе больных сахарным диабетом с болевой формой ИБС у 89,5% (17 из 19) пациентов, в том числе по развитию полной блокады ЛНПГ у одного пациента. В группе больных сахарным диабетом с безболевой формой ИБС стресс-спироэхокардиография была положительной по ЭКГ–критериям у меньшего числа пациентов – у 63,2% (12 из 19) человек, но выявленные различия были статистически не достоверны (2=3,6).
Стресс-спироэхокардиография была отрицательной по ЭКГ–критериям (ЭКГ-негативная) у 36,8% (7 из 19) пациентов в группе больных диабетом с безболевой формой ИБС, в то время как в группе с болевой формой ИБС ЭКГ-негативных результатов исследования не было. Выявленные различия были статистически значимы (2=8,9).
В группе больных с болевой формой ИБС стресс-спироэхокардиография была сомнительной по ЭКГ-критериям у 10,5% (2 из 19) пациентов с низкой толерантностью к нагрузке, у которых проба была прекращена по развитию типичного болевого приступа, не сопровождающегося ишемическими изменениями ЭКГ, что не имело достоверных отличий от группы с безболевой формой ИБС (2=8,9).
Из полученных данных следует, что 18,4% больных сахарным диабетом 2 типа с ишемической болезнью сердца, выявленной при стресс-спироэхокардиографии, имели ЭКГ-негативные проявления ИБС, а в группе больных с безболевой формой ИБС – электрокардиографические проявления ИБС отсутствовали у 36,8% пациентов. По результатам проведенного исследования пациентам с диабетом, имеющих факторы риска развития ИБС целесообразно проведение стресс-спироЭХОКГ в целях скринингового выявления коронарной недостаточности, минуя стадию проведения стандартного нагрузочного теста, предложенного Американской Коллегией Кардиологов и Американской Диабетологической Ассоциацией (Consensus Development Conference on the Diagnosis of Coronary Heart Disease in People With Diabetes, 1998, 2002).
При анализе факторов, способных влиять на чувствительность ЭКГ к ишемии (микрососудистые осложнения диабета) ЭКГ-позитивные и ЭКГ-негативные пациенты не различались между собой. Тем не менее, такие осложнения СД 2 как диабетическая нефропатия и диабетическая ретинопатия недостоверно чаще встречались в группе с индуцированной нагрузкой ишемической депрессией сегмента ST, чем при ее отсутствии.
Оценена так же способность факторов риска развития ИБС влиять на чувствительность ЭКГ к миокардиальной ишемии у больных с разными формами ИБС (табл.5 )
Табл. 5
Факторы риска ИБС у больных СД 2 с ЭКГ-позитивными и ЭКГ негативными проявлениями ИБС (M + m)
| Показатели | C ЭКГ- позитивной ИБС (n=29) | C ЭКГ- негативной ИБС (n=7) | р | 2 |
| Курение (n) | 5 (17%) | 1 14%) | - | 0,04 |
| Индекс массы тела, кг/м2 | 30,3+0,7 | 28,4+1,9 | 0,436 | - |
| САД, мм. pт. cт. | 137,11+2,88 | 126,43+4,19 | 0,335 | - |
| ДАД, мм. pт. cт. | 83,96+1,06* | 78,57+1,43* | 0,043 | - |
| Общий холестерин, ммоль/л | 5,91+0,2 | 5,92+0,6 | 0,764 | - |
| ХСЛПВП, ммоль/л | 1,32+0,1 | 1,23+0,2 | 0,587 | - |
| ХСЛПНП, ммоль/л | 3,56+0,3 | 2,88+0,6 | 0,359 | - |
| Триглицериды, ммоль/л | 2,29+0,17* | 1,55+0,21* | 0,038 | - |
| Микроальбуминурия (n) | 6 (20,7%) | 1 (14%) | - | 0,80 |
| Мочевая кислота, мкмоль/л | 292,8+36,9 | 207,3+36,5 | 0,855 | |
| *достоверные различия между группами | ||||
Выявлены достоверные различия по уровню ДАД и концентрации триглицеридов. Для диабетиков с ЭКГ-позитивной формой ИБС уровень ТГ превышал нормативную величину – 2,29+0,17 ммоль/л и достоверно превышал уровень этих липидов в группе с ЭКГ-негативной формой ИБС – 1,55+0,21 ммоль/л (р=0,038). Кроме того, больные СД 2 с ЭКГ-позитивной формой имели достоверно более высокие цифры диастолического артериального давления в покое (р=0,04).
При корреляционном анализе у больных СД 2 с ИБС была выявлена достоверная отрицательная взаимосвязь глубины депрессии сегмента ST с уровнем гликированного гемоглобина (r=- 0,385, р=0,048) (Рис.1).
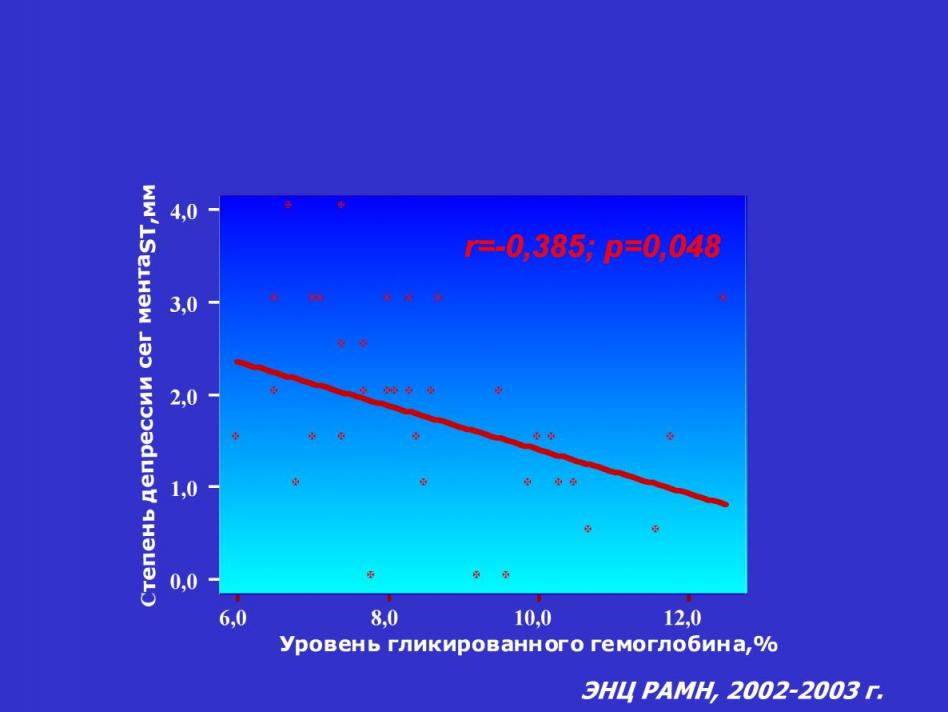
Рис.1 Влияние степени компенсации углеводного обмена (НВА1С%) на степень депрессии сегмента ST
Так же у этих пациентов выявлены достоверная положительная связь глубины депрессии сегмента ST со значением систолического АД в покое (r=0,376, р=0,049), выявлена близкая отрицательная связь глубины депрессии сегмента ST с индексом массы тела (r=- 0,319, р=0,098) и близкая положительная связь с уровнем холестерина липопротеидов низкой плотности (r=0.413, р=0,079).
У больных СД 2 с ИБС установлены достоверные положительные связи глубины депрессии сегмента ST с отношением толщины МЖП к толщине задней стенки ЛЖ (r=0,442, р=0,021) и с отношением конечно-диастолического объема ЛЖ к площади поверхности тела (r=0,449, р=0,016).
Таким образом, на чувствительность ЭКГ к ишемии миокарда у больных сахарным диабетом 2 типа могут влиять как метаболические параметры (степень компенсации углеводного обмена, ожирение, дислипидемия), так и проявления ремоделирования диабетического сердца.
| Показатели | Контрольная группа (n =15) | Группа пациентов с СД 2 (n =12) |
| Возраст, лет | 43,6 ± 9 | 48,4 ± 8 |
| Мужчины/женщины | 11/4 | 6/3 |
| ИМТ (кг\м2) | 30,74 (29,71;32,87) | 33,68 (31,82; 34,31) |
| Hbl % | - | 7,65 (7,54;8,15) |
| ЧСС исходно (сек.) | 76(71;79) | 73 (71; 75) |
| САД исходно (мм.рт.ст.) | 128 (118; 134) | 132 (124; 138) |
| ДАД исходно (мм.рт.ст.) | 84 (76; 98) | 88 (72; 96) |
Осбенности газообмена у больных СД2 в условиях непрерывной спирометрии (протокол 1)
В ходе проведения стрессЭХОКГ были изучены показатели газообмена, которые использовались в качестве "анаэробных критериев" прекращения нагрузочного теста. В более ранних исследованиях эти показатели применялись в целях стандартизации диагностики недостаточности кровообращения (Д.М. Аронов, 1980; K. Weber,1988, 1997). Нами проанализированы особенности внешнего дыхания и газообмена у пациентов с СД2, не имеющих жалоб со стороны сердечно-сосудистой системы в сравнении со здоровыми людьми в условиях непрерывной спирометрии.
С этой целью в исследование включены 12 пациентов с СД 2 типа без ИБС (средний возраст 48,4 ±8 лет) и 15 лиц без диабета, составившие контрольную группу (средний возраст 43,6 ±9 лет) (Табл.6).
Табл. 6 Клиническая характеристика пациентов с СД 2 и контрольной группы
. Данные результатов обследования представлены в виде медианы с интерквартильным размахом.
Включенные лица не имели общепринятых противопоказаний для проведения нагрузочного теста. Критерием исключения послужила необходимость приема лекарственных препаратов, влияющих на проявления ишемических изменений на ЭКГ. Так же не включались больные с СД 2, находящиеся на инсулинотерапии, имеющие выраженную декомпенсацию углеводного обмена, частые гипогликемии в анамнезе, а также такие осложнения СД как диабетическая нефропатия, диабетическая пролиферативная ретинопатия. В дальнейшем из анализа исключались пациенты, у которых при проведении стресс-спироэхокардиографии (стресс-спироЭХОКГ) были выявлены диагностически значимые изменения конечной части желудочкового комплекса и/или зоны нарушения локальной сократимости миокарда, а также те лица, которые не смогли достичь "анаэробного порога" в условиях непрерывной спирометрии.
Обе группы были сопоставимы по возрасту, полу, индексу массы тела, исходному уровню ЧСС, САД и ДАД. Пациенты с диабетом не различались между собой по уровню физической активности, степени компенсации углеводного обмена, стажу заболевания, выраженности микро и макрососудистых осложнений, типу сахароснижающей терапии, т.е. факторов, способных влиять на показатели газообмена
Показатели гемодинамики и спироэргометрии, полученные во время стресс-теста, у пациентов с СД 2 и в контрольной группе представлены в таблице 7.
Табл.7 Показатели гемодинамики и спироэргометрии у пациентов
СД 2 и контрольной группы
| Контрольная группа (n = 15) | Группа пациентов с СД 2 (n =12) | |
| Длительность теста (сек.) | 511,00(469,00; 561,00) | 419,00 (415,00;444,00)** |
| METS (усл.ед.) | 9,30 (8,70;10,80) | 6,20 (5,40; 7,00) ** |
| Макс ЧСС (уд. в мин.) | 165,00(156,00; 173,00) | 154,00 (151,00; 159,00) |
| Макс.САД (мм.рт.ст) | 181,00 (160,00; 200,00) | 160,00 (148,00; 170,00) |
| Макс ДАД (мм.рт.ст) | 95,00 (80,00; 115,00) | 100,00 (94,00; 105,00) |
| V O2 мл/мин) | 32,40 (30,30; 37,50) | 20,90 (18,80; 24,50)** |
| V CO 2 (мл/мин) | 2922,00(2213,00;3568,00) | 2164,00(1664,00;2682,00)* |
| VE (л/мин) | 69,00 (60,00; 91,00) | 65,00 (50,00; 69,00) |
Данные результатов представлены в виде медианы с интерквартильным размахом;
р< 0,05* ; р< 0,001**
Группы не различались между собой по уровню максимально достигнутых ЧСС, САД и ДАД, а так же по длительности теста. При этом такие показатели газообмена, как метаболический эквивалент (МЕТ), уровни утилизации углекислого газа (VCO2) и поглощения кислорода (VO2) были достоверно ниже у лиц с СД2, чем в контрольной группе (p<0,05; p<0,01). Таким образом, при одинаковой высокой толерантности к физической нагрузке пациенты с диабетом, не имеющие коронарную патологию демонстрировали сниженный уровень потребления кислорода, являющегося важным маркером стадии недостаточности кровообращения (К.Weber, 1997).Функциональное состояние этих пациентов по числу метаболических единиц (МЕТ) соответствует II функциональному классу ИБС у лиц, не имеющих эндокринную патологию (Д.М. Аронов, 1980).
Пути коррекции ИБС при СД 2 (протокол 2)
В последние годы для коррекции сердечной недостаточности активно применяются бета-блокаторы. Европейское Общество Кардиологов и Европейская Ассоциация по Изучению Диабета (Guidelines on diabetes, pre-diabetes and cardiovascular diseases, 2007) рекомендовали использовать селективный бета-блокатор метопролол (наряду с бисопрололом и карведилолом) как препарат "первой линии" для лечения недостаточности кровообращения у больных СД 2. В ряде работ указано, что бета-блокаторы уменьшают индуцированную нагрузкой гипервентиляцию, которая провоцирует усиление выделения углекислого газа и неадекватный рост минутной вентиляции легких (VE), что в свою очередь приводит к быстрому достижению анаэробного порога. Эти изменения характерны для недостаточности кровообращения (K.Weber, 1997).
В целях изучения влияния бета-блокаторов на показатели газообмена при диабете пациенты с СД 2 (основная группа, протокол 1) в течение 2 месяцев принимали метопролол в суточной дозе 50-75 мг. Остальная терапия при этом не менялась. На этом фоне проводилась спироэргометрия. В таблице 8 приведены показатели гемодинамики и газообмена у пациентов с СД 2 до и на фоне приёма метопролола.
Табл.8. Показатели гемодинамики и спироэргометрии
у пациентов с СД 2 до и на фоне приема метопролола
| До назначения метопролола (n =12) | На фоне приема метопролола (n =12) | |
| Длительность теста (сек.) | 419,00 (415,00; 44,00) | 513,00 (498,00; 528,00)* |
| METS (усл.ед) | 6,20 (5,40; 7,00) | 7,30 (6,60; 8,00) |
| ЧСС исходно (уд\мин) | 73,00 ( 71,00; 75,00) | 59,00 (55,00; 62,00) ** |
| Макс ЧСС (уд\мин) | 154,00 (151,00; 159,00) | 127,00 (121,00;129,00)** |
| Макс САД (мм рт.ст.) | 160,00 (148,00; 170,00) | 145,00 (144,00;150,00)** |
| Макс ДАД (мм рт.ст.) | 100,00 (94,00; 105,00) | 90,00 (85,00; 95,00)** |
| V O2 (мл/мин) | 20,90 (18,80; 24,50) | 27,90 (23,30; 31,40) |
| V CO 2 (мл/мин) | 2164,00(1664,00;2682,00) | 2891,00(2453,00;2998,00)* |
| VE (л/мин) | 65,00 (50,00; 69,00) | 71,00 (59,00;73,00) |
Данные результатов группы сравнения представлены в виде медианы с интерквартильным размахом
р< 0,05 *; р< 0,001**
В нашем исследовании у пациентов с СД 2 вследствие приема метопролола отмечалось усиление продукции СО2 (р<0,05) на фоне увеличения времени достижения "анаэробного порога" (р<0,01) и уменьшения пиковой ЧСС (р<0,05), что может отражать снижение степени тканевой гипоксии. (табл.8).
При анализе данных, полученных при проведении теста на фоне приема метопролола, выявлено статистически достоверное увеличение продолжительности нагрузки до момента наступления «анаэробного порога» (р<0,05). Как и следовало ожидать, уровень исходной и максимальной ЧСС, максимальных САД и ДАД при приеме бета-блокатора был ниже, чем до его назначения (р<0,05).
При этом отмечалось повышение МЕТ и VO2 мах. Несмотря на отсутствие статистической достоверности хотелось бы подчеркнуть, что на фоне приема метопролола пациенты с диабетом «приближались» к представителям контрольной группы (протокол 1), что продемонстрировано на рис № 2.
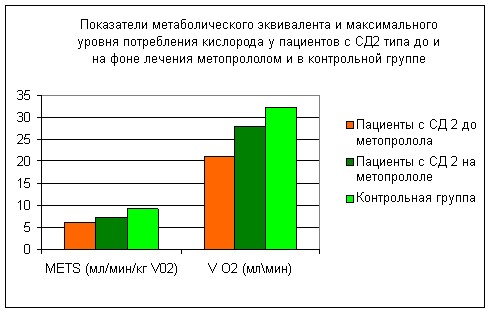
Рис.2 Динамика МЕТ и VO2 у пациентов с СД2 до и на фоне
приема метопролола и в контрольной группе

Рис.3 Динамика VCO2 у пациентов с СД 2 до и на фоне
Приема метопролола и в контрольной группе
Скорость выведения углекислого газа достоверно увеличивалась на фоне лечения метопрололом (рис 3). При этом динамика потребления кислорода и выведения углекислого газа привели к повышению минутной вентиляции легких и увеличения эффективности работы кардиореспираторной системы.
Оптимизация выбора терапии при СД 2 и ИБС (протокол 3)
1. Метаболические последствия применения бета-блокторов
у больных с СД2
Очевидность пользы применения бета-блокаторов для коррекции тканевой гипоксии у больных СД 2 привела к поиску тех из них, которые не только оказывают положительное влияние на диабетическое сердце, но и способны воздействовать на метаболические последствия сахарного диабета.
. Заслуживают внимание высокоселективные бета-блокаторы, т.к. ожидается минимальное их влияние на инсулинорезистентность. Особый интерес представляет новое поколение этой группы, имеющих NO модулирующую активность и способность уменьшать дисфункцю эндотелия. К таким препаратам относится небиволол. Есть данные, что за счет перечисленных свойств небиволол не влияет на метоболизм глюкозы и инсулиновую чувствительность тканей у больных сахарным диабетом, в отличие от атенолола, снижающего чувствительность к инсулину ( Lacourciere,1997). У пациентов без диабета небиволол существенно не менял показатели липидного спектра и уровни аполипопротеинов А1 и В, маркеров атерогенеза (Chan 1992, Fogari 1997).
Нами изучено влияние суперселективного бета-блокатора и донатора дополнительного монооксида азота небиволола на показатели липидного и углеводного обмена у больных СД 2. На 1 этапе исследования с этой целью обследовано 35 пациентов, имеющих СД 2, страдающих мягкой артериальной гипертонией (27 пациентов- основная группа, 15 пациентов – группа контроля). Сопутствующая ИБС была диагностирована у 20 больных основной группы (74,1%). У 16 из них ИБС протекала в форме стабильной стенокардии, у 4-х в виде безболевой ишемии миокарда, выявляемой при стандартном нагрузочном тесте на тредмиле. Группы были сопоставимы по основным клиническим характеристикам, которые представлены в табл.9
Табл.9 Основные клинические характеристики больных
СД 2 типа с артериальной гипертонией (М±SD)
| Показатели | Основная группа (n=27) | Группа контроля (n=15) | 2 | p |
| Возраст (годы) | 58,8±7,56 | 51,4±3,8 | - | >0,1 |
| Количество мужчин/женщин (n/n) | 14/13 | 9/6 | 0,03 | >0,1 |
| Продолжительность СД 2 типа (годы) | 10,4±5,1 | 8,2±1,8 | >0,1 | |
| Гликированный гемоглобин HbA1c (%) | 7,6±0,8 | 8,7±1,4 | >0,1 | |
| Гликемия натощак (ммоль/л) | 9,0±1,9 | 9,1±2,1 | >0,1 | |
Больные на пероральной сахароснижающей терапии (n):
| 27 (100%) 18 (66,7%) 9(33,3%) | 15 (100%) 9(60%) 6(40%) | - 0,01 0,01 | - >0,1 >0,1 |
| Индекс массы тела (кг/м2) | 29,5±3,1 | 30,0±1,6 | >0,1 | |
| Ожирение (n) | 12 (44,4%) | 8(53,3%) | 0,05 | >0,1 |
| Диабетическая ретинопатия (n) | 11 (40,7%) | 7 (46,7%) | 0,00 | >0,1 |
| Микроальбуминурия (n) | 3 (11%) | 2(13%) | 0,01 | >0,1 |
| Артериальная гипертония (n) | 27 (100%) | 15(100%) | - | - |
| Семейный анамнез по ИБС (n) | 19 (70,4%) | 12(80%) | 0,10 | >0,1 |
Применение в течение 8 недель небиволола в дозе 5 мг в сутки сопровождалось достоверным снижением САД и ДАД в 1группе (р<0,05; р<0,05). В группе контроля достоверных изменений не произошло.
Через 8 недель приема небиволола у больных основной группы не отмечено значимых изменений уровней общего ХС и ХС ЛПНП по сравнению с исходными значениями (табл.10). При этом отмечалось снижение концентрации триглицеридов в крови. Различие средних концентраций ТГ до и после применения небиволола у больных СД 2 основной группы имело достоверную тенденцию к статистическому различию (0,05 < p < 0,1). В контрольной группе существенных изменений уровня ТГ за период наблюдения не отмечено.
Табл. 10
Динамика уровней липидов крови на фоне приёма небиволола у больных СД 2 типа (M±)
| Показатели (ммоль/л) | До приёма небиволола (n=20) | На фоне приёма небиволола (n=20) | P |
| ХС общий ХС ЛНП ХС ЛВП ТГ | 6,8±1,1 4,7±0,4 0,86±0,2 2,9±0,7 | 6,9±1,3 4,5±0,6 0,84±0,3 2,3±0,4 | >0,1 >0,1 >0,1 0,05<p<0,1 |
Средний уровень триглицеридов стал соответствовать рекомендуемому для лиц с умеренным риском развития ИБС- 2,3 ммоль/л (NCEP, 1993).
Целесообразность применения бета-блокаторов у больных с СД 2, имеющих ИБС привела к изучению не только антиишемической эффективности небиволола, но и оценке его метаболической нейтральности.
Второй этап исследования: С этой целью из основной группы было отобрано 14 пациентов с СД 2, имеющих верифицированную с помощью стресс-теста ИБС. Обязательным условием участия на втором этапе исследования являлась воспроизводимость на фоне бета-блокаторов (минимум в двух стресс-тестах) ишемической депрессии сегмента ST на ЭКГ не менее 1,5 мм от точки j и продолжительностью не менее 80 мсек от изолинии при наличии ангинозной боли и не менее 2 мм при отсутствии клинических проявлений стенокардии. Пациентам назначался атенолол в дозе 50 мг в сутки с последующей его заменой через 3 месяца на небиволол в дозе 5 мг в сутки и возвращением к исходной терапии атенололом через такой же промежуток времени. Дизайн исследования представлен на рис. 4
На каждом из этапов замены бета-блокатора проводились cтрессЭХОКГ с непрерывной спирометрией, измерение липидного профиля и уровня НВА1С. Кроме того, на фоне изменения терапии определялась чувствительность к инсулину с помощью эугликемического клэмп-метода.

Рис. 4Схема применения бета-блокаторов на 2 этапе исследования.
С помощью такого перекрестного метода было изучено воздействие небиволола на показатели инсулинорезистентности и компенсацию углеводного обмена, а так же связь этих показателей со степенью ишемии миокарда левого желудочка, уровнем физической работоспособности и динамикой показателей газообмена.
Было обнаружено, что после перехода на небиволол показатели чувствительности к инсулину у большинства больных (у 11 из 14 больных-79%) улучшились (рис.5). 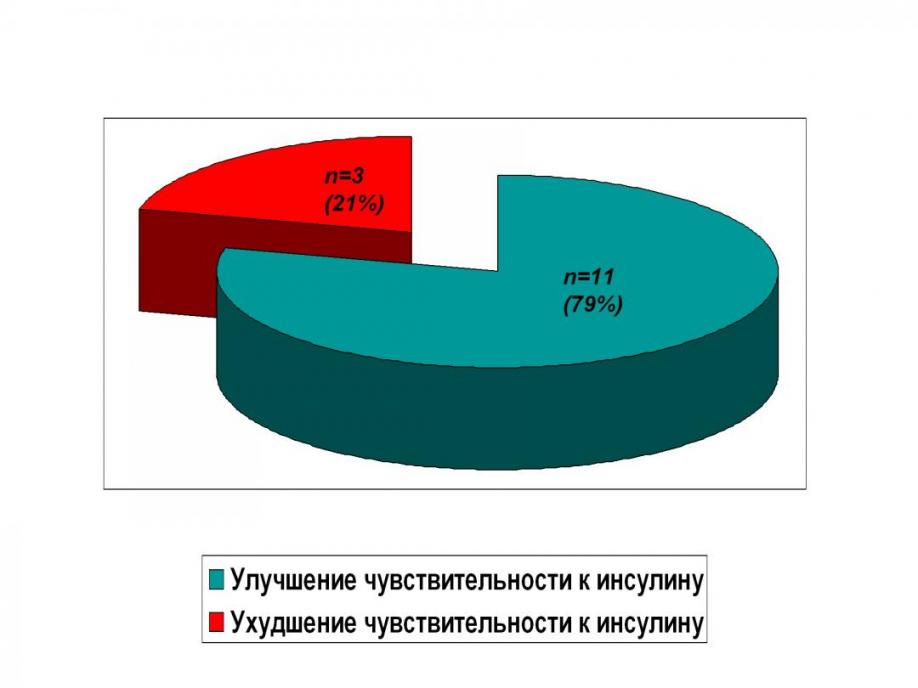
Рис.5 Количество больных СД 2 типа и ИБС с улучшением и ухудшением инсулинорезистентности (по результатам клэмп-теста) при переходе с атенолола на небиволол.
В то же время у 2-х больных инсулинорезистентность незначительно увеличилась, а еще у 1-го больного нарастание инсулинорезистентности было весьма выражено. Полученные данные свидетельствуют о том, что улучшение NO- активности под влиянием небиволола благоприятно воздействует на механизмы формирования инсулинорезистентности, свойственные большинству больных СД2. Отсутствие этого эффекта у ряда больных может быть связано с тем, что в формировании инсулинорезистентности у данных больных участвуют и другие, менее широко распространенные факторы.
После отмены небиволола в течение длительного времени сохранялись проявления уменьшения инсулинорезистентности (рис.6)
Предположительно, механизм снижения уровня ТГ у больных СД2 следующий: за счет дополнительного синтеза монооксида азота в эндотелии сосудов периферический кровоток может увеличиваться, способствуя снижению уровня ТГ. Кроме того, за счет бета-блокирующих свойств, небиволол тормозит липолиз в жировой ткани, снижая концентрацию свободных жирных кислот в плазме крови и уменьшая их участие в синтезе триглицеридов в печени (William-Olsson et al., 1979). Оба механизма способствуют увеличению утилизации глюкозы тканями организма и снижению проявлений инсулинорезистентности.
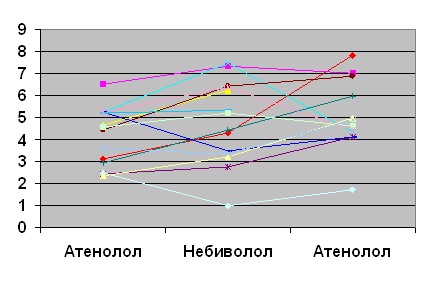
Рис. 6. Изменение инсулинорезистентности на фоне приёма небиволола и при его отмене у больных СД 2 типа и ИБС (по данным клэмп-теста).
Замена атенолола на небиволол и обратно не привела к достоверным изменениям липидного профиля и уровня гликозилированного гемоглобина, хотя отмечалась тенденция к уменьшению НВА1С.
Не было отмечено и существенных изменений в "ишемическом пороге": достоверно не изменились продолжительность теста, уровень «двойного произведения», количество потребляемого кислорода и выделяемого углекислого газа на пике нагрузки.
Учитывая, что оба препарата относятся к селективным бета1- адреноблокаторам это вполне объяснимо. Принципиальное воздействие через бета1-блокирующий эффект на коронарную перфузию и инотропные свойства миокарда у этих препаратов и должно быть сопоставимо.
Влияние дополнительных, NO-модулирующих свойств небиволола на показатели стресс-теста тем не менее было обнаружено. При анализе величины прироста максимального потребления кислорода при переходе на небиволол и величины снижения его потребления при отмене небиволола была отмечена достоверная корреляционная взаимосвязь между этими величинами (рис. 7).
Разность по потреблению
кислорода, мл/мин p=0,002

Рис. 7. Изменение разности потребления кислорода при проведении стресс-спироэхокардиографии у больных СД 2 типа и ИБС на фоне приёма и отмены небиволола.
Подобные достоверные взаимосвязи были обнаружены и для показателей максимального выделения углекислого газа (рис. 8) и для суммарного показателя метаболического эквивалента (МЕТ) (рис. 9), отражающего потребление кислорода на килограмм массы и величину площади поверхности тела больного.
Разность по выделению
углекислого газа, мл/мин p=0,000

Рис.8 Изменение разности выделения углекислого газа при проведении стресс-спироэхокардиографии у больных СД 2 и ИБС на фоне приёма и отмены небиволола.
Разность по МЕТ, мл/кг/мин p=0,002
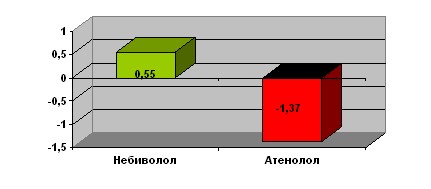
Рис.9 Изменение разности метаболического эквивалента при проведении стресс-спироэхокардиографии у больных СД 2 типа и ИБС на фоне приёма и отмены небиволола
Указанные взаимосвязи свидетельствуют о том, что небиволол реально воздействует на показатели, участвующие в тканевом газообмене при физической нагрузке у больных СД 2, имеющих ИБС, возможно, за счет усиления интенсивности окислительных процессов, а не за счет увеличения потребления кислорода в целом. В результате достигается в большей мере эффективность его использования и уменьшается кислородная задолженность тканям организма. Полученные результаты проведенного исследования косвенно подтверждают такое предположение.
Было обнаружено, что на фоне приема небиволола максимальное выделение углекислого газа при физической нагрузке достоверно обратно коррелирует с величиной инсулинорезистентности, рассчитанной по величине потребления глюкозы данным больным в условиях постоянной инфузии инсулина и глюкозы (клэмп-тест) (рис.9).
Выделение углекислого газа, мл/мин
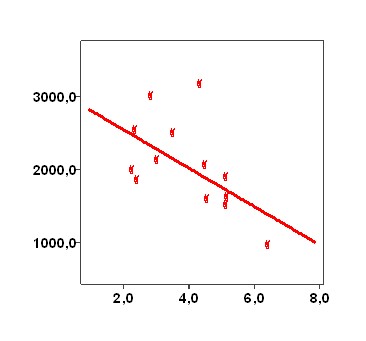
М-индекс, мг/кг/мин.
Рис. 9. Взаимосвязь показателя инсулинорезистентности с выделением углекислого газа при проведении стресс-спироэхокардиографии у больных СД 2 типа и ИБС (r= - 0,56; p=0,04; n=13).
Чем лучше утилизируется глюкоза, т.е. чем меньше проявляет себя инсулинорезистентность, тем интенсивнее работает кардио-респираторная система, интенсифицируя процессы окисления и выделения углекислого газа.
Эти особенности влияния небиволола на уменьшение выраженности тканевой гипоксии нашли свое отражение в достоверном увеличении переносимости миокарда ишемии, индуцированной стресс-тестом. (рис.10). Обращает на себя внимание "эффект последействия" приема небиволола. После его отмены и возвращения к терапии атенололом степень депрессии сегмента ST увеличилась, но достоверно не вернулась к исходному значению.
Депрессия сегмента ST, мм p=0,003 p>0,1
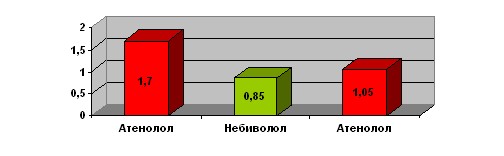
n=14 (n=12) (n=12)
Рис.10. Величина депрессии сегмента ST при нагрузке у больных СД 2 типа и ИБС на фоне приёма и отмены небиволола.
В то время же время наблюдалось достоверное уменьшение индекса нарушения сегментарной сократимости левого желудочка (рис.11) с достоверным увеличением этого показателя после возобновления приема атенолола.
Индекс нарушения локальной сократимости
на пике тредмил-теста, усл. ед.
p=0,007 p=0,022
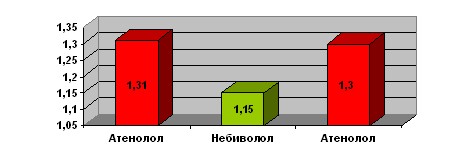
(n=14) (n=12) (n=12)
Рис.11. Снижение индекса нарушения локальной сократимости на нагрузке у больных СД 2 типа и ИБС на фоне приёма и отмены небиволола.
На основании полученных результатов можно предположить, что эффективнось препаратов, используемых для лечения ИБС, но при этом меняющих чувствительность тканей к инсулину у больных с СД2 более выражена.
В связи с этим у пациентов с СД2 и ИБС определялся коронарный резерв и изучалась взаимосвязь этого показателя с метаболическими и функцональными возможностями диабетического сердца при ИБС.
Влияние коронарного резерва сердца на показатели инсулинорезистентности и функциональные возможности миокарда у больных СД2, имеющих ИБС
Под коронарным резервом сердца (КР) понимают возможность коронарной сосудистой сети увеличивать объемный кровоток соизмеримо запросам миокарда в конкретной гемодинамической ситуации (А.В. Врублевский, 2007). В норме этот показатель для артериального звена составляет 2-3 усл.ед (D. Baumgart, 1998; А.В.Врублевский, 2007).
В целях изучения КР, важнейшего фактора в формировании кардиального прогноза при ИБС пациентам из протокола 3, принявших участие во 2 этапе исследования исходно проводилась чреспищеводная доплерографическая оценка КР в коронарном синусе и в правой нисходящей артерии (ПНА). Коронарный синус является венозным коллектором левой коронарной артерии левого желудочка (ЛКА) и является самым информативным показателем уровня коронарного резерва сердца (Врублевский А.В., 2007). Средний уровень КР в коронарном синусе у включенных в исследование пациентов с СД 2 и ИБС составил 1,4±0,7 усл.ед.
Изменение этого показателя в коронарном синусе при смене бета-блокаторов достоверно не произошло, хотя рост КР на фоне приема небиволола наблюдался у 75% пациентов. Уменьшение инсулинорезистентности по данным М-индекса под воздействием небиволола так же не достигло статистической значимости (табл. 11).
Средние значения показателей инсулинорезистентности и коронарного резерва коронарного синуса до, во время и после приема небиволола (М±m)
Табл.11
| Показатели | На фоне атенолола | На фоне небиволола | На фоне атенолола |
| М-индекс (усл.ед) | 4,1±0,4 | 4,7±0,5 | 5,2±0,5 |
| Коронарный резерв в коронарном синусе (усл.ед) | 1,4±0,7 | 1,8±0,5 | 1,5±0,6 |
Статистические различия между средними значениями указанных показателей по Mann-Whitney не являются достоверными (р>0,1)
Однако при оценке взаимосвязи КР в коронарном синусе и М-индексом на фоне приема небиволола была получена достоверная связь (р=0,04,r=-0,883), не полученная на фоне исходной и последующей терапии атенололом. Т.е. наличие NO-модулирующей активности позволяет небивололу активно "вмешиваться" во взаимоотношения инсулинорезистентности и КР: наблюдается улучшение чувствительности к инсулину и увеличение коронарного резерва (Рис.12)
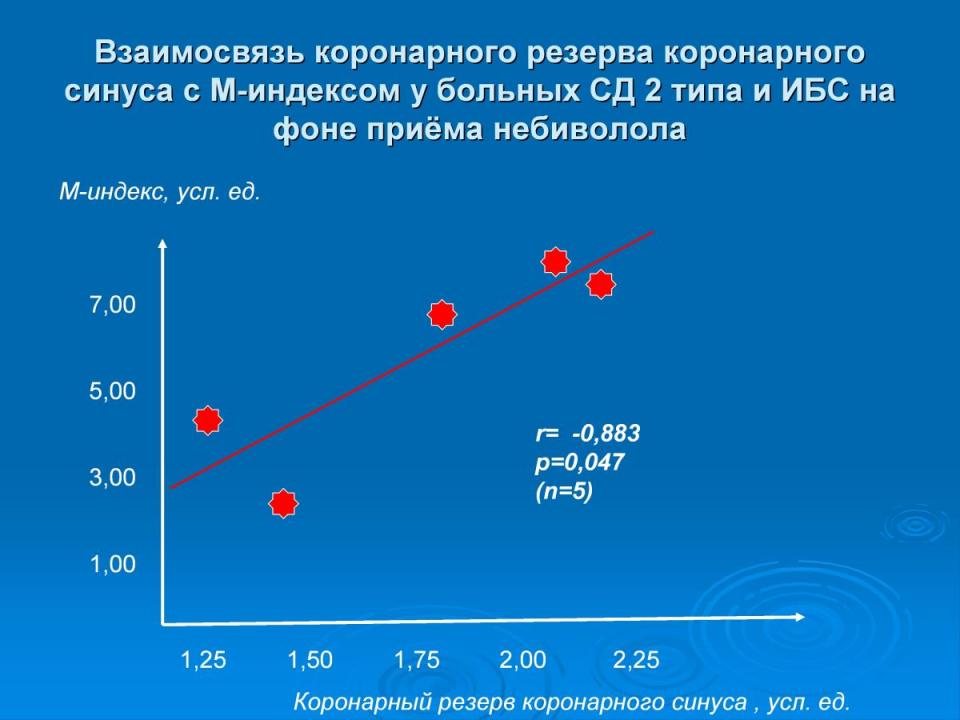
Рис. 12 Изменение коронарного резерва и инсулинорезистентности на фоне приема небиволола
При сравнении величины коронарного резерва в ПНА у больных СД с показателями работоспособности сердца на пике стресс-теста виде «двойного произведения» была получена высоко достоверная корреляционная взаимосвязь(p=0,013,r=0,858). Интересно, что величина коронарного резерва не коррелировала с выраженностью нарушений локальной сократимости левого желудочка (p=0,285;r=-0,432) и со степенью максимальной депрессии интервала ST на ЭКГ (p=0,208; r=-0,543).
Таким образом, при СД 2 показатели работоспособности миокарда формируются под воздействием как гемодинамических, так и метаболических показателей. Использование препарата, сочетающего свойства селективной 1- адреноблокады с NO-модулирующей активностью (небиволола), у больных СД 2, страдающих артериальной гипертонией и ишемической болезнью сердца обладает рядом метаболических и клинических преимуществ по сравнению с селективными 1-адреноблокаторами, не изменяющими активность эндотелиального оксида азота.
2. Кардиальные последствия применения препаратов сульфанилмочевины.
В рамках оптимизации выбора лекарственной терапии, применяемой для лечения больных с СД 2 и ИБС было изучено влияние препаратов сульфанилмочевины, наиболее часто используемых в отечественной диабетологии
С этой целью обследовано 45 пациентов, у которых наличие ИБС подтверждено с помощью стресс- спироэхокардиографии. Из них было отобрано 16 пациентов (9 мужчин, 7 женщин, средний возраст 56,5±6,9 лет) с воспроизводимой ишемической депрессией сегмента ST, индуцированной нагрузкой на тредмиле (см. протокол 3)
Клиническая характеристика представлена в табл. 12
Табл. 12
Клиническая характеристика обследованных пациентов (M±m)
| Показатели | Пациенты, принимавшие амарил (п=16) |
| Возраст (годы) | 56,5±1,8 |
| Мужчины/женщины | 9/7 |
| Индекс массы тела (кг/м) | 28,4±0,7 |
| Длительность СД(годы) | 7,4±1,1 |
| САД мм.рт.ст | 135,3 + 17,4 |
| ДАД мм.рт.ст | 82,5 + 8,7 |
У 6 больных диагностирована стенокардия напряжения II функционального класса, (по классификации Канадской ассоциации кардиологов). У 10 больных выявлена безболевая ишемия миокарда.
Мягкая и умеренная артериальная гипертония обнаружена у 13 пациентов. У 10 больных она была связана с наличием гипертонической болезни 1-2 стадии, у 3 – с диабетической нефропатией без нарушения азотовыделительной функции почек.
До включения в исследование все пациенты для коррекции углеводного обмена принимали пероральные сахароснижающие препараты. У 7 больных проводилась монотерапия препаратами из группы сульфанилмочевины. Из них 6 человек получали глибенкламид (манинил) и 1 человек – гликлазид (диабетон). Комбинированную терапию препаратами сульфанилмочевины и бигуанидами получали 9 пациентов. Из них 6 человек принимали глибенкламид с метформином и 3 человека - гликлазид с метформином (табл. 13).
Табл.13
Показатели углеводного и липидного обмена, уровень суточной микроальбуминурии у больных сахарным диабетом 2 типа с коронарной болезнью сердца (M + SD)
| Биохимические показатели | Исходная терапия | Терапия амарилом | Исходная терапия |
| 1 | 2 | 3 | |
| Глюкоза, ммоль/л Гликозилированный гемоглобин (%) Триглицериды ммоль/л Общий ХС ммоль/л ХС ЛНП ммоль/л ХС ЛВП ммоль/л Суточная микроальбуминурия, мг/сутки | 8,5 + 1,9 8,2 + 1,5 2,0 + 0,8 5,7 + 1,1 3.3 + 1,1 1,4 + 0,3 110,0 + 311,9 | 9,9 + 2,9 7,9 + 1,3 2,0 + 0,7 5,6 + 1,0 3.3 + 0,9 1,4 + 0,3 | 9,6 + 2,3 8,0 + 1,2 2,0 + 0,7 5,6 + 1,0 3.3 + 0,9 1,3 + 0,3 |
| * - p1 и 2 < 0,05 достоверное различие между 1 и 2, ** - p2 и 3 <0,05 достоверное различие между 2 и 3. ХС – холестерин, ЛНП – липопротеиды низкой плотности, ЛВП – липопротеиды высокой плотности. | |||

